文献解读|Cell(42.5):马来西亚半岛原住民的同心毛癣菌真菌感染和皮肤微生物组
✦ +
+
论文ID
原名:Trichophyton concentricum fungal infections and skin microbiomes of Indigenous Peninsular Malaysians
译名:马来西亚半岛原住民的同心毛癣菌真菌感染和皮肤微生物组
期刊:Cell
影响因子:42.5
发表时间:2025.06.26
DOI号:10.1016/j.cell.2025.05.034
背 景
近期暴发的多重耐药真菌感染人类皮肤,凸显了了解真菌病理生理学和传播机制的重要性。为了解决马来西亚半岛原住民(Orang Asli,OA)的健康问题,一种名为毛癣菌(Trichophyton concentricum)的真菌性皮肤感染—叠瓦癣菌(tinea imbricata)—引起了特别关注。OA患者的叠瓦癣临床治疗通常包括一线经济有效的抑菌唑类药物,常与皮质类固醇联合使用。患有广泛性、顽固性叠瓦癣感染的患者通常需要住院长期服用 特比萘芬(TRB),TRB 是 FDA 批准用于治疗甲真菌病(趾甲真菌感染)的二线抗真菌药物。OA患者的叠瓦癣的治疗监测受到地理和人口统计学障碍的影响,包括他们的半游牧生活方式和不受限制地获得非处方外用抗真菌药物。过去 5 年,在特定村庄已记录了两次大规模干预措施,但未进行抗真菌耐药性检测或长期随访。最近在五个马来西亚半岛原住民村庄进行了一项关于皮肤病及其相关危险因素的流行病学研究,发现真菌感染和疥疮等疾病的患病率很高。对叠瓦癣菌和皮肤微生物组的分析可以为这种独特的疾病提供重要的见解。
实验设计
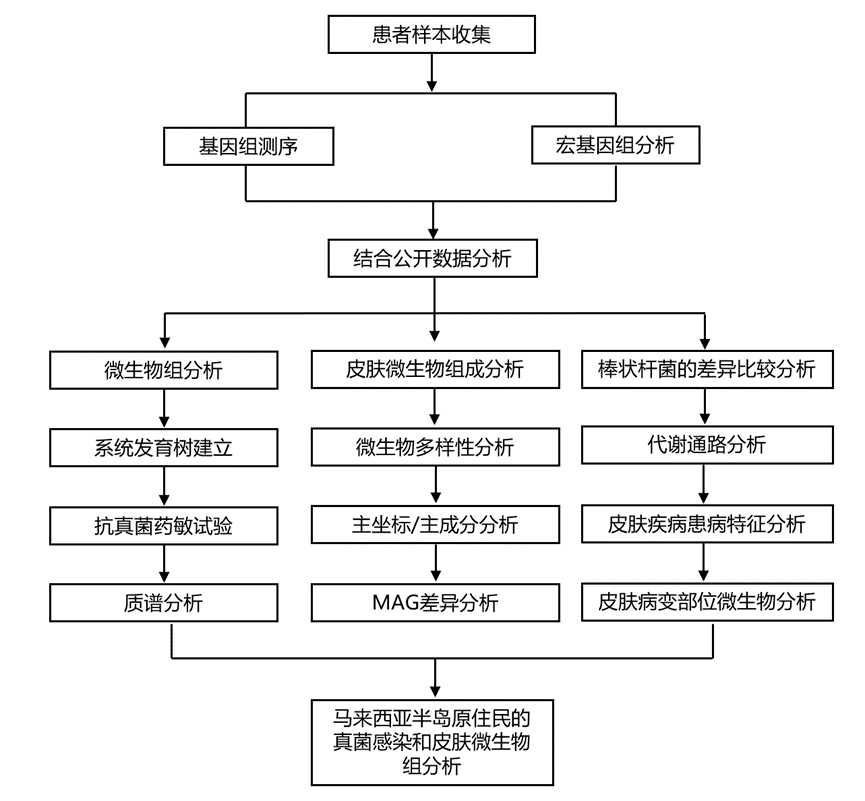
结 果
01
OA患者的叠瓦癣感染
在研究团队对马来西亚半岛原住民开展临床流行病学工作期间,社区成员报告称,他们担心慢性圆形鳞状皮疹会影响他们身体的大部分区域,有些病例从儿童时期就开始出现。这些皮肤病变的独特模式是叠瓦癣的特征性症状(图 1 A)。在过去的二十年中,研究团队与OA患者群体和当地领导人密切合作,尤其是在原住民健康领域。在提供医疗保健的背景下,临床研究最初侧重于了解 OA 人群中流行的寄生虫感染。随后,合作关系扩展至以社区为基础的疾病预防健康教育。本研究是一个关键案例,展示了 OA 患者群体和研究人员如何共同设计一项研究,OA 患者群体将复发性皮肤感染和叠瓦癣的传播确定为两大临床和社会问题。2022 年 3 月至 2023 年 3 月期间,他们招募了 82 名 OA 患者(63 名成人和 19 名儿童),他们居住在 5 个不同的地点(根据处理/未处理水、月收入、距离市中心的距离和出入方式,按城市化程度排序,依次为 F、D、G、AB 和 C 村),参与了这项关于皮肤感染的研究。超过一半的 OA 患者属于巴特克人,他们是居住在彭亨州和吉兰丹州塔汉山脉沿线的尼格利陀部落,可能代表了马来西亚半岛最后的半游牧土著群体之一。根据直接从受影响皮肤采集的刮屑的特征性临床形态和氢氧化钾 (KOH) 染色中存在的菌丝,20 例患者诊断患有叠瓦癣(图1A-B),随后在菌胶琼脂上培养并对真菌标记区(内部转录间隔区 [ITS]1 和 ITS2)进行基因组测序和微生物组分析,证实分离株为同心叠瓦癣菌(同心毛癣菌)。
MALDI-TOF 质谱法已用于经认证的临床实验室的真菌鉴定,但是它依赖于与参考光谱的匹配。当他们检测同心叠瓦癣菌 (T. concentricum)分离株时,突显了当前光谱数据库在皮肤癣菌鉴定方面的局限性,同心叠瓦癣菌分离株显示出低置信度的光谱匹配。这些同心叠瓦癣菌分离株现在有助于扩展 MALDI-TOF 参考数据库,从而提高未来临床诊断的准确性和效率。对这些T. concentricum基因组的数据分析表明,虽然地理来源各异,但其一致性很高,变异率很低,这与区域性疫情相一致。由于缺乏其他现有的T. concentricum基因组测序,因此无法计算全球多样化程度。这 42 个 OA 衍生分离株表现出 99.9% 的平均核苷酸同一性 (ANI) 和 253 个 SNP,总共观察到 1397 个 SNP,表明即使从居住在相距最远 440 公里的村庄的受试者中培养,也存在遗传相似性。通过系统发育分析揭示了从 OA 村庄获得的分离株的遗传结构。具体而言,来自村庄 AB、D 和 F 的分离株形成不同的聚类,而来自最大的村庄 C 的分离株形成两个不同但密切相关的聚类(图 2 A-B)。
为了评估抗真菌药物的疗效和潜在的耐药性发展,他们对八种外用和全身抗真菌药物进行了抗真菌敏感性测试,包括氟康唑、酮康唑、咪康唑、伊曲康唑、伏立康唑、TRB、灰黄霉素和环吡酮酮。总体而言,大多数分离株对三唑类药物、伊曲康唑和伏立康唑的最低抑菌浓度 (MIC) 较低(几何平均 [GM] MIC 范围:0.125 至 2 μg/mL)(图 2C)。正如预期的那样,氟康唑的 MIC 高于其他唑类药物(≥16 μg/mL)。咪唑类药物(咪康唑和酮康唑)的 MIC 升高,GM MIC 分别为 2 和 6 μg/mL。酮康唑的MIC也较高,范围为2至8 μg/mL,表明与其他抗真菌药物相比,其对分离菌的有效性较低。用于治疗皮肤癣菌感染的外用抗真菌药物环吡咯酮的MIC范围为0.5至1 μg/mL,这与先前关于其抗皮肤癣菌功效的研究结果一致。灰黄霉素的 MIC 范围为 0.5 至 4 μg/mL,而烯丙胺 TRB 的 MIC 范围为 0.031 至 2 μg/mL。虽然尚未确定同心毛癣菌和其他皮肤癣菌的临床断点或流行病学截断值,但研究表明,TRB 的 MIC ≥ 0.25 μg/mL 可能表明在具有临床重要性的、系统发育相关的毛癣菌种中存在非野生型表型。该 MIC 阈值可能反映了靶基因 SQLE 的突变,表明 15% 的分离株对 TRB 的敏感性降低。这些分离株也表现出升高的伊曲康唑 MIC(≥0.5 μg/mL)。值得注意的是,TRB的MIC升高仅限于来自C村的分离株,特别是来自同居配偶的C07和C08受试者,这引发了人们对可能出现获得性耐药性的担忧。
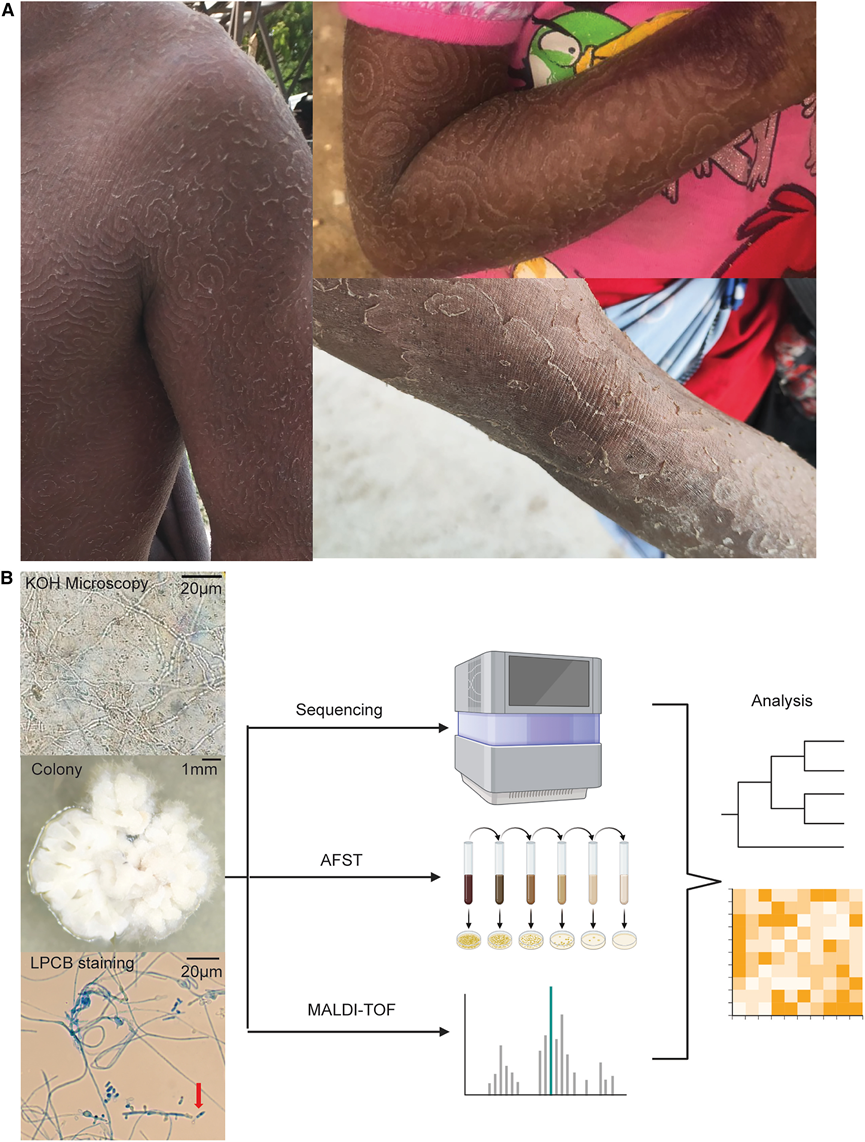
图1. 原住民中的癣菌。
(A) 原住民叠瓦癣的临床表现,具有广泛的同心鳞状环和层状鳞屑。(B) Trichophyton concentricum菌株的微生物特征和基因组特征示意图。
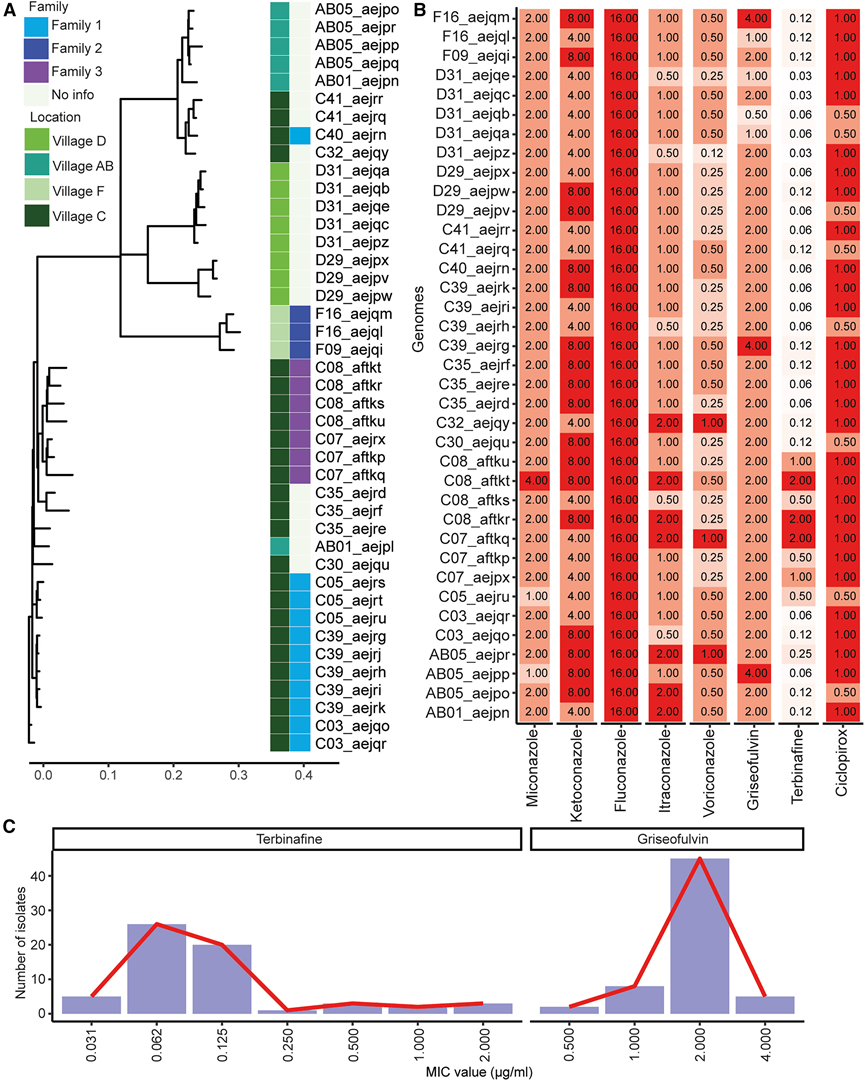
图2. T. concentricum在其基因组和抗真菌药物敏感性方面存在变异。
(A) 来自居住在4个村庄(包括3个家庭单位)的OA个体的T. concentricum分离株的系统发育树。(B) 热图显示T. concentricum分离株的AFST结果。(C) 对多种T. concentricum分离株进行抗真菌敏感性测试后,以原始数据和曲线(红线)形式显示的特比萘芬(左)和灰黄霉素(右)的最低抑菌浓度 (MIC) 结果。
02
土著和城市人口的皮肤微生物组成
为了研究T. concentricum的传播,他们接下来试图探究原住民人群中是否发生了无症状定植。此外,基于T. concentricum对南岛原住民群体的宿主特异性,他们扩大了调查范围,以探索原住民和马来西亚城市人群之间皮肤微生物组组成的差异。对 82 名原住民个体(63 名成人和 19 名儿童)的皮肤样本进行了宏基因组测序,这些样本与T. concentricum培养同时采集(图 3 A)。本项研究还包括来自吉隆坡市中心(n = 23)和华盛顿特区大都市区(n = 12)的健康个体进行比较分析。对来自前额、前臂掌侧和趾蹼的拭子进行了宏基因组测序(图 3 A)。他们从 117 名受试者中生成了总共 1.92 × 10 10 个读段对的宏基因组数据,并对他们的皮肤微生物组进行了读段映射分析。
使用皮肤微生物组基因组目录 (SMGC) 数据库对皮肤微生物组进行初步分类,结果显示 OA 样本的分类率低于城市样本;华盛顿特区样本的平均分类率为 75.10% ± 14.22%,而 C 村样本的平均分类率仅为 36.98% ± 13.63%,这表明需要扩大参考基因组集合,以更好地代表未充分探索群体中的微生物变异。为此,他们采用基于组装的方法,重建宏基因组组装基因组 (MAG)图谱,共产生了 1796 个原核 MAG 和 210 个真核 MAG。原核MAG主要归类为放线菌门、假单胞菌门、拟杆菌门和芽孢杆菌门(图S2 A),而真核MAG均归类为真菌,包括毛癣菌属和马拉色菌属。对这些马来西亚MAG(653个原核生物,17个真核生物)进行进行聚类,得到了一个包含来自马来西亚人群的437个MAG的全面的新微生物基因组目录(图S2 A)。将OA和吉隆坡宏基因组读段与本研究定义的基因组目录进行分类,可对61.44% ± 18.99%的序列进行分类(图S2 B),较单独使用SMGC数据库获得的46.10% ± 22.03%的分类准确率有显著提高(图S2 B)。因此,这些数据有助于扩展人类皮肤微生物组库。
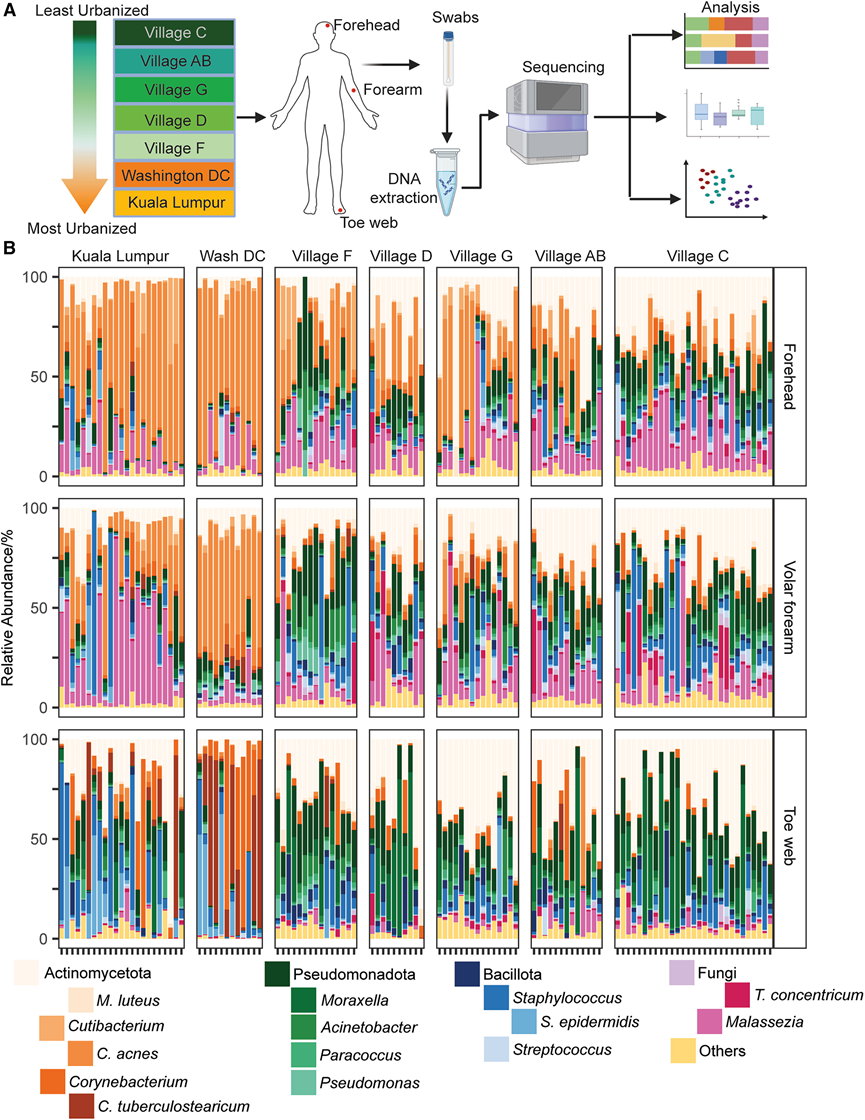
图3. OA 患者和马来西亚城市居民的皮肤微生物组。
(A)实验流程图。(B) 居住在城市(吉隆坡、华盛顿特区)和OA村的参与者的皮肤微生物组多界相对丰度。
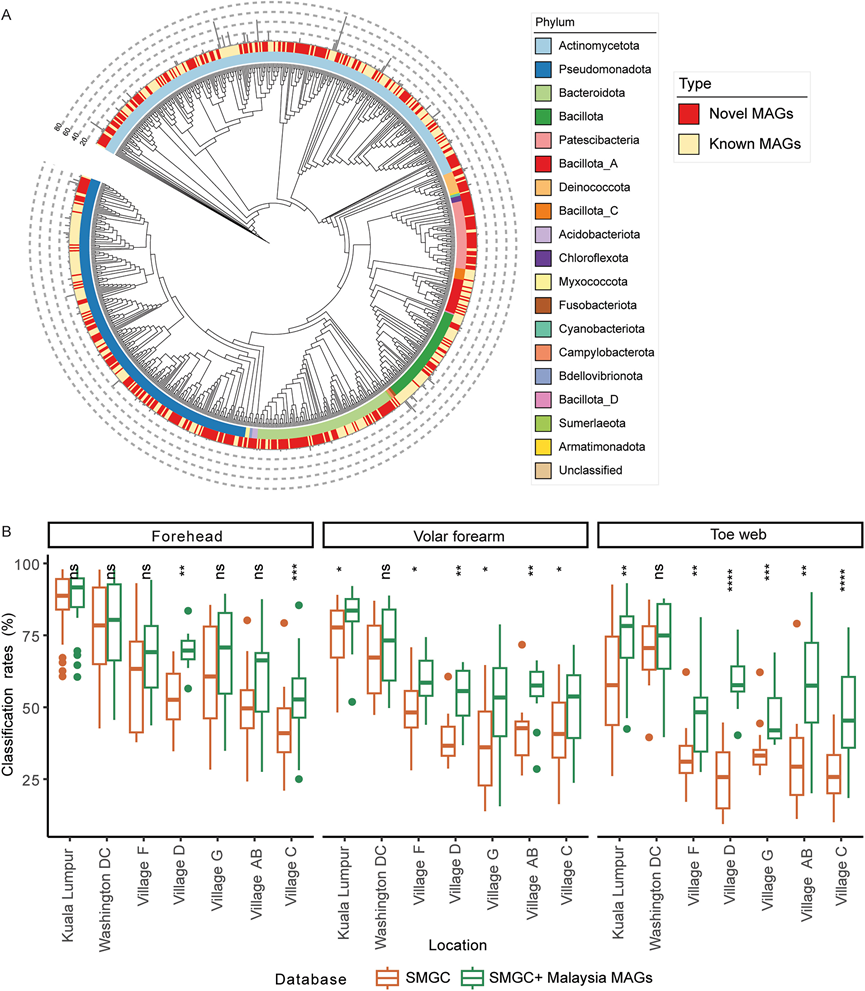
图S2. 将马来西亚 MAG 与 SMGC 数据库相结合可提高映射率。
(A) 本研究中原核生物MAG的系统发育树。(B)箱线图比较了 SMGC 和 SMGC +马来西亚数据库的映射率。
03
马来西亚半岛原住民的独特皮肤微生物组特征和变异
为了探究城市化与皮肤微生物组多样性之间的关系,他们分析了按村庄分组的OA受试者的物种水平α和β多样性。总体而言,与城市居民相比,马来西亚半岛原住民表现出统计学上显著更高的α多样性(图4 A)。C村的多样性最高(4.47±1.24),其次是AB村(4.15±1.33),几乎是吉隆坡地区(2.49±1.22)和华盛顿特区(2.42±1.29)的两倍。此外,主坐标分析(PCoA)显示马来西亚半岛原住民与城市居民之间的微生物存在明显的隔离(图4 B)。值得注意的是,在排序图上,城市化程度最低的地区(村庄C)距离城市样本(吉隆坡和华盛顿特区)最远(图4 B),这表明城市化生活方式的梯度变化以及OA人群中微生物组多样性的相应变化。对马来西亚半岛原住民和城市居民的微生物组数据进行主成分分析(PCA)(图4 C)显示,其分布由底层微生物组中的3或4个特征(分类单元)决定,其中一个组对应于城市人口,两个不同的组分别代表半城市化(村庄F和村庄D)和城市化程度最低(村庄AB和村庄C)的OA样本。发展指标包括厕所的存在、参与森林活动(狩猎/清道夫)、河流活动(游泳和钓鱼)和村庄状况,表明这些因素在单变量、多变量和交互模型中协同调节皮肤微生物组景观(图S3A-B)。村庄状况尤其值得注意,因为搬迁的村庄通常拥有更好的基础设施并且更靠近城市地区,而内陆村庄则更为偏远。此外,工业化程度较低的马来西亚半岛原住民往往比城市居民显示出更高的微生物物种数量(图S3C)。这些研究结果强调,城市化水平的提高导致接触自然环境的减少和接触加工食品和化学物质的增加,这似乎与不同身体部位的微生物群落组成的明显变化有关。
然后,他们试图确定导致马来西亚半岛原住民和城市居民之间观察到的差异的关键分类单元。在 PCA 上,痤疮丙酸杆菌始终是这种组间变异的主要贡献者,无论是在前额还是前臂掌侧部位(图 4 C)。同样,皮肤共生菌结核分枝杆菌和表皮葡萄球菌是城市化人群趾蹼中微生物组特征的主要贡献者。值得注意的是,结核分枝杆菌的相关系数非常高,在高度城市化的华盛顿特区达到 0.51,在城市化程度最低的村庄(村庄 C)为 -0.51。同样,表皮葡萄球菌与城市人口呈现出很强的正相关性,吉隆坡的系数为 0.34,华盛顿特区的系数为 0.28,而村 C 的系数为 -0.21,村 D 的系数为 -0.24。总之,这些结果确定了与城市化相关的皮肤细菌,与传统的、城市化程度较低的社区相比,痤疮梭菌、结核杆菌和表皮葡萄球菌在现代工业化环境中占主导地位。
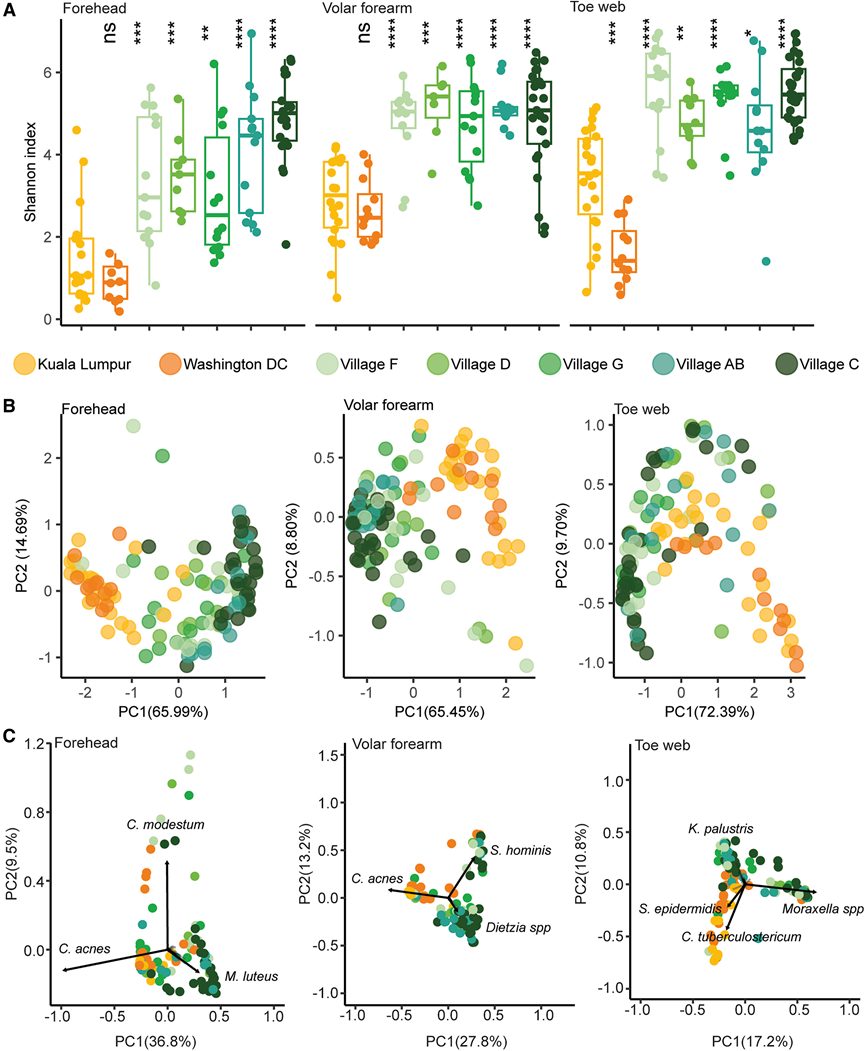
图4. 马来西亚半岛原住民的皮肤微生物组具有更高的微生物多样性。
(A) 箱线图展示了以香农多样性指数(Shannon Diversity Index)分析的各村庄皮肤微生物组(前额、前臂掌侧和趾蹼)的 α 多样性。(B) 基于来自不同地理位置的样本的Bray-Curtis距离的皮肤微生物组谱(物种水平)的主坐标分析(PCoA)。(C) 对前额、前臂掌侧和趾蹼的物种水平微生物组数据进行主成分分析。
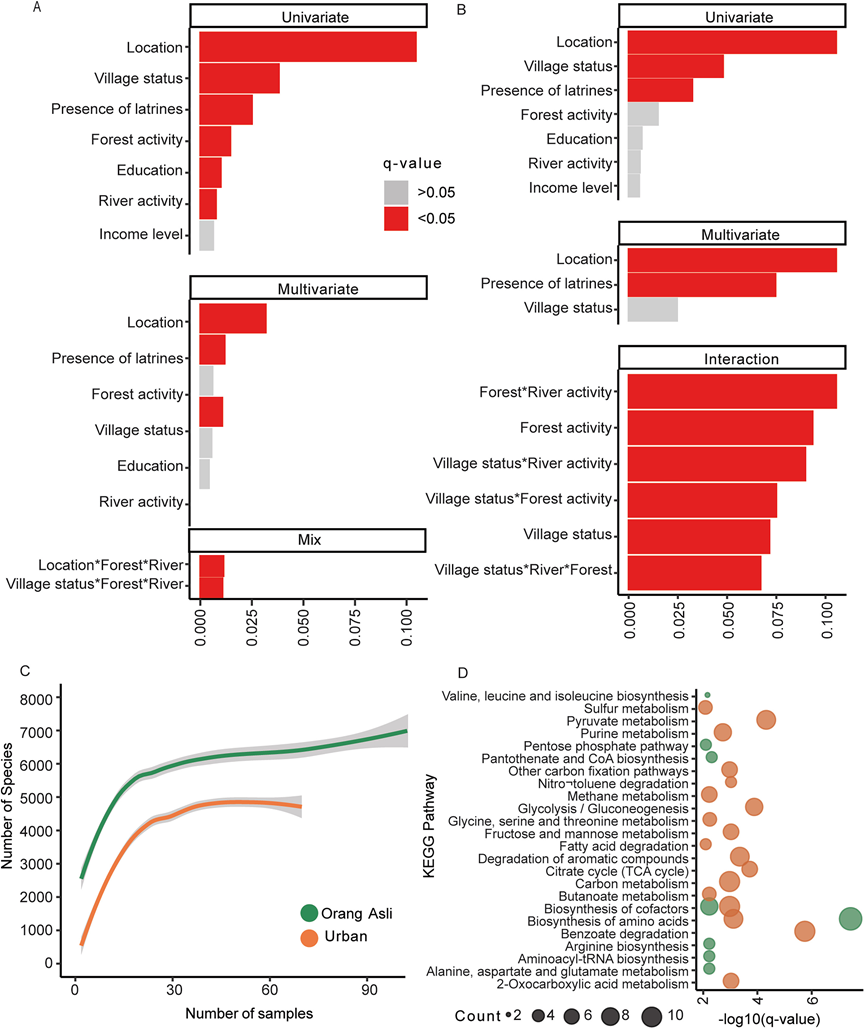
图S3. 城市化对宿主皮肤微生物组、物种多样性和功能途径的影响。
(A) 条形图显示皮肤样本 PERMANOVA 分析的效应大小,按模型类型(单变量、多变量或混合/交互作用)分层。(B) 条形图显示皮肤样本MDMR分析的效应大小,按模型类型(单变量、多变量或混合/交互作用)分层。(C) 阿尔法稀疏曲线显示了不同 OA 种群(绿色)和城市(吉隆坡和华盛顿特区,橙色)中物种丰富度( y轴)随样本数量(x轴)增加而变化的情况。(D)差异富集通路。
04
OA中棒状杆菌的比较研究
为了探索马来西亚半岛原住民人群中发现的细菌菌株和物种之间的遗传变异,他们研究了棒状杆菌属,该属在人类皮肤中很常见,此前已证明其表现出洲际菌株水平的基因组差异。本研究共回收了 31 个完整、接近完整和高质量棒状杆菌MAG,其中大多数来自 OA 并与其他参考基因组有相当大的距离(图 5A)。这些新型棒状杆菌MAG 对该属内整体系统发育变异的贡献率为 5.63%,突显了 OA 群体中显著的基因组变异。棒状杆菌MAGs的分布呈现出独特的模式——C. tuberculostericum在城市队列中占主导地位,而一组独特的棒状杆菌种在 OA 队列中占主导地位(图 5 B)。
使用差异丰度线性模型 (LinDA) 方法对城市和马来西亚半岛原住民人群之间差异丰度的棒状杆菌MAG进行比较基因组分析,揭示了不同的功能富集。在 OA 中相对丰度较高(“OA 富集”)的棒状杆菌MAG 富集与能量代谢(甲酸转运蛋白C4-二羧酸转运蛋白)、细胞壁合成(甘露糖依赖性 α-(1-6)-甘露糖基转移酶和还原酶 FabG)和铁吸收调节(铁依赖性阻遏物 IdeR)相关的基因(图5 C)。相比之下,棒状杆菌属。城市地区相对丰度较高的棒状杆菌(“城市富集”)表现出与耐药性有关的基因的富集,包括大环内酯类输出 ATP 结合/通透酶蛋白 MacB 和多药耐药蛋白 MdtL。城市丰富的棒状杆菌MAG 还显示出更高含量的多胺相关基因,包括多胺氨丙基转移酶(图 5C)。最后,对城市富集和 OA 富集的棒状杆菌进行京都基因和基因组百科全书 (KEGG) 通路的比较分析,揭示了不同的代谢特征。城市丰富的棒状杆菌表现出与局部化合物代谢相关的途径的富集,例如苯甲酸和烟酰胺,以及空气污染物甲烷和芳香族化合物以及其他污染物,包括硝基甲苯(图 S3 D)。相比之下,与城市富集的MAG相比,OA富集的棒状杆菌MAG表现出糖代谢通路的富集,并在氨基酸代谢方面表现出独特的模式。总而言之,与城市丰富的棒状杆菌相比,富含OA的棒状杆菌MAG表现出更大的基因组变异,并参与了不同的代谢通路。
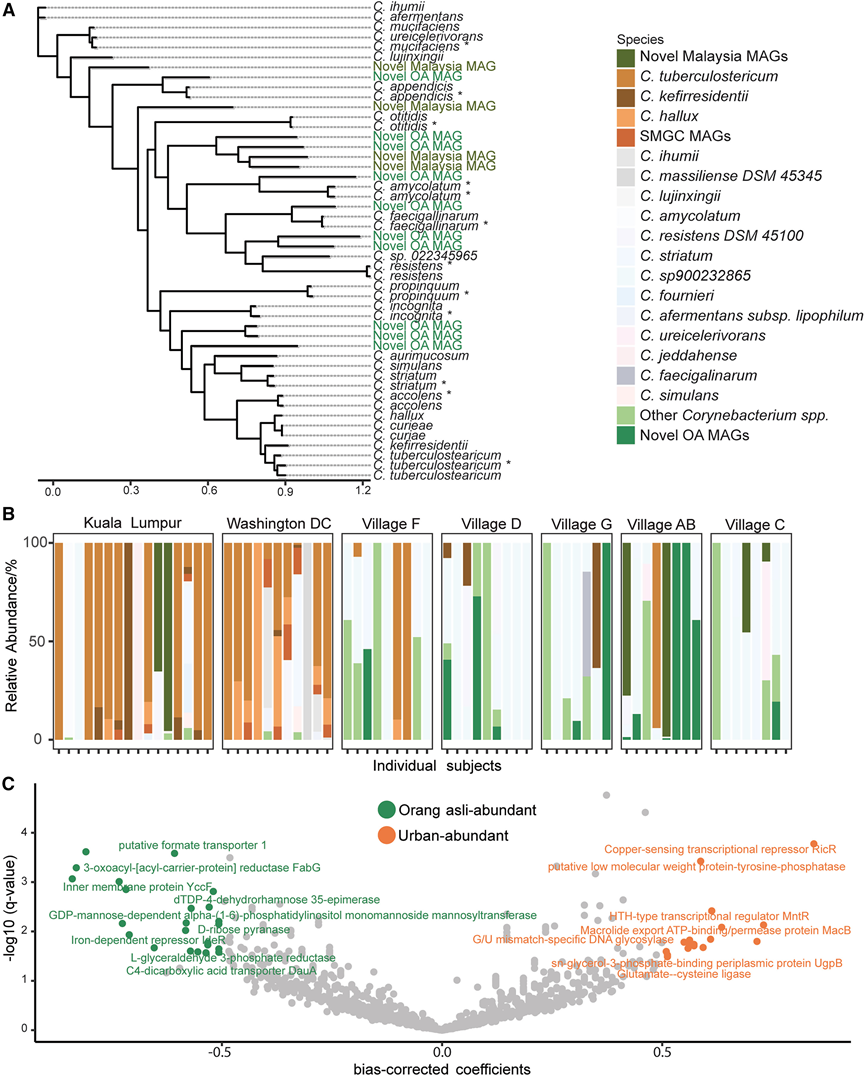
图5. OA村民与城市人群相比,棒状杆菌种群不同,且富含不同的基因组。
(A) 马来西亚样本棒状杆菌MAG及其参考基因组的系统发育树。(B) 趾蹼皮肤微生物群中数量最多的 20种棒状杆菌的相对丰度。(C) 差异丰度线性模型(LinDA)分析图描绘了 OA 和城市棒状杆菌物种中富集的基因。
05
与皮肤疾病相关的皮肤微生物群
在 OA 受试者中,观察到各种皮肤健康状况,包括 22 名健康个体、20 名患有叠瓦癣、16 名患有疥疮和 15 名患有花斑癣,不同地理位置的患病率各不相同(图 6 A)。疥疮是由疥螨侵入皮肤引起的感染,导致剧烈瘙痒的丘疹性皮疹,而花斑癣是由真菌马拉色菌引起的,导致鳞状圆形变色皮肤病变,并伴有轻微瘙痒,在不同皮肤状况的个体中观察到不同的皮肤微生物组组成(图 6 B)。患有叠瓦癣的受试者展示了研究中一个特别有趣的方面,揭示了这种疾病的独特特征和其潜在因素的潜在见解。了解感染遗传易感性的关键问题之一是微生物在多大程度上无症状地定植于个体中。传播网络随着无症状定植而发生巨大变化,这是仅某些微生物的特征(例如,耳念珠菌在无症状的情况下定植于皮肤,这些定植的个体可以传播给他人)。患有叠瓦癣的 OA 患者的样本中T. concentricum的相对丰度中位数为 3.9%,而 OA 健康对照者的前额、前臂和趾蹼上未检测到T. concentricum(图 6 B-C)。受试者T. concentricum的相对丰度在不同身体部位存在差异,前额为0.7%–15.8%(平均4.1%),前臂掌侧为1.2%–42.4%,趾蹼为0.5%–15.8%。此外,与健康对照组相比,患有叠瓦癣的受试者前臂掌侧其他非叠瓦癣真菌的相对丰度更高(图S6A),导致微生物组组成发生改变(图S6B-C)。比较叠瓦癣患者的病变或非病变皮肤和 OA 健康对照者的皮肤,即使在调整年龄、性别、身体部位和位置后,T. concentricum仍然是丰度差异最大的菌种。病变和健康对照样本之间的比较分析显示,叠瓦癣患者中多种共生葡萄球菌的相对丰度增加,包括山羊葡萄球菌、沃氏葡萄球菌和其他菌种(图S6D-E)。然而,皮肤微生物组分析的一个重要发现是,在未诊断患有叠瓦癣的 OA 个体中没有T. concentricum的特征。这些研究表明,与其他叠瓦癣菌种相似,T. concentricum在定植于皮肤后会引起感染,从而降低了无症状定植在未来传播研究中的作用。
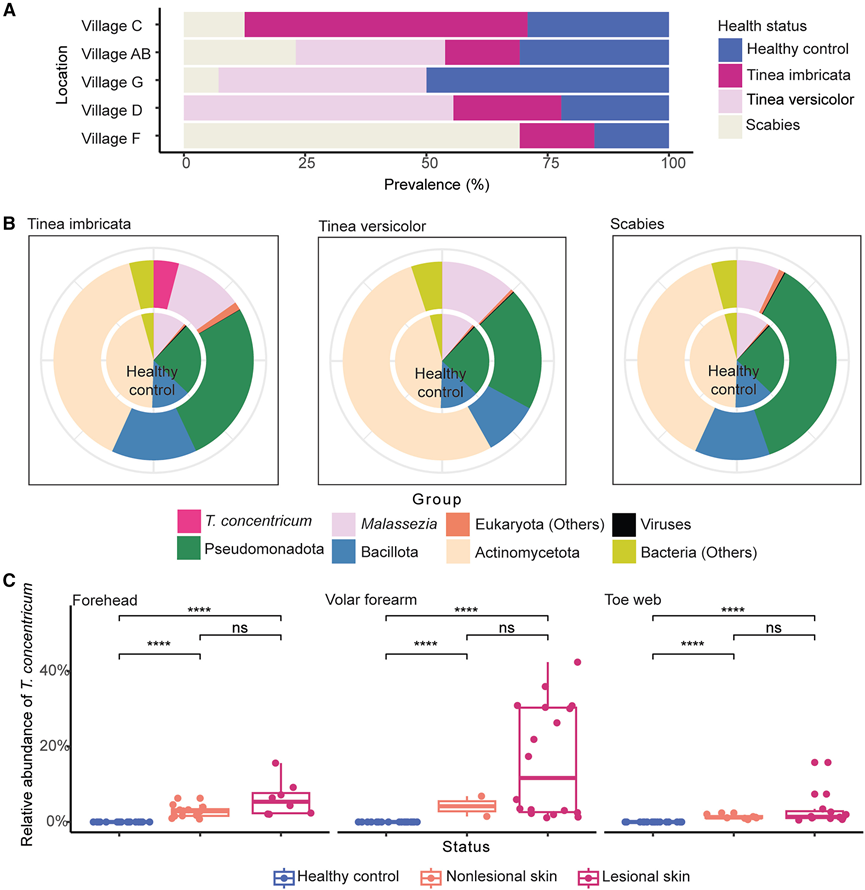
图6. OA 伴皮肤疾病的患病率和皮肤微生物组。
(A) 条形图显示了每个 OA 村皮肤病的患病率。(B) 饼图显示患有叠瓦癣、花斑癣和疥疮(外圈)的患者的皮肤微生物组的门级相对丰度与健康对照组(内圈)的比较。(C) 箱线图描绘了健康对照组与患有叠瓦癣的患者(分为从指示皮肤部位的非病变皮肤和病变皮肤采集的样本)的前额、前臂掌侧和趾蹼T. concentricum的相对丰度。
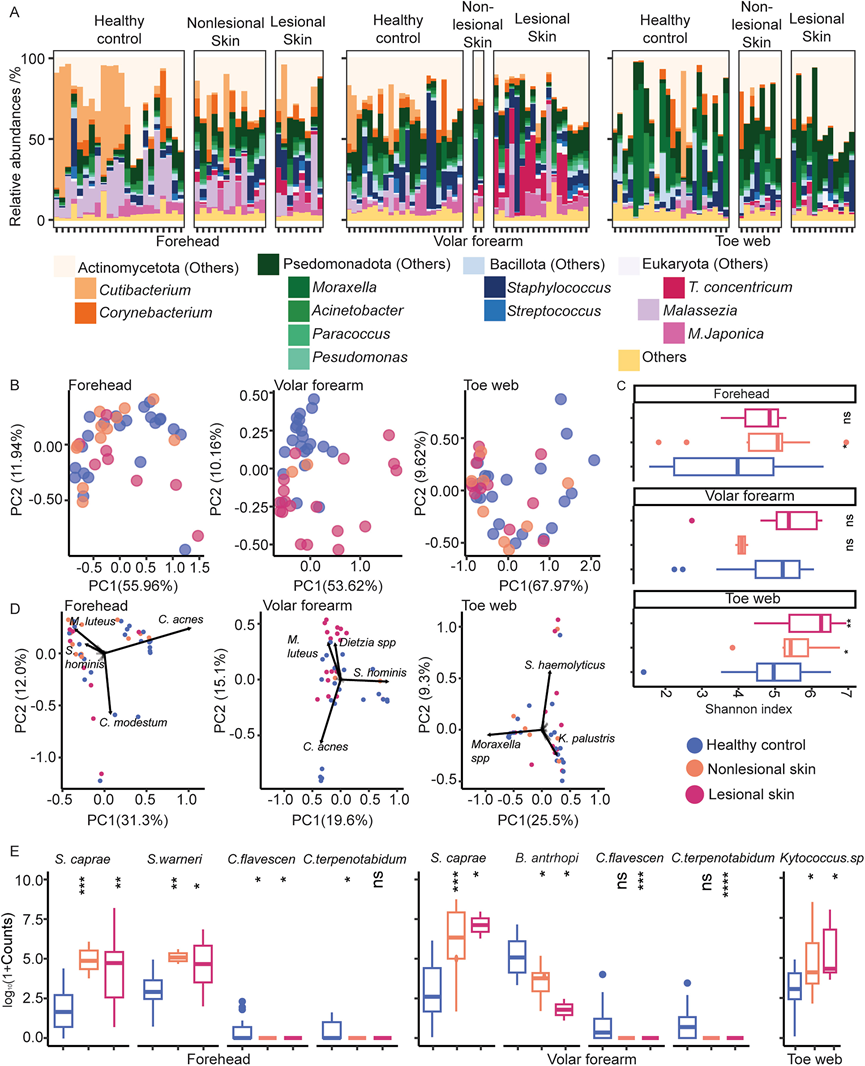
图S6. 患有叠瓦癣的受试者在病变部位和非病变部位的皮肤微生物组组成上存在差异。
(A) 不同疾病状态(健康对照、非病变皮肤和病变皮肤)样本中不同身体部位皮肤微生物组的相对丰度。(B) 散点图显示基于样本皮肤微生物组谱(物种水平)的 Bray-Curtis 距离的 PCoA,不同疾病状态的样本用不同的颜色表示。(C) 基于不同疾病状态和身体部位的 Shannon 多样性指数的 Alpha 多样性箱线图。(D)对物种水平的微生物组数据进行主成分分析。(E) 条形图显示了T. concentricum定植样本和健康对照样本之间丰度差异物种。
+ + + + + + + + + + +
结 论
本研究通过在偏远的马来西亚半岛原住民村庄对T. concentricum分离株进行培养、抗真菌药物敏感性测试和测序,研究了叠瓦癣菌的病因和传播途径。在区域性保守的分离株中,通过微生物学和基因组学方法鉴定了特比萘芬耐药的T. concentricum。通过研究82例本土OA患者的皮肤微生物组,发现OA患者的微生物组独特,且细菌共生菌(痤疮丙酸杆菌、表皮葡萄球菌)的相对丰度较低,这与马来西亚和美国城市人群的差异显著。这些发现为慢性真菌性皮肤感染的临床、微生物学和基因组学特征提供了宝贵的见解,有望为应对耐药性和有效治疗提供策略。
+ + + + +



 English
English


