文献解读|Signal Transduct Target Ther(52.7):多维肿瘤-血液分析揭示垂体神经内分泌肿瘤中系统性淋巴细胞-单核细胞失衡
✦ +
+
论文ID
原名:Multidimensional tumor-blood profiling uncovers systemic lymphocyte-monocyte imbalance in pituitary neuroendocrine tumors
译名:多维肿瘤-血液分析揭示垂体神经内分泌肿瘤中系统性淋巴细胞-单核细胞失衡
期刊:Signal Transduction and Targeted Therapy
影响因子:52.7
发表时间:2025.11.18
DOI号:10.1038/s41392-025-02489-0
背 景
垂体神经内分泌肿瘤(PitNET)起源于垂体前叶的激素分泌细胞,是一类独特的原发性颅内肿瘤,兼具内分泌和肿瘤学意义。流行病学数据显示,其发病率约为每年每10万人4.54例,占所有原发性脑肿瘤的17.2%,是继脑膜瘤之后第二常见的颅内肿瘤。2022年世界卫生组织(WHO)的分类将PitNET的分子分型细化为三个转录因子驱动的谱系:PIT1谱系肿瘤(泌乳素细胞、促甲状腺激素细胞、生长激素细胞)、TPIT谱系肿瘤(促肾上腺皮质激素细胞)和SF1谱系肿瘤(促性腺激素细胞),另有极少数的无谱系细胞肿瘤缺乏谱系特异性标记。临床上,PitNET表现出双重特征。一方面,功能性PitNET过度分泌催乳素(PRL)、促肾上腺皮质激素(ACTH)和生长激素(GH)等激素,导致全身性内分泌紊乱,例如催乳素瘤引起的不孕症、库欣病相关的代谢紊乱以及肢端肥大症相关的器官肿大。另一方面,非功能性PitNET约占病例的15%~35%(主要属于SF1谱系),通常在出现明显的占位效应之前难以发现,导致双颞侧偏盲或颅神经麻痹等并发症。因此,PitNET的影响不仅限于颅内病变,还会作为全身性疾病修饰因子,需要更全面地看待其垂体外影响。
实验设计
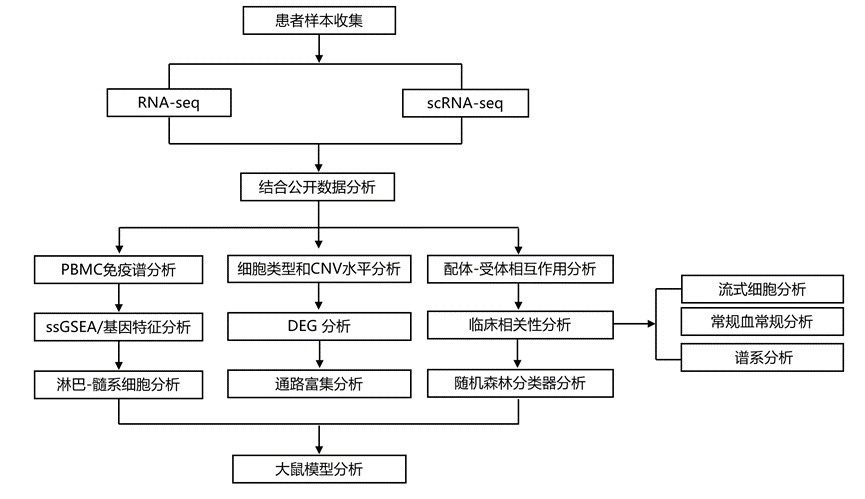
结 果
01
垂体神经内分泌肿瘤患者的表征
研究团队开展了一项多维度研究,将肿瘤组织特征与外周血免疫数据相结合。他们利用以下数据:对 883 例肿瘤、108 例 PitNET 患者外周血单核细胞 (PBMC) 样本和 175 例健康对照进行转录组分析 (RNA-seq);对 59 例肿瘤样本、4 例正常垂体组织、3 例 PitNET 患者 PBMC 样本和 3 例健康个体 PBMC 样本进行单细胞转录组分析 (scRNA-seq);并通过流式细胞技术、血常规检查和术后 PBMC追踪进行临床验证(图1a),从而绘制出 PitNET 的系统性免疫图谱。肿瘤谱系特异性分泌程序与 PBMC 上的相应受体相互作用,扰乱淋巴细胞和髓系细胞群的平衡,而肿瘤切除可以逆转这种平衡。结合雌激素驱动的大鼠模型,他们发现PitNET是肿瘤-外周免疫轴的关键调节因子,其中分泌配体(例如谱系特异性激素或趋化因子)直接影响循环免疫细胞。这项工作将PitNET重新定义为免疫调节实体,并将PBMC定位为动态生物标志物,为靶向激素-免疫相互作用的治疗策略提供了框架。
他们对三种样本类型(包括 883 例 PitNET 肿瘤组织、108 例 PitNET 患者PBMC 和 175 例正常 PBMC)中的 19353 个蛋白质编码基因进行了主成分分析 (PCA)。结果显示,在校正批次效应后,肿瘤组织样本与两种 PBMC 样本之间存在显著差异(图1b)。值得注意的是,与正常 PBMC 相比,PitNET 患者的 PBMC 更接近肿瘤组织(图1b),因此他们进行了重点 PCA,比较 PitNET 患者 PBMC 和正常 PBMC。在这些样本中,有 9 例正常 PBMC 是自行构建的,其与公开的正常 PBMC 谱图吻合良好,进一步证实了 PitNET 患者 PBMC 中观察到的独特表达模式(图1c)。
他们鉴定PitNET和正常PBMC之间的差异表达基因(DEG),并将性别和年龄作为混杂协变量进行校正。结果显示,共有322个基因显著上调,685个基因显著下调(图1d)。对 PitNET PBMC 中 322 个上调基因进行通路富集分析,结果显示其富集于细胞因子-细胞因子受体相互作用和趋化因子信号通路(例如CXCL5、CCL3L3、CXCL8)等通路(图1e),这与 PitNET PBMC 中细胞因子活性增强相一致。基因集富集分析 (GSEA) 证实 PitNET PBMC 中细胞因子-细胞因子受体相互作用通路显著增强。此外,PI3K-Akt 信号通路、cGMP-PKG 信号通路和雌激素反应也在上调基因中富集(图1e)。他们还观察到与昼夜节律同步(例如GNG11、GUCY1B1)和肥厚型心肌病(例如ITGB3、ITGA2B、IL6)相关的通路富集,提示PitNET患者PBMC存在系统性紊乱(图1e)。相反,685个下调基因与炎症反应、中性粒细胞胞外陷阱形成、造血细胞谱系和自然杀伤细胞介导的细胞毒性等过程相关(图1f),提示PitNET患者PBMC的免疫细胞组成与正常PBMC相比发生了显著改变。
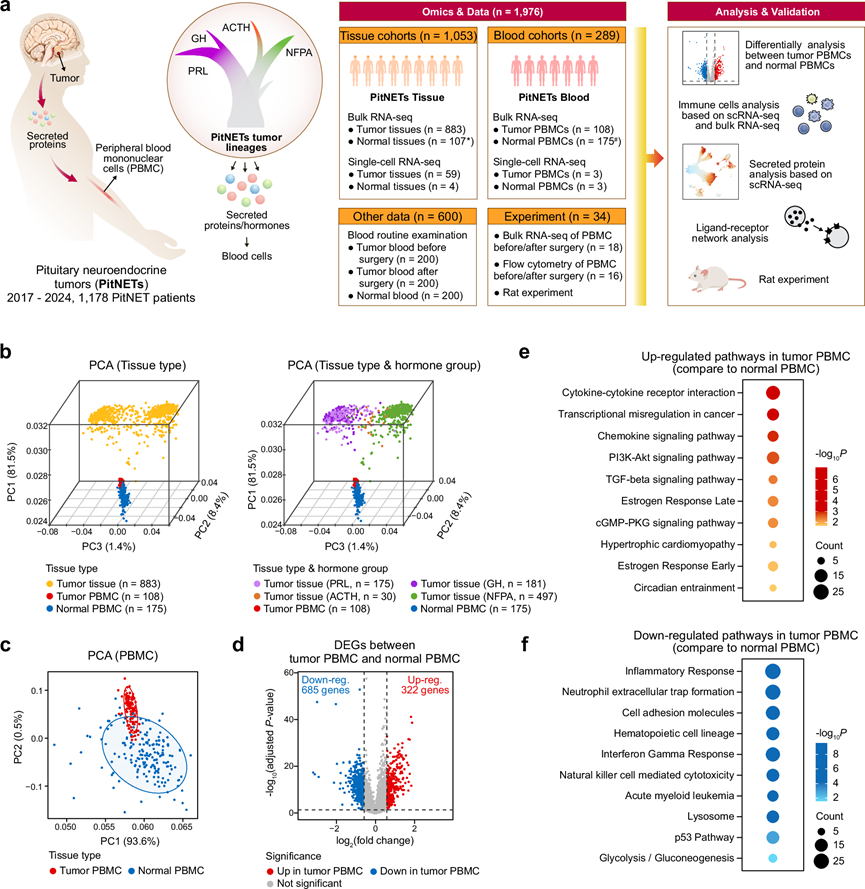
图1. 整合蛋白质基因组学和正向遗传学以揭示 TNBC 的新靶点。
(A) 对一组TNBC患者来源异种移植(PDX)模型进行了蛋白质组学表征。(B) 基因筛选,以识别在PTPN12缺陷细胞中选择性必需的基因。(C) 利用基因集富集分析(GSEA)整合。
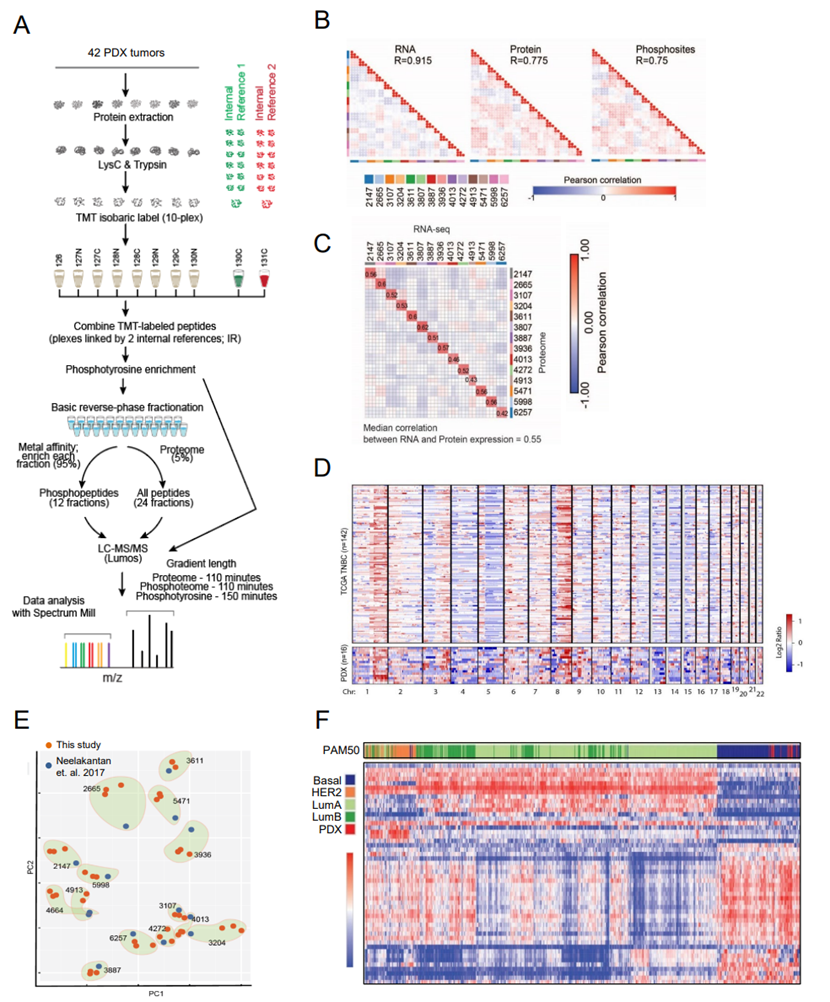
图1. PitNET PBMC 的研究设计概述及通路特征。
(a) 研究框架示意图。(b) 使用蛋白质编码基因进行主成分分析 (PCA) 图。(c) 外周血单核细胞 (PBMC) 的主成分分析 (PCA) 图。(d) 火山图展示了 PitNET 患者 PBMC 与正常 PBMC 之间的差异表达基因 (DEG)。 (e-f) 点图分别突出显示了 PitNET 患者 PBMC 与正常 PBMC 相比,上调和下调的差异表达基因所显著富集的通路。
02
免疫谱分析显示淋巴细胞和单核细胞数量失衡。
为了阐明PitNET中的系统性免疫改变,他们对3例未经治疗的PitNET患者和3例健康对照者的PBMC进行了scRNA-seq,经质量过滤后获得了54298个高质量细胞。他们发现了17个不同的细胞聚类,根据经典标记物将其注释为13种免疫细胞类型,例如T细胞(CD3E)、CD8+ T细胞(CD8A)、B细胞(CD79A)、单核细胞(CD14)等(图2a-b)。值得注意的是,PitNET 患者PBMC表现出显著的淋巴细胞与单核细胞比例失衡,其特征是 T/NK 细胞和 B 细胞比例增加,而单核细胞比例减少(图2a)。这种失衡也体现在 PitNET 患者 PBMC 中淋巴细胞与单核细胞的比值显著高于健康对照组(图2c)。对 T/NK 细胞进行进一步的亚群分析和注释,揭示了七个亚群(图2d-e),其中包括 PitNET 患者中 CD4+调节性 T 细胞(CD4T_Treg;FOXP3高表达)的扩增(图2f)。
为了在更大范围内验证这些发现,他们应用单样本基因集富集分析 (ssGSEA)从 108 个 PitNET PBMC 和 175 个正常 PBMC 的RNA-seq 谱中推断细胞类型丰度(图2g)。 ssGSEA结果显示,PitNET患者外周血单核细胞(PBMC)中存在淋巴细胞偏倚,表现为记忆性CD8+ T细胞(CD8T_Tm)和效应记忆性CD8+ T细胞(CD8T_Tem)、效应记忆性CD4+T细胞(CD4T_Tem)以及调节性CD4+ T细胞(CD4T_Treg)的富集,同时单核细胞亚群(monocyte_CD14+和monocyte_CD16+)减少,以及中性粒细胞丰度呈下降趋势(图2g-h)。此外,与健康对照组相比,在不同的激素组之间,生长激素(GH)水平较高的PitNET患者表现出Monocyte_CD14+水平较低,但CD4T_Treg、CD4T_Tem和CD8T_Tm水平较高(图2i)。鉴于PitNET中激素分泌(例如生长激素)之间可能存在相关性,内分泌活动可能与外周免疫变化有关。为了在独立的队列中验证这些发现,他们对200例PitNET患者和200例年龄和性别匹配的健康对照者的新鲜血液样本进行了全面的血液常规检查。该验证结果与scRNA-seq和RNA-seq的结果一致,显示PitNET患者的绝对淋巴细胞计数显著升高(P值=0.017)(图2j),且淋巴细胞与单核细胞的比值也显著升高(图2k)。同时,PitNET 患者血液中的中性粒细胞计数和百分比明显降低,证实了在 PBMC 批量分析中观察到的趋势(图2l)。
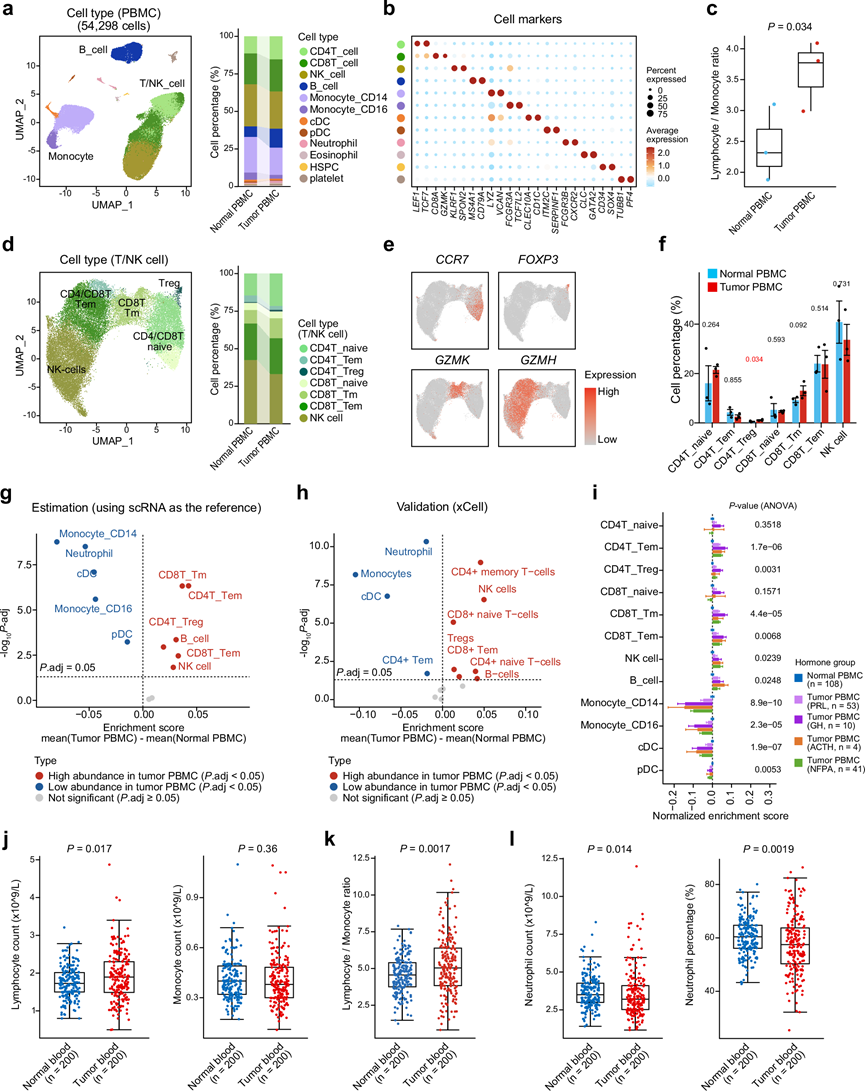
图2. 利用scRNA-seq和RNA-seq数据估计,对PitNET患者外周血单核细胞(PBMC)和正常PBMC进行免疫谱分析。
(a)UMAP可视化。(b) 点阵图,显示了每种细胞类型的归一化表达(颜色标度)和表达关键标记基因的细胞百分比。(c) 箱线图比较 PitNET 患者外周血单核细胞 (PBMC)和正常PBMC中淋巴细胞与单核细胞的比例。(d) UMAP 图展示了 PitNET 患者 PBMC 和正常 PBMC 中 T/NK 细胞亚群的鉴定结果。(e) UMAP 图显示了根据CCR7、FOXP3、GZMK和GZMH表达水平分别着色的细胞。(f) 条形图比较 PitNET 患者 PBMC和正常 PBMC中 T/NK 细胞类型的百分比。(g) 对 PitNET 患者 PBMC 和正常 PBMC 中的细胞类型丰度进行估计和比较。(h) 分析PitNET PBMC和正常 PBMC的细胞类型丰度并进行比较。(i) 条形图比较 PitNET PBMC 和正常 PBMC 批量 RNA-seq 中估计的细胞类型丰度。(j) 箱线图比较了PitNET患者和健康个体血常规检查数据中的淋巴细胞计数(左图)和单核细胞计数(右图)。(k) 箱线图比较了PitNET患者和健康个体的淋巴细胞/单核细胞比值。(l) 箱线图比较了PitNET患者和健康个体血常规检查数据中的中性粒细胞计数(左图)和中性粒细胞百分比(右图)。
03
术后免疫重建揭示了动态的淋巴-髓系细胞平衡
鉴于PitNET患者与健康个体外周免疫谱存在差异,他们研究了切除肿瘤是否能减轻其全身免疫调节作用。为此,他们分析了9例PitNET患者术前(第0天)和术后5天(第5天)的配对PBMC样本,这些患者的催乳素(PRL)水平显著升高,并推断免疫细胞丰度(图3a)。值得注意的是,术后5天,包括CD4T_Tem和CD8T_Tm在内的几种淋巴细胞亚群显著减少,而单核细胞(Monocyte_CD14)水平显著升高(图3b)。与此一致的是,这9例患者的PRL水平均下降,恢复至正常生理范围(图3c)。为了阐明这些变化背后的分子机制,他们分析在术前和术后样本之间共鉴定出128个DEG,其中34个基因显著下调,94个基因显著上调。在上调基因中,一些髓系相关标志物(例如CD14、S100A12、S100A8和S100A9)显著升高。对这些上调基因进行通路富集分析发现,炎症反应和中性粒细胞胞外陷阱(NET)形成相关通路活性增强。相反,Hedgehog和Wnt信号通路显著下调(补充图3c),提示这些变化可能对免疫调节具有更广泛的影响。
为了验证这些转录组学结果,他们对另外8例患者术前和术后5天采集的新鲜PBMC样本进行了流式细胞分析。这些分析证实,术后粒细胞和单核细胞显著增加,而CD8 + T细胞和B细胞则显著减少(图3d)。他们还利用一个包含200例PitNET患者的大型独立队列,通过收集术前和多个术后时间点(从术后第2天到第30天及以后)的纵向血常规检查数据,获得了进一步的临床验证。分析结果显示,术后淋巴细胞计数和百分比均显著下降(在术后第2至3天最为明显),同时单核细胞计数和百分比相应升高,并在术后第3至5天达到峰值(图3e)。因此,淋巴细胞与单核细胞的比值逐渐下降(图3f)。此外,中性粒细胞计数和百分比出现短暂但显著的升高,尤其是在术后第2至5天之间,进一步强调了髓系细胞的扩增。与此同时,他们观察到术后第3至5天激素水平(催乳素、生长激素、促肾上腺皮质激素)下降,并在30天后恢复至正常范围(图3g-i)。综上所述,这些结果表明, PitNET的手术切除可能启动全身免疫的动态平衡。术后髓系细胞(尤其是单核细胞和中性粒细胞)的显著复苏,以及特定淋巴细胞亚群的收缩,凸显了肿瘤相关分泌失调对全身免疫稳态和恢复的关键影响。
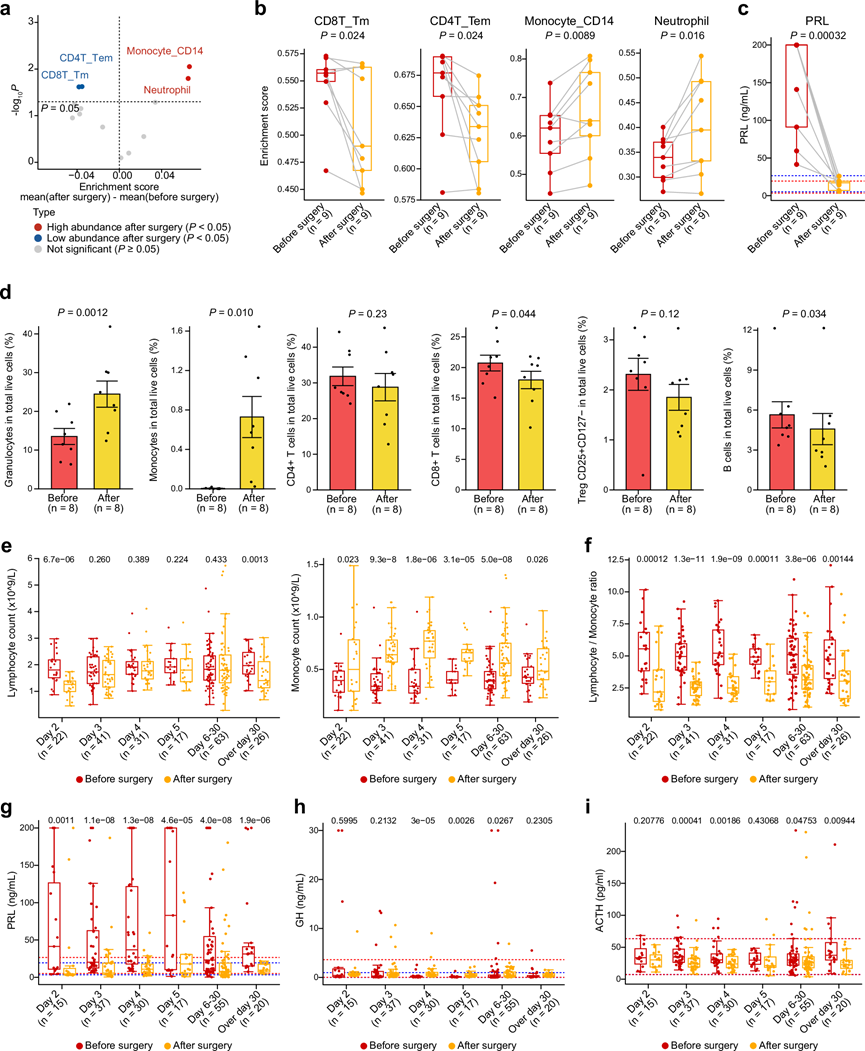
图3. PitNET患者术后外周免疫恢复情况。
(a) 火山图展示了PitNET患者术前和术后5天配对PBMC样本中免疫细胞丰度评分的变化。(b) 箱线图比较了四种代表性免疫细胞类型(CD4T_Tem、CD8T_Tm、单核细胞_CD14和中性粒细胞)术前和术后5天的富集评分。(c) 箱线图比较了PRL水平在术前和术后5天的变化。(d) 条形图显示了 PitNET患者术前和术后5天细胞变化。(e) 箱线图描绘了200例PitNET患者术前和术后不同时间点血常规检查的淋巴细胞和单核细胞计数。(f) 箱线图比较了同一组 200 例 PitNET 患者术前和术后不同时间点的淋巴细胞与单核细胞比值。(g-i) 箱线图比较了同一组(有激素记录)患者术前和术后不同时间点的PRL、生长激素 (GH) 和促肾上腺皮质激素 (ACTH) 水平。
04
谱系特异性分化和基因组不稳定性影响PitNET的分泌能力
基于对周围免疫影响的观察,他们接下来试图阐明PitNET组织固有的细胞和分子异质性。通过分析来自59例PitNET肿瘤组织和4例正常垂体组织的scRNA-seq数据,他们构建了一个全面的PitNET单细胞图谱。经过质量控制后,保留了377586个细胞用于后续分析。基于图的聚类分析识别出21个不同的细胞群,每个细胞群均由独特的基因表达标记物定义。值得注意的是,三个主要的二分化聚类具有高表达的EPCAM,以及谱系特异性转录因子POU1F1、TBX19和NR5A1,确定为代表PitNET的三个主要谱系(图4a-b)。将肿瘤细胞分为一个共同的前体细胞群(Lineage_undiff_1 至 Lineage_undiff_3)和三个谱系特异性分支:PIT1 谱系进一步细分为四个亚群(Lineage_PIT1_1 至 Lineage_PIT1_4),TPIT 谱系细分为两个亚群(Lineage_TPIT_1 和 Lineage_TPIT_2),SF1谱系细分为三个亚群(Lineage_SF1_1 至 Lineage_SF1_3)(图4a-b)。此外,其他细胞群包括来自肿瘤组织微环境的免疫细胞(巨噬细胞/树突状细胞、中性粒细胞、B 细胞、T/NK 细胞)、基质细胞(上皮细胞、成纤维细胞、内皮细胞)以及少量增殖的肿瘤细胞(图4a)。随后,他们对PitNET患者的细胞组成进行了分类,并使用密度图对其进行了可视化(图4c)。密度图显示,PIT1谱系PitNET中的细胞可分为两种表达模式:一种亚组表现出高PRL表达(PIT1-PRL亚型),另一种亚组表现出高GH1表达(PIT1-GH亚型)(图4b-c)。此外,TPIT谱系PitNET中的细胞主要定位于Lineage_TPIT_1和Lineage_TPIT_2,而SF1谱系细胞主要分布于Lineage_SF1_1、Lineage_SF1_2和Lineage_SF1_3(图4c)。有趣的是,不分泌激素的空细胞 PitNET主要发现于 Lineage_undiff_1、Lineage_undiff_2 和 Lineage_SF1_1 中,这表明末端分支群体(例如 Lineage_PIT1_3 和 Lineage_PIT1_4)可能表现出增强的激素分泌能力(图4c)。
利用 Monocle3 软件,他们重建了 PitNET 肿瘤细胞类型的潜在分化轨迹(图4d)。该分析表明,终末分支细胞可能起源于更早期的中间细胞(Lineage_undiff_1、Lineage_undiff_2 和 Lineage_undiff_3),因此他们将所有细胞归类为四个主要组:Lineage_undiff、Lineage_PIT1、Lineage_TPIT 和 Lineage_SF1(图4e)。为了表征基因组改变并评估拷贝数变异 (CNV),他们以正常垂体细胞为参考,应用了 inferCNV 算法。结果显示,与正常垂体组织相比,PitNET 肿瘤细胞的 CNV 水平显著升高,其中终末分化细胞的 CNV 变异性更高(图4f-g)。例如,在PIT1谱系中,Lineage_PIT1_3和Lineage_PIT1_4相对于Lineage_undiff_1表现出更显著的CNV改变(图4g)。随后,以Lineage_undiff为参考,他们鉴定了终末肿瘤细胞分支中的DEG,并进行了富集分析(图4g)。上调的通路与蛋白质分泌以及生长激素和甲状旁腺激素的合成、分泌和作用显著相关(图4h)。此外,MAPK、IL-2/STAT5和PI3K-AKT/mTOR等关键信号通路在终末分化细胞中显著上调(图4h)。相反,下调的通路主要涉及核糖体生物合成(图4h)。总而言之,这些发现揭示了PitNET肿瘤细胞的内在异质性,并提供了谱系特异性分化和CNV变异性的详细单细胞图谱。PitNET 是分化相关肿瘤,具有谱系特异性转录程序和不断增加的基因组不稳定性,这可能有助于其分泌特化。
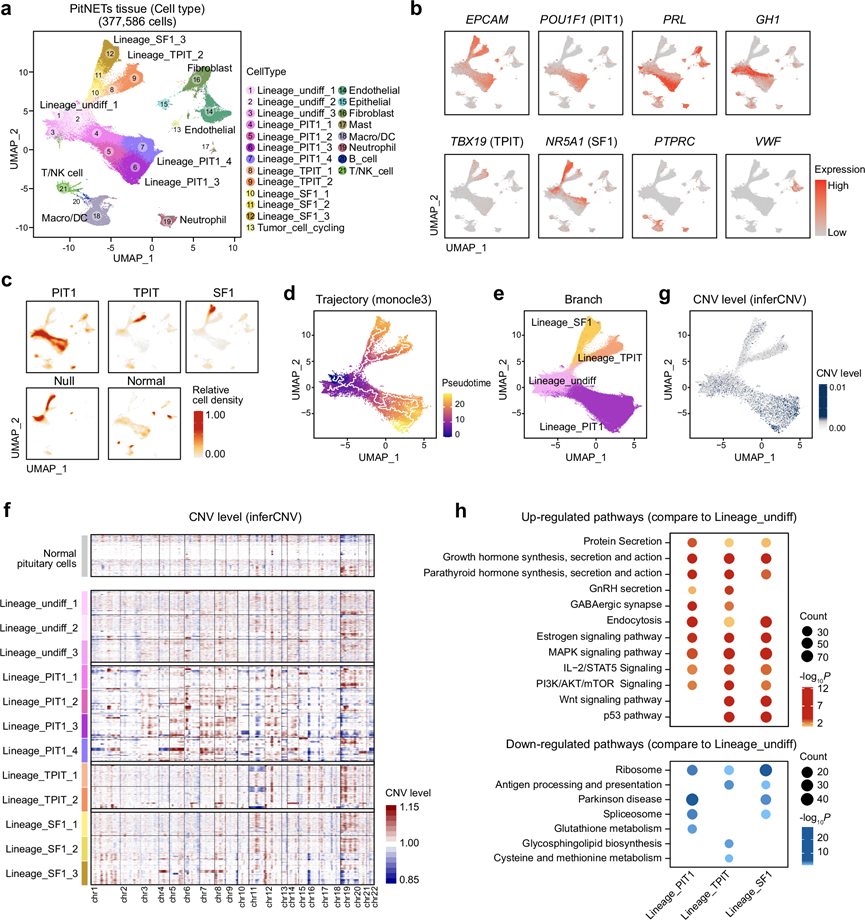
图3. 对PitNET组织进行单细胞分析,并鉴定主要细胞类型和拷贝数变异(CNV)水平。
(a) 源自PitNET组织的377586个细胞的UMAP图,按细胞群着色。(b) 特征图显示了与特定肿瘤谱系以及免疫细胞和基质细胞相关的关键标记基因的表达模式。(c) UMAP密度图突出显示了不同PitNET谱系以及正常垂体细胞的相对细胞密度。(d) 使用Monocle3进行细胞轨迹分析,展示了不同PitNET谱系之间潜在的分化路径。(e) PitNET组织的UMAP图,按细胞分支着色。(f) 热图显示了使用inferCNV方法推断的不同PitNET肿瘤细胞谱系的CNV水平。(g) UMAP图描绘了推断的PitNET肿瘤细胞的CNV水平。(h) 点图展示了基于 PitNET 细胞与 Pre_branch 细胞相比显著上调(上图)和下调(下图)基因的富集通路。
05
谱系特异性的分泌谱
接下来,他们进一步探讨了PitNET肿瘤细胞的分泌特性。分泌蛋白,例如激素和细胞因子,是由特定的蛋白质编码基因编码,由细胞产生并通过特定的分泌途径释放到细胞外环境中的蛋白质。在细胞间通讯中,许多分泌蛋白作为配体与靶细胞上的受体结合,从而启动信号级联反应,调节细胞增殖和分化等过程。由于细胞通常同时分泌多种蛋白质,因此细胞间相互作用通常涉及复杂的配体库(图5a)。为了捕捉这种复杂性,他们构建了一个包含大量细胞外可检测分泌蛋白和配体-受体相互作用的数据库,该数据库整合了来自13个已发表的细胞间相互作用工具的数据,包括CellPhoneDB、CellChat、NicheNet以及其他工具(图5b)。总而言之,综合数据库包含了1841个配体、1510个受体和17919个配体-受体相互作用对。接下来,他们根据文献报道,鉴定出328个疑似分泌蛋白的配体,这些配体在肿瘤细胞中高表达。然后,基于这些蛋白的平均基因表达水平分析了分泌评分(图5c),并观察到终末分化肿瘤细胞,例如Lineage_PIT1_3 ( PRL )、Lineage_PIT1_4 ( GH1 )、Lineage_TPIT_2和Lineage_SF1_3中的细胞,其分泌评分显著高于早期或中间分化细胞(例如Lineage_undiff_1)(图5d)。
将分泌评分与临床特征进行相关性分析发现,肿瘤体积较小、无侵袭性或激素染色阳性的肿瘤具有更高的分泌能力(图5e-f)。这些分泌蛋白的平均基因表达热图进一步证实,终末分化肿瘤细胞表现出较高的分泌活性(图5g)。对来自scRNA-seq的这些分泌蛋白的基因表达进行无监督聚类分析,鉴定出三个不同的组,分别对应于主要的PitNET谱系:配体聚类1(LC-PIT1)对应PIT1谱系,配体聚类2(LC-TPIT)对应TPIT谱系,配体聚类3(LC-SF1)对应SF1谱系(图5g)。对 883 例 PitNET 肿瘤样本进行RNA-seq 分析证实了分泌蛋白基因表达与 PitNET 亚组之间的关联,提示这些分泌蛋白可能作为肿瘤分类的潜在关键标志物(图5g)。例如,LC-PIT1 包含与激素分泌(如PRL、GH1、TSHB、TRH)、MAPK 信号通路(如MET)和 WNT 家族(如WNT10A、WNT5B、WNT3、WNT4)相关的基因(图5g和补充图5e)。 LC-TPIT 主要包含与库欣综合征相关的基因(例如POMC、EGFR),而 LC-SF1 富含 GnRH 信号通路成分(例如LHB、FSHB)(图5g)。
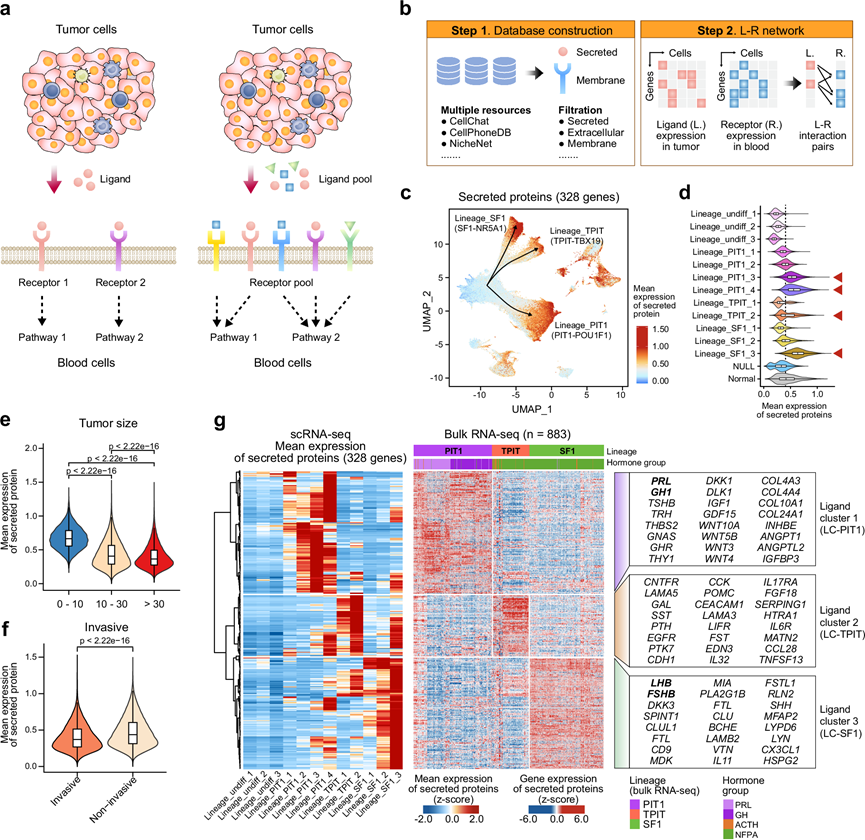
图5. PitNET中谱系特异性分泌谱。
(a) 示意图展示了由肿瘤分泌蛋白驱动的细胞间相互作用。(b) 构建综合配体-受体(LR)相互作用网络的工作流程。(c) UMAP图描绘了328种分泌蛋白在不同PitNET谱系中的基因表达模式。(d) 小提琴图比较了不同 PitNET 谱系中分泌蛋白的平均表达水平。(e) 小提琴图显示了不同大小肿瘤中分泌蛋白的表达水平。(f) 小提琴图对比了侵袭性和非侵袭性 PitNET 之间的分泌蛋白表达水平。(g) 热图显示了 scRNA-seq(左)和 RNA-seq(右)数据中 328 种分泌蛋白的平均表达水平。
06
肿瘤-血液配体-受体串扰及基于外周血单核细胞的PitNET分类
为了将肿瘤来源的分泌配体与PBMC的免疫重塑联系起来,他们分析了配对的RNA-seq样本中肿瘤组织配体表达与 PBMC 细胞丰度之间的 Spearman 相关性(图6a)。PBMC 细胞群聚类为四组:初始/调节性淋巴细胞群(CD4T_Treg、CD4T_naive、CD8T_naive、CD8T_Tm)、B 细胞相关细胞群(pDC、B 细胞)、髓系细胞群(Monocyte_CD14、Monocyte_CD16、cDC)和效应记忆淋巴细胞群(CD8T_Tem、CD4T_Tem、NK 细胞)(图6a)。在LC-PIT1中,大多数配体(包括GH1)与初始/调节性淋巴细胞群呈正相关,尤其是CD4T_Treg(图6a)。与此一致的是,激素分泌分析显示,循环GH水平与CD4T_Treg、CD4T_naive和CD8T_naive细胞的丰度显著相关(图6b)。这一观察结果与之前的报道一致,即GH支持CD4T_Treg的功能和维持,同时促进初始CD4/CD8 T细胞的胸腺输出(图6b)。为了进一步验证这些相互作用,他们分析了经受体表达筛选的PBMC scRNA-seq数据,并构建了一个基于血液的配体-受体网络,该网络包含311个配体、662个受体和3334个配体-受体对(图6a)。使用Fruchterman-Reingold算法可视化的网络拓扑结构显示,配体位于网络中心,受体位于网络外周(图6c)。在单细胞水平上,受体表达表现出明显的谱系特异性,淋巴细胞亚群(CD4T_naive、CD4T_Tem、CD4T_Treg、CD8T_naive、CD8T_Tm、CD8T_Tem、NK细胞、B细胞)通常比髓系细胞群(pDC、单核细胞_CD14)表达的受体少(图6d),从而证明PitNET分泌的配体可以映射到外周血中相应的受体表达。
利用这些差异,他们基于PBMC细胞类型丰度训练了一个随机森林分类器来预测PitNET状态。总共283个PBMC样本(108个PitNET样本,175个健康样本)随机分为训练集(75%)和验证集(25%)。该模型在完整数据集上达到了93.2%的准确率(AUC = 0.987),在验证集中达到了73.2%的准确率(AUC = 0.862)(图6e-f)。为了进一步评估其转化应用潜力,他们使用108个PBMC样本中的75%训练了一个分类器来区分激素分泌型(PRL/GH/ACTH)和非功能型(NFPA)PitNET。该模型在完整数据集上达到了0.985的AUC,在验证集中达到了0.829的AUC(图6g-h)。总的来说,这些结果表明,PBMC 免疫谱不仅能以很高的准确度区分 PitNET 患者和健康个体,而且还为术前功能性与非功能性亚型的分类提供了一个实用的框架,从而在临床决策和患者分层方面具有潜在的实用价值。
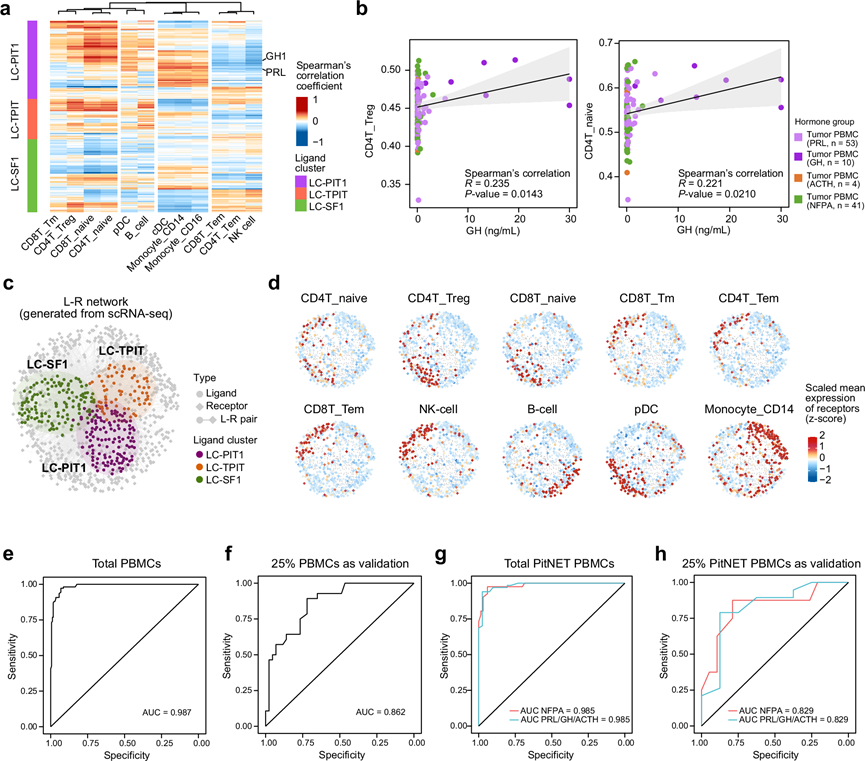
图6. 肿瘤-血液配体-受体相互作用及基于外周血单核细胞(PBMC)的亚型预测。
(a) Spearman相关系数热图,展示了匹配的PitNET病例中肿瘤-配体基因表达与估计的PBMC细胞丰度之间的关联。(b) 血清生长激素(GH)水平与估计的PBMC CD4T_Treg和CD4T_naive丰度水平之间的相关性。(c) 配体-受体网络。(d) LR网络中不同免疫细胞群中受体的表达水平。(e-f) 基于PBMC中免疫细胞谱,训练用于区分PitNET患者和健康个体的随机森林模型的ROC曲线。(g-h) h.基于PBMC免疫细胞谱,训练用于区分PitNET亚型的随机森林模型的ROC曲线。
07
雌激素诱导的大鼠高催乳素血症可重现垂体-免疫内分泌轴功能障碍
在 PIT1-PRL 谱系 PitNET 中,LC-PIT1 配体的表达相对于正常垂体组织显著升高(图7a),同时,患者PBMC中相应的受体也(与正常 PBMC 相比)发生了显著改变(图7b)。鉴于雌激素通过下丘脑-垂体轴内的反馈机制调节催乳素 (PRL) 的分泌,并且考虑到PIT1-PRL 谱系 PitNET中PRL和雌激素受体 1 (ESR1) 的表达升高(图7c),他们假设雌激素信号通路可能重现类似的病理和免疫改变。基于之前的报道,他们建立了一个雌激素诱导的大鼠模型来模拟 PIT1-PRL 谱系 PitNET的特征。F344 大鼠从第 1 周到第 6 周隔日接受雌激素治疗(图7d)。为减少药物的直接影响,治疗在随后的两周(第7-8周)内停止,并在第10周采集外周血和垂体组织。结果显示,与对照组相比,雌激素治疗组大鼠的垂体体积显著增大(图7e-f)。组织病理学检查(H&E染色)显示,几乎所有雌激素诱导组大鼠的垂体中均存在由嗜酸性大细胞组成的增生性结节,与催乳素细胞增生相符(图7g)。此外,ELISA检测证实,雌激素诱导组大鼠的PRL水平显著升高(图7h)。
与临床观察结果一致,雌激素诱导的大鼠外周血免疫细胞群发生显著变化,表现为淋巴细胞百分比升高(图7i)、单核细胞百分比降低(图7i),以及淋巴细胞/单核细胞比值升高(图7j)。中性粒细胞水平显著降低(图7k)。对PRL-PitNET患者的细胞类型丰度分析显示,淋巴细胞群有增加的趋势,特别是CD4T_Tem、CD4T_Treg和CD8T_Tm细胞。随后,将每两只大鼠的外周血混合,并对分离的PBMC进行RNA-seq。雌激素诱导大鼠与对照组之间的DEG分析鉴定出371个显著上调基因和134个显著下调基因(图7l)。对上调基因进行富集分析,发现其富集于包括癌症、MAPK、趋化因子和雌激素信号通路在内的多个通路(图7m)。此外,GSEA显示,与对照组相比,雌激素诱导大鼠PBMC中LC-PIT1配体聚类对应的受体显著富集(图7n)。这些结果表明,雌激素驱动的激素-垂体-免疫轴反馈机制可能影响全身免疫调节。
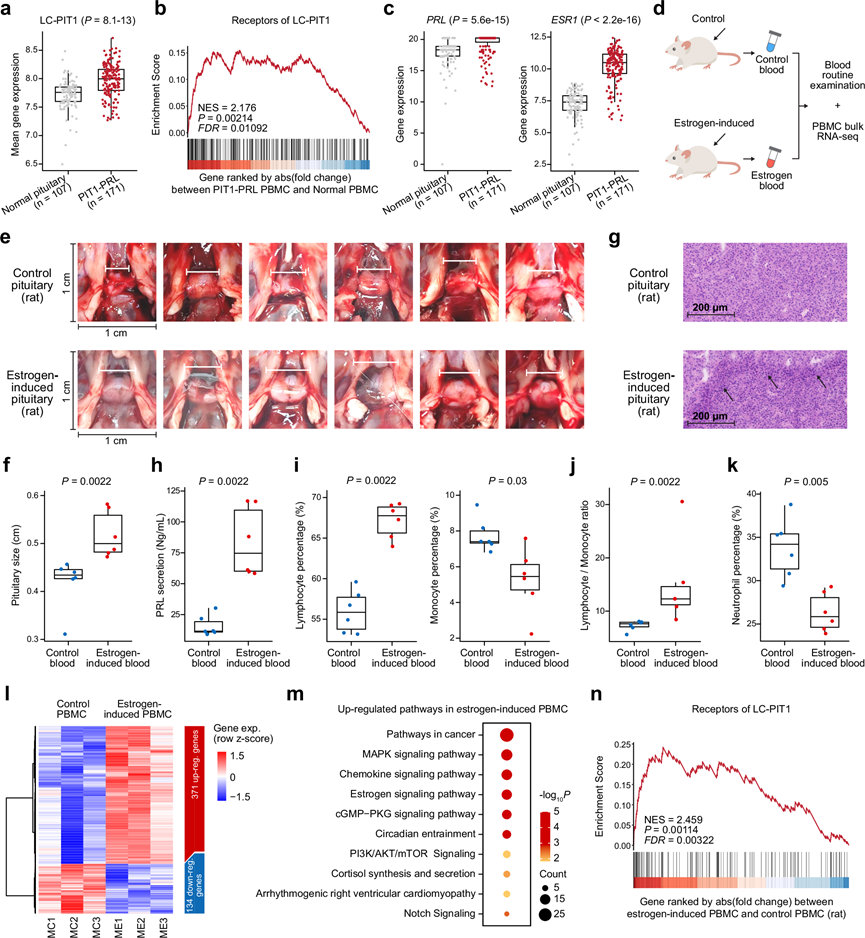
图7. 雌激素诱导的大鼠模型重现了PitNET PIT1-PRL谱系样特征和免疫改变。
(a) 箱线图比较了正常垂体组织和PIT1-PRL谱系PitNET组织中分泌蛋白(LC-PIT1)的平均基因表达水平。(b) GSEA图展示了LC-PIT1的受体基因。(c) 箱线图展示了正常垂体组织与 PIT1-PRL 谱系 PitNET 组织中PRL和ESR1基因表达的比较。(d) 雄性大鼠雌激素注射方案示意图。(e) 对照组(上)和雌激素诱导组(下)大鼠垂体的代表性图像。(f) 箱线图比较对照组大鼠 和雌激素诱导组大鼠的垂体大小。(g) 垂体组织切片的组织病理学检查显示大鼠垂体中存在多激素结节。(h) 箱线图显示对照组和雌激素诱导组大鼠的血清催乳素 (PRL) 水平。(i-k) 箱线图显示对照组和雌激素诱导组大鼠的淋巴细胞百分比和单核细胞百分比、淋巴细胞/单核细胞比值以及中性粒细胞百分比。(m) 雌激素诱导组大鼠 PBMC 中上调基因的富集通路。(n) 基因集富集分析(GSEA) 图。
+ + + + + + + + + + +
结 论
本研究系统分析了883例PitNET肿瘤、108例PitNET相关PBMC样本和175例健康PBMC对照的RNA-seq数据,并结合69例scRNA-seq样本(涵盖肿瘤、正常垂体以及肿瘤来源和正常PBMC),发现PitNET患者存在系统性免疫失衡,表现为循环淋巴细胞比例升高,并伴有细胞因子-受体相互作用特征的上调。值得注意的是,肿瘤切除术逆转了这种失衡,单核细胞和中性粒细胞计数恢复正常。轨迹分析鉴定出终末分化、分泌特化的细胞群,这些细胞群具有谱系特异性激素和细胞因子过度分泌的特征。配体-受体推断表明,这些肿瘤来源的因子可能与循环免疫细胞受体结合。基于PBMC转录组的随机森林分类器能够区分PitNET亚型,凸显了外周免疫特征的诊断潜力。此外,在雌激素诱导的大鼠模型中,PRL水平升高与相同的外周免疫偏倚同时发生。
+ + + + +



 English
English


