文献解读|Cell(42.5):爬行脂肪来源的机械敏感性成纤维细胞驱动克罗恩病狭窄部位的肠道纤维化
✦ +
+
论文ID
原名:Creeping fat-derived mechanosensitive fibroblasts drive intestinal fibrosis in Crohn's disease strictures
译名:爬行脂肪来源的机械敏感性成纤维细胞驱动克罗恩病狭窄部位的肠道纤维化
期刊:Cell
影响因子:42.5
发表时间:2025.09.17
DOI号:10.1016/j.cell.2025.08.029.
背 景
克罗恩病 (CD) 是炎症性肠病 (IBD) 的一种亚型,其特征是主要累及肠道的斑片状、全层肠壁炎症的周期性发作。慢性炎症会引发肠道纤维化,导致增厚的瘢痕组织取代正常的肠实质,使肠腔变窄,形成狭窄。虽然成人和儿童患者均会出现狭窄,但儿童 CD 狭窄的研究尚不充分,其疾病进展过程可能有所不同。据估计,30%-50% 的儿童患者在确诊后 5 年内会出现肠道狭窄,约28% 的患者在确诊后 10 年内需要接受腹腔手术,且 22%-47% 的狭窄在术后会复发。最后,目前尚无获批的抗纤维化疗法。因此,狭窄会给 CD 患者带来显著的并发症。爬行脂肪(CF)是指肠系膜脂肪组织(MAT)扩张并包裹病变肠段,是CD的特征性病理表现,70%–90%的肠狭窄部位存在CF,CF与肠切除术后的复发相关,切除CF可降低狭窄发生率。组织学上,CF包裹与纤维化程度和肠壁(BW)增厚相关,CF 衍生基质细胞对 CD 狭窄进展的贡献仍未得到充分研究。
实验设计
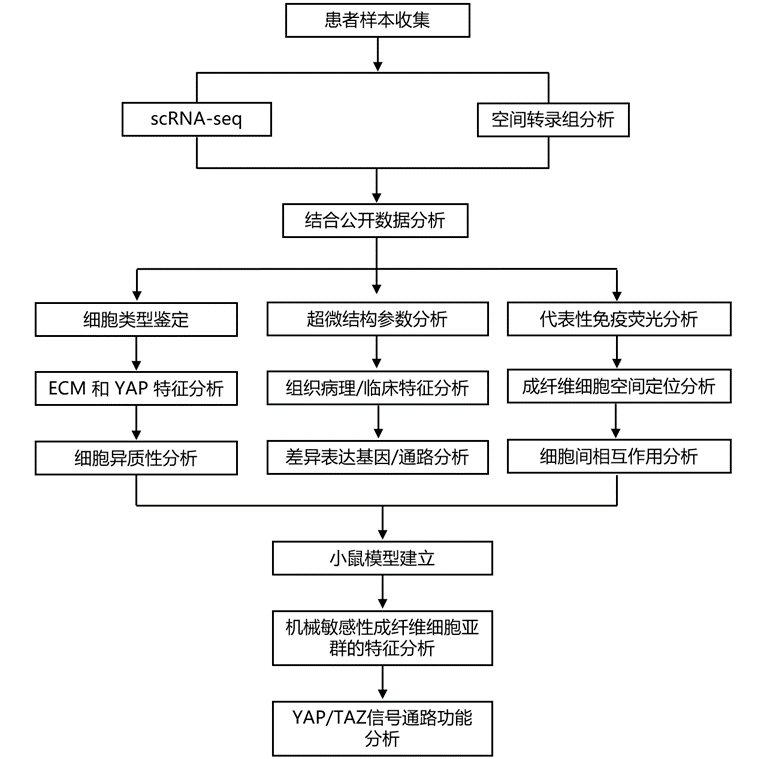
结 果
01
人类CD成纤维细胞图谱揭示了CF中的致病性、机械敏感性成纤维细胞
CF包裹与CD的纤维化严重程度相关,提示MAT可能参与狭窄进展(图1A)。他们最初假设一部分CF来源的促纤维化成纤维细胞迁移至BW并促进狭窄进展。为了验证这一假设,他们进行了单细胞转录组分析(scRNA-seq),并构建了一个泛研究CD的scRNA-seq成纤维细胞图谱,以识别致病性成纤维细胞(图1B)。首先,他们整理了公开可用的关于CD患者或非CD患者的肠道和MAT样本的scRNA-seq研究,这些样本取自活检或全层切除标本。同时,他们对CD狭窄患儿及其邻近未受累组织的全层配对肠道和MAT样本,以及非CD患儿的造口术拆除标本进行了内部scRNA-seq测序。然后,他们根据疾病表现对疾病状态进行分类,并将所有研究整合,构建了一个包含约180万个细胞(80327个来自MAT,1729759个来自肠道)的CD图谱,这些细胞来自426名患者。在确定了整体细胞类型后,他们对成纤维细胞进行了亚聚类,最终得到了10个整体成纤维细胞聚类,这些细胞聚类在所有研究参数中均具有均匀的代表性,但黏膜活检除外,因为黏膜活检缺乏全层样本中完整的成纤维细胞谱(图1C)。
为了表征成纤维细胞表型,他们检测了推断成纤维细胞活化来源(YAP/TAZ信号通路、炎症和抗原呈递)、细胞外基质(ECM)生成或迁移能力的基因特征的表达。CTHRC1+成纤维细胞的ECM基因表达最高,YAP/TAZ靶基因水平升高,并表达YAP/TAZ通路组分和迁移基因(图1D)。随后,他们通过将分析范围限定于非CD组织学正常组织、CD狭窄邻近的非CD受累组织以及来自全层肠道和MAT样本的CD狭窄组织,评估了CD成纤维细胞图谱在不同组织和疾病状态下的整体成纤维细胞富集情况(图1E)。与正常和非受累组织相比,CTHRC1+成纤维细胞是唯一在整体以及狭窄肠道和MAT中均显著增加的细胞群(图1F)。有趣的是,他们发现治疗方式对狭窄处CTHRC1+成纤维细胞的富集没有显著影响。与其它疾病状态相比,CTHRC1+成纤维细胞在未受累和狭窄组织中均强烈激活ECM和YAP/TAZ特征,尤其是在CF中,这表明这些成纤维细胞在狭窄发病早期激活(图1G)。为了更准确地评估成纤维细胞的组织异质性,他们根据组织对整体成纤维细胞进行亚聚类,使用组织特异性标记物对细胞群进行注释,并检测成纤维细胞的富集情况。正如预期的那样,CTHRC1+成纤维细胞在狭窄肠道和 CF 患者中均富集。此外,通过 MAT 和肠道成纤维细胞之间的锚定标记转移评估基因表达相似性,结果显示CTHRC1+成纤维细胞在不同组织间相似。
由于CD成纤维细胞图谱涵盖了多种疾病状态、采样方法和组织来源,他们试图通过专门分析包含来自狭窄部位和邻近未受累组织的配对肠道和MAT样本的儿科数据集来验证。他们从CD图谱中提取了本研究中标记的成纤维细胞,独立地以高分辨率重新聚类,并通过锚定标记转移将其映射回原始CD图谱。正如预期的那样,CTHRC1+成纤维细胞存在于肠道和MAT中,在狭窄部位较邻近未受累组织中扩增,并且与他们在CD图谱中鉴定的CTHRC1+成纤维细胞高度相似。有趣的是,他们还发现了一些与CD图谱中的成纤维细胞群(主要来自成人患者)不同的成纤维细胞群,这表明儿科和成人狭窄部位的成纤维细胞异质性可能存在差异。两组患者中CTHRC1+成纤维细胞的扩增进一步证实了CTHRC1+成纤维细胞是 CD 纤维化的重要组成部分。总之,这些结果表明,机械敏感性CTHRC1+成纤维细胞是一种与狭窄相关的成纤维细胞,存在于肠道和 CF 中(图 1H)。
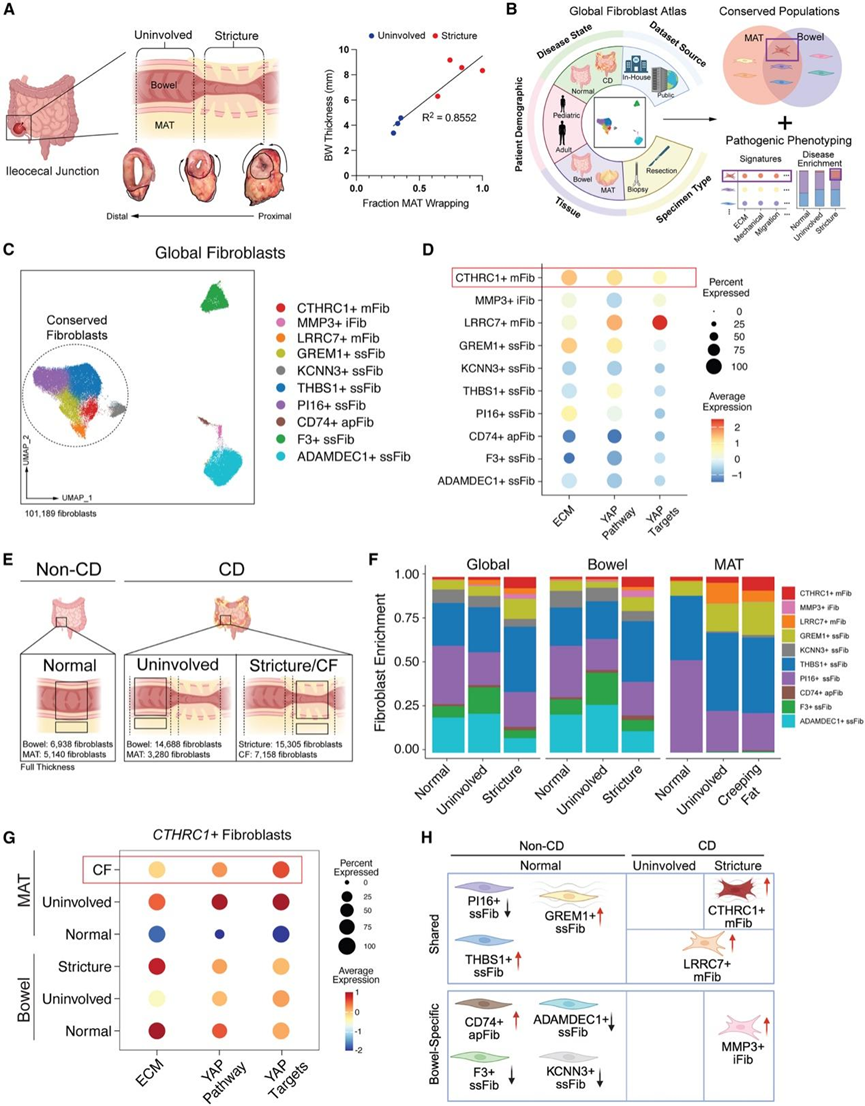
图1. 机械敏感性成纤维细胞存在于人类CF中并增殖。
(A) 示意图(上)和大体横截面(下),取自CD儿童回肠切除标本,涵盖狭窄段至远端未受累(UI)肠段,并可见MAT包裹(箭头,黑色轮廓)(左)。(B) 示意图显示了促纤维化 CF 衍生成纤维细胞的鉴定。(C) 对 101189 个独立重新聚类和整合的成纤维细胞进行均匀流形近似和投影(UMAP)。(D) 成纤维细胞亚群中 ECM 和 YAP 特征表达量的标度平均点图。(E) CD 患者和非 CD 患者全层小肠和 MAT 样本疾病状态比较示意图。(F) 成纤维细胞亚群富集情况的条形图。(G) 不同疾病状态下CTHRC1+成纤维细胞中 ECM 和 YAP 特征表达量的散点图。(H) CD狭窄处成纤维细胞异质性的示意图。
02
CF 和 BW 之间的间质纤维化程度很高
接下来,他们推测CTHRC1+成纤维细胞会定位于狭窄处的纤维化区域。为了识别这些区域,采用了一种多模态方法,将ECM超微结构分析与Visium ST软件相结合(图2A)。最初观察到,MAT-BW 肠道交界处(IF)区域在固有肌层(MP)下方存在一层较厚的纤维化层(图2B)。因此,他们将狭窄或未受累的肠道组织划分为三个不同的区域:未受累和狭窄的BW区域(穿过MP的管腔)以及IF区域(MP和CF之间的基质),后者仅存在于狭窄的肠道中。然后,他们对用天狼猩红染色的样本进行成像,定量了294个ECM超微结构参数,进行了降维处理,并赋予从正常到纤维化的ECM递增的值,他们将其称为纤维化伪时间。ECM超微结构分析显示,IF区域的ECM超微结构倾向于聚集在远离未受累ECM超微结构的区域,且其纤维化伪时间值显著高于其他区域(图2C-D)。与先前的超微结构分析结果一致,这些发现表明CF/BW IF区域可能是晚期狭窄中纤维化的主要部位。
随后,他们对队列中的一例儿童狭窄进行了空间转录组分析(ST),将狭窄样本解剖为两个区域:内壁(从管腔到浅层间质)和外壁(从下壁至中膜、间质和纤维环)(图2E)。与其他区域相比,间质中质的细胞外基质、机械转导、细胞迁移以及致病性成纤维细胞特征和基因显著富集(图2F)。为了确认间质是一个转录特征独特的区域,使用低分辨率对Visium斑点进行了亚聚类。在识别出的四个亚群中,基质3斑点独立聚类,与间质斑点重叠,并且在转录水平上与间质斑点相似。与其他基质区域相比,基质3也富集了机械敏感基因特征和细胞外基质重塑通路。最后,对核内YAP(一种反映成纤维细胞机械激活的指标)的定量分析表明,CF和IF的核内YAP含量最高,进一步证实CF和IF均为人类狭窄中的机械敏感区域。
随后,他们对队列中的一例儿童狭窄进行了结构化转录组分析(ST),将狭窄样本解剖为两个区域:内壁(从管腔到浅层间质)和外壁(从下壁至中膜、间质和纤维环)(图2E和图S3A)。与其他区域相比,间质中质的细胞外基质、机械转导、细胞迁移以及致病性成纤维细胞特征和基因显著富集(图2F,图S3B-D)。为了确认间质是一个转录特征独特的区域,他们使用低分辨率对Visium斑点进行了亚聚类。在鉴定出的四个亚群中,基质3斑点独立聚类,与间质斑点重叠,并且在转录水平上与间质斑点相似(图S3E-G)。与其他基质区域相比,基质3也富集了机械敏感基因特征和细胞外基质重塑通路(图S3 H-I)。最后,对核内YAP(一种反映成纤维细胞机械激活的指标)的定量分析表明,CF和IF的核内YAP含量最高,进一步证实CF和IF均为人类狭窄中的机械敏感区域(图S3 J)。
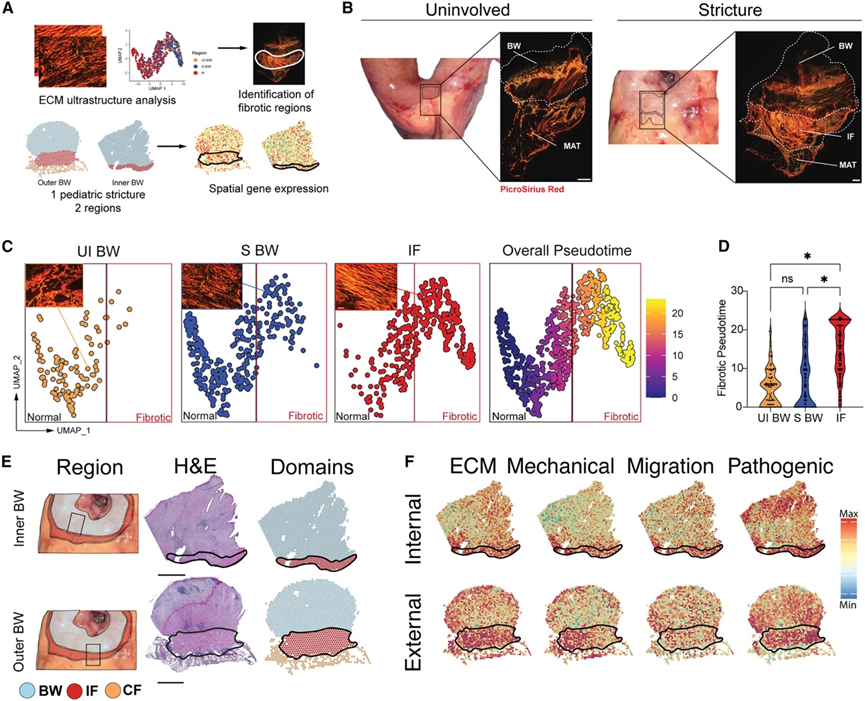
图2. 肠道与MAT之间的间质纤维化区域高度纤维化。
(A) ECM 超微结构分析与 Visium ST 集成的示意图。(B) 图左侧为儿童UI部位的组织大体组织学图像,右侧为经Picrosirius染色处理的代表性切片。(C) 分别绘制 UI BW(左)、狭窄 BW (S BW)(中)和 IF(右)的 ECM 超微结构 UMAP 图(左);以正常 ECM 为原点,使用 Monocle 3 伪时间绘制的 ECM 超微结构整体 UMAP 图(右)。(D) 小提琴图显示每个区域中 ECM 超微结构伪时间图。(E) 示意图,展示了同一患者两处肠段的切片位置(左)、H&E染色(中)和最终区域分类(右)。内肠(肠腔经肠壁至浅层肠纤维层)(上)。外肠(肠壁经肠纤维层至肠囊)(下)。(F) 成纤维细胞特征模块得分的空间特征图。
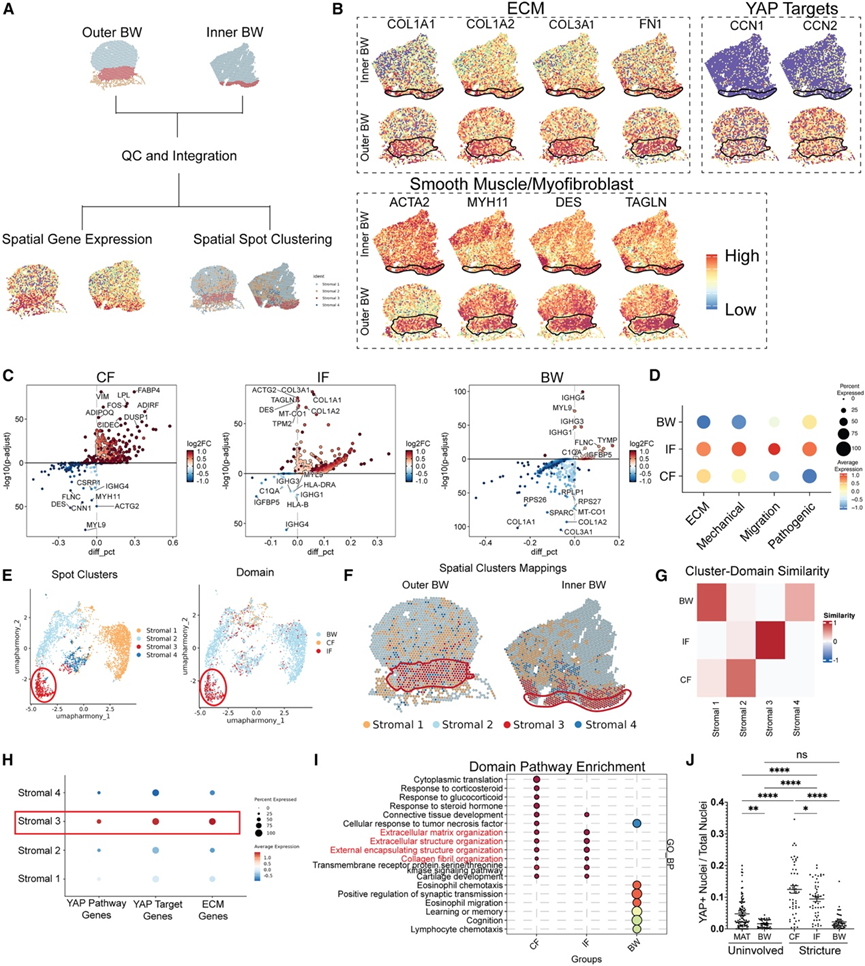
图S3. CF-BW IF是狭窄段内的纤维化区域。
(A) Visium 空间整合及后续分析示意图。(B) 代表性 ECM(左上虚线框)、YAP 靶基因(右上虚线框)和平滑肌/肌成纤维细胞基因(下虚线框)在外层(下)和内层 BW(上)的空间基因表达。(C) CF(左)、IF(中)和BW(右)中差异表达基因的火山图。(D) 点图显示每个区域中成纤维细胞表型特征的空间表达。(E) Visium斑点聚类的UMAP图,分别按基质邻近区域(左)和结构域(右)划分。(F) 基质邻域的空间图。(G) 与基质邻域相比,每个区域中前 100 个差异表达基因的余弦相似性得分的热图。(H) 基质邻域中 YAP 特征和 ECM 表达的散点图。(I) Visium结构域的通路分析。(J) YAP1+DAPI+ 细胞核与总 DAPI+ 细胞核比例的散点图。
03
CTHRC1+机械敏感性成纤维细胞定位于CF-BW IF中的纤维化微环境
在确认IF是狭窄段内的纤维化区域后,他们试图确定CTHRC1+成纤维细胞是否定位于该区域。使用包含额外脂肪细胞数据集的scRNA-seq CD细胞图谱对空间数据进行反卷积,并使用Niche Covariation推断细胞邻域(图3 A)。正如预期的那样,预测的CTHRC1+成纤维细胞在CF和IF中富集,并且其中一部分细胞同时表达CTHRC1、POSTN和YAP靶基因CCN1的转录本(图3B-D)。与未受累组织相比,狭窄部位的CF和IF中核内YAP1+POSTN+细胞显著富集,表明这些细胞就是在CD成纤维细胞图谱中鉴定的促纤维化CTHRC1+成纤维细胞。为了确定CF来源的CTHRC1+成纤维细胞的激活位置,他们对定位的CTHRC1+成纤维细胞中YAP靶基因的转录本进行了定量分析,这些细胞位于距BW三个不同距离范围内,从IF到远端CF(图3 E)。出乎意料的是,靶基因转录本的数量在IF中最低,而在距离BW最远的CF中最高,提示CTHRC1+成纤维细胞在远离狭窄部位时发生机械激活(图3F-G)。
鉴于狭窄区域内ECM的异质性,他们试图阐明CTHRC1+细胞群的细胞组成,通过鉴定对CTHRC1+成纤维细胞具有高预测能力的邻近细胞来分析细胞间相互作用评分。按区域分析CTHRC1+细胞群的相互作用发现,CTHRC1+成纤维细胞占据不同的纤维化微环境(图4A-B)。总体而言,在血管周围区域,CTHRC1+成纤维细胞与巨噬细胞以及PI16+和GREM1+成纤维细胞存在强烈的相互作用。CF-CTHRC1+细胞群表现出免疫细胞(巨噬细胞和中性粒细胞)和成纤维细胞(PI16+和CD74+)的相互作用。IF- CTHRC1+细胞群主要由血管周围区域的巨噬细胞、浆细胞、周细胞和成纤维细胞相互作用构成(GREM1+和THBS1+)。而BW- CTHRC1+细胞群则主要由成纤维细胞相互作用构成(GREM1+、MMP3+和PI16+)。因此,细胞外基质的异质性与CTHRC1+成纤维细胞微环境的变化密切相关。
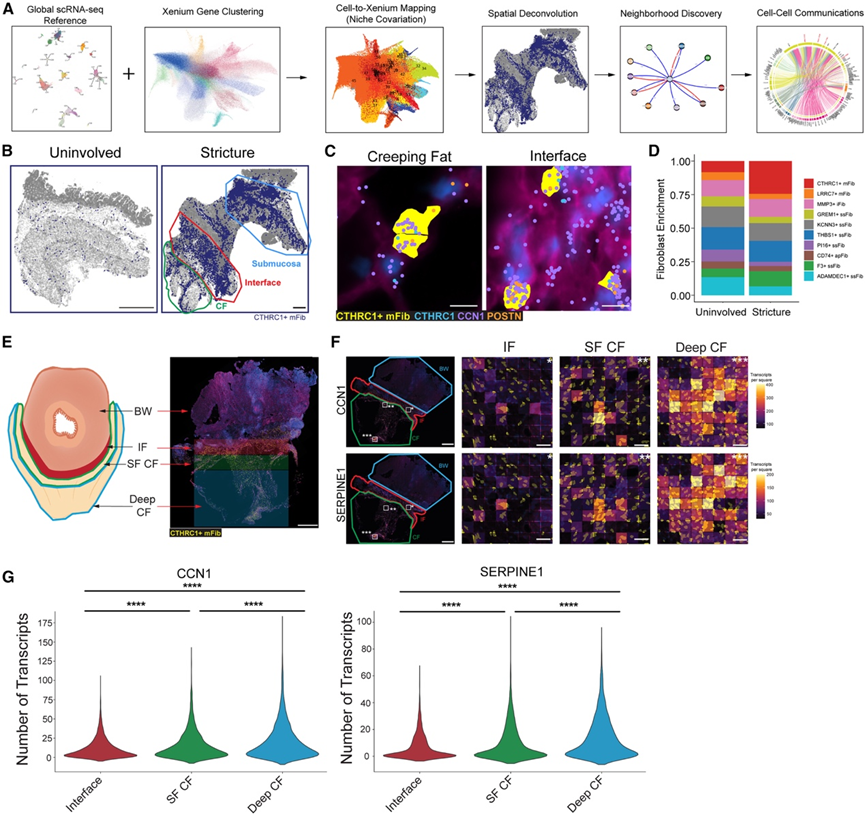
图3. CTHRC1+机械敏感性成纤维细胞定位于儿童狭窄的间质纤维环和纤维环中层。
(A) 反卷积的示意图。(B) 代表性的NiCo预测图谱显示了尿失禁(左)和狭窄(右)Xenium切片中CTHRC1 +成纤维细胞的分布。(C) DAPI(蓝色)和ATP1A1/CD45/E-钙黏蛋白(品红色)的代表性免疫荧光区域显示了CF(左)和IF(右)代表性区域中CTHRC1 +成纤维细胞(黄色)的预测分布。(D) 预测 UI和狭窄样本中成纤维细胞亚群富集的柱状图。(E) 狭窄肠组织分段标记示意图,包括 BW、IF、浅表 CF(SF CF)和深部 CF(左)。(F) YAP靶基因CCN1和SERPINE1转录本的密度图。(G) 小提琴图显示了 CF 亚组中 CTHRC1+成纤维细胞数量最多的狭窄样本中预测的 CTHRC1+成纤维细胞的CCN1(左)和SERPINE1(右)转录本计数。
04
成纤维细胞-微环境相互作用
随后,以CD细胞图谱为参考,从CTHRC1+细胞邻域的配体-受体基因表达中推断出主要的细胞间通讯通路。为了更精确地定位促纤维化通路,他们比较了狭窄组织与未受累组织和正常细胞中差异上调的通路。之后,他们分离出CTHRC1+成纤维细胞与其先前鉴定的邻近细胞之间的相互作用。与邻域分析结果一致,CTHRC1 +成纤维细胞与大多数预测的邻近细胞存在强烈的通讯。配体-受体分析显示,CTHRC1+成纤维细胞主要通过细胞外基质-整合素通路与大多数邻近细胞相互作用,同时还受到促纤维化巨噬细胞来源细胞因子(肿瘤坏死因子α [TNFα]、转化生长因子β [TGF-β] 和抑瘤素M [OSM])以及促血管生成周细胞来源因子(成纤维细胞生长因子 [FGF] 和 JAG1)的少量影响(图4C-F)。这些数据表明,CTHRC1+成纤维细胞主要通过细胞外基质与其微环境相互作用。
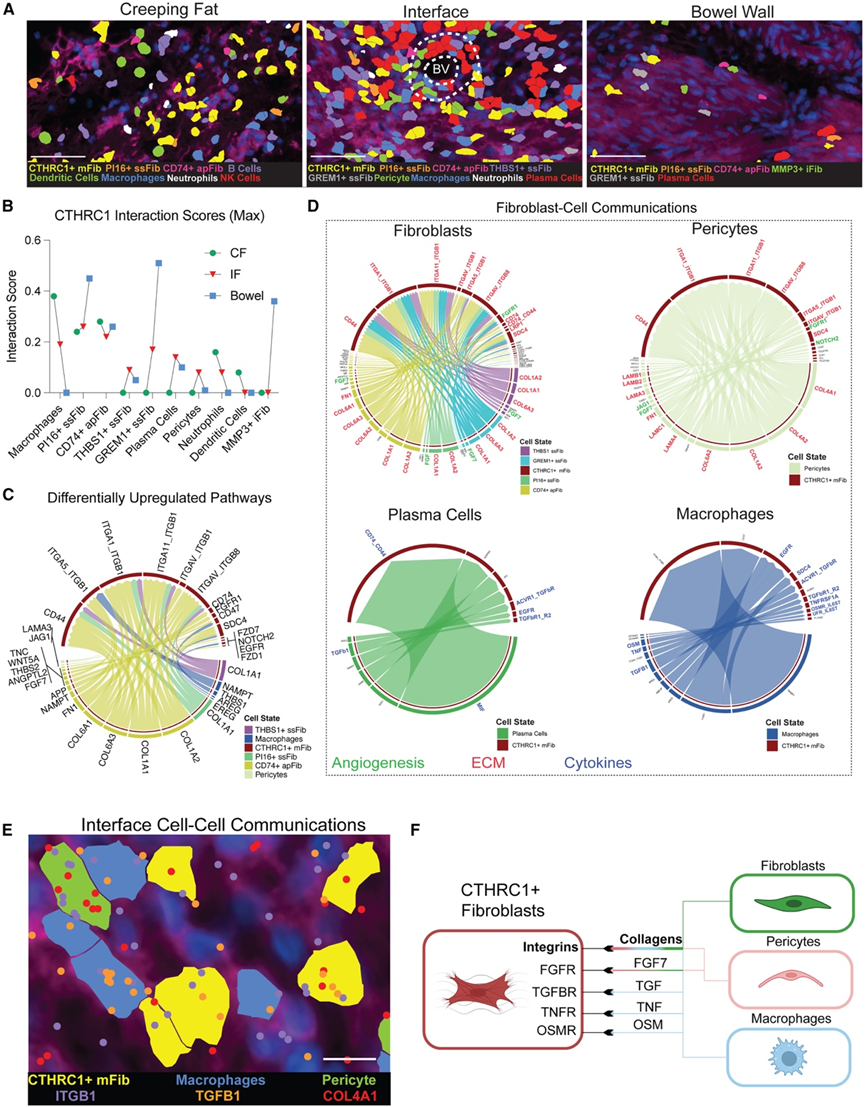
图4. CTHRC1+成纤维细胞-微环境相互作用主要通过细胞外基质发生。
(A) 代表性的免疫荧光区域,显示DAPI(蓝色)和ATP1A1/CD45/E-钙黏蛋白(品红色)染色,以及CF(左)、IF(中)和BW(右)中CTHRC1 +邻近区域的预测细胞类型标记。(B) 折线图描绘了儿科狭窄中 CF(绿色圆圈)、IF(红色三角形)和 BW(蓝色方块)中预测的CTHRC1 + 成纤维细胞与邻近细胞之间的最大归一化相互作用得分。(C) CellChat 绘制的 CD 图谱中CTHRC1+邻域中差异上调的配体-受体相互作用的弦图。(D) 弦图显示了来自 CellChat CD 图谱的CTHRC1+成纤维细胞与邻近成纤维细胞(左上)、周细胞(右上)、浆细胞(左下)和巨噬细胞(右下)之间显著上调的相互作用。(E) DAPI(蓝色)和ATP1A1/CD45/E-钙黏蛋白(品红色)的代表性免疫荧光区域显示了CTHRC1+成纤维细胞(黄色)、巨噬细胞(蓝色)和周细胞(绿色)的预测定位。(F) 示意图总结了CTHRC1+成纤维细胞与邻近细胞之间的主要相互作用。
05
小鼠肠道纤维化模型重现了CD肠道狭窄的主要特征
虽然在人类CD狭窄中发现了促纤维化的CTHRC1 +成纤维细胞,但无法确定它们的来源及其对肠道纤维化的贡献。对炎症性肠病(IBD)小鼠模型和CF的初步调查显示,除需要特殊设备的内镜穿刺活检模型外,大多数模型无法稳定地诱发CF。因此,他们试图设计一种稳定且易于操作的肠道纤维化和CF小鼠模型,旨在专门研究机械张力如何激活晚期狭窄中的CTHRC1+成纤维细胞。为此,他们构建了一种小鼠模型,即在结肠上做一个纵向的、对肠系膜的切口(结肠切开术)(图5A)。随后,剥离周围肠壁黏膜以诱导肠壁全层损伤,在张力下横向缝合结肠切口形成肠袋,并以最大张力水平拉伸结肠切口。考虑到狭窄主要发生在末端回肠,他们选择近端结肠,因为与回肠相比,其直径更大、肠壁更厚,这使得肠壁能够在不引起肠梗阻的情况下扩张,并能够施加更大的机械张力。为了进行初步比较,他们从假手术组(sham)或未包裹脂肪的邻近结肠切口(unsvolved)中获取肠段。假手术组和结肠切口组小鼠的体重变化相似,并在术后第6天(POD 6)恢复至基线水平。从宏观上看, MAT最早在术后第7天(POD 7)就包裹在结肠切开部位周围,在术后第14天(POD 14)达到高峰,并持续到术后第90天(POD 90),但并未包裹假手术组或未受累的肠段(图5B)。组织学上,BW在结肠切开部位表现出全层纤维化,包括MAT和BW之间的纤维化区域,类似于人类狭窄中的IF(图5C)。最后,他们发现结肠切开部位的MAT和IF中富含核YAP1+细胞,这与在人类CD狭窄中发现的YAP结果一致。因此,该模型模拟了CD狭窄和CF的宏观和组织学特征。
为了确定该模型中CF形成和纤维化随时间推移的演变过程,在术后第3天(POD 3)至第90天(POD 90)之间,分别从结肠切开术组和未受累组以及假手术组(POD 14)的五个时间点采集组织样本。然后,他们定量了MAT覆盖肠段的肠壁厚度、标准化三色染色阳性面积和肠壁厚度,发现所有这些指标均在POD 7至POD 14之间达到峰值,并在POD 90之前逐渐下降(图5D-E)。此外,MAT覆盖率达到肠周长的50%,且在此期间肠壁与MAT之间的角度显著减小,符合CF的临床定义(图5F)。虽然其中一些指标恢复至基线水平,但ECM超微结构的伪时间分析显示,纤维化在POD 90之前持续增加,表明纤维化是长期存在的(图5G-H)。此外,由MAT包绕的结肠切开术BW比未由MAT包绕的BW纤维化程度更高(图5I-J)。总之,这些结果表明,该模型能够产生持久的、全层纤维化和CF,其表型与CD狭窄的关键特征相似。由于未观察到假手术组和未受累组样本之间存在显著的组织学差异,因此他们在术后第14天(POD 14)纤维化指标达到最大值时,使用未受累和受累组织进行所有后续组织学分析。
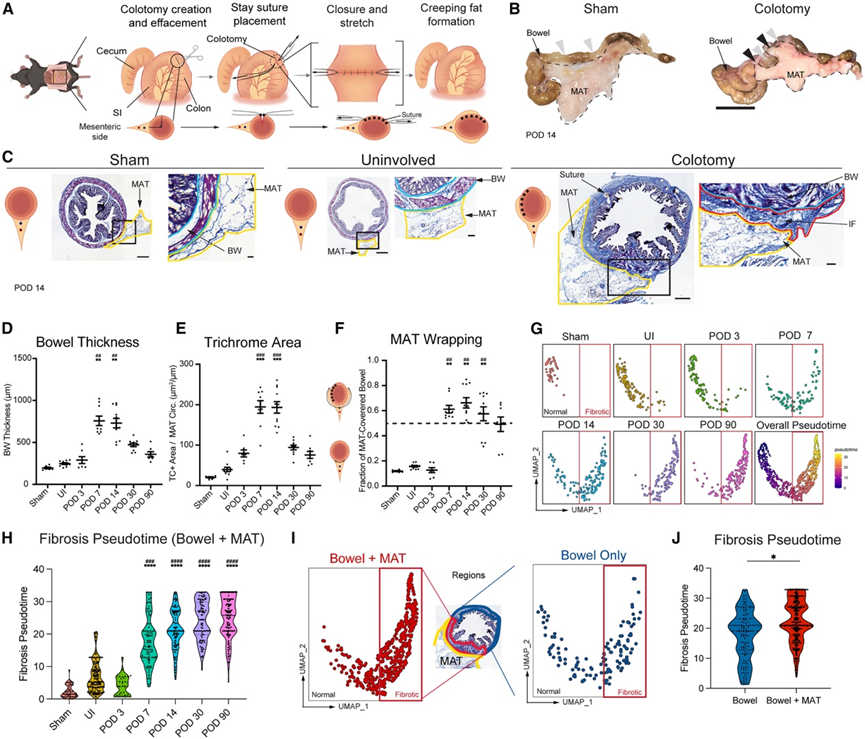
图5. 小鼠结肠切开模型重现了人类狭窄和CF的特征。
(A) 从上方(上)和横截面(下)观察,在张力下创建结肠切开术以产生纤维化和CF的示意图。(B) 术后第 14 天分离的假手术(左)和结肠切开术(右)肠道的宏观图像。(C) 术后第14天假手术组、尿路感染组和结肠切开组的Masson三色染色。(D-F) MAT 邻近肠壁 (MAT-ADJ) 的平均肠壁厚度和归一化三色阳性面积的散点图,以及 MAT 覆盖的肠壁比例的时间进程、假手术和尿失禁 (POD 14)。(G) 分别绘制肠道中 ECM 超微结构的时间进程图、假手术组(POD14)和 UI 组(POD 3-90)的 UMAP 图,分别对应有无 MAT 的情况。(H) 小提琴图显示了仅用 MAT 处理的肠道中 ECM 超微结构的时间进程、假手术(POD 14)和 UI(POD 3-90)的伪时间。(I) 结肠切开术后第 7 天至第 90 天,仅肠道(右)或肠道与 MAT(左)的 ECM 超微结构 UMAP 图像。(J) 结肠切开术图像中,从术后第 7 天到第 90 天,仅肠道和肠道与 MAT 的 ECM 超微结构伪时间的提琴图。
06
小鼠Cthrc1+成纤维细胞在肠道纤维化中富集
在确认小鼠模型与CD狭窄特征相符后,他们对术后第14天(POD 14)结肠切开术和假手术小鼠的肠道和MAT进行了scRNA-seq,以验证通过该模型是否也能捕获CTHRC1+机械敏感性成纤维细胞(图6A)。他们对成纤维细胞进行亚聚类,并鉴定出十个主要的全局簇,随后评估了这些簇的富集情况和表型(图6B)。在结肠切开术中富集的Cthrc1+成纤维细胞具有高表达的ECM、机械敏感性、迁移能力和病理成纤维细胞特征(图6C-F)。为了确定小鼠Cthrc1+成纤维细胞是否与人类CTHRC1+机械敏感性成纤维细胞类似,他们在小鼠成纤维细胞数据集和人类CD成纤维细胞图谱之间进行了锚定标记转移。小鼠Cthrc1+成纤维细胞与人类CTHRC1+成纤维细胞高度重合,表明这些成纤维细胞群在不同物种间保守(图 6G)。为了在蛋白水平上验证小鼠scRNA-seq结果,他们对 YAP1 和Cthrc1+成纤维细胞标记物 POSTN进行了共染色,结果显示,与未受累的 BW 和 MAT 相比,结肠切开术后的 MAT 和 IF 中核内 YAP1+POSTN+ 细胞数量显著增加(图 6H),这与人类狭窄中CTHRC1+成纤维细胞的扩增情况相似。
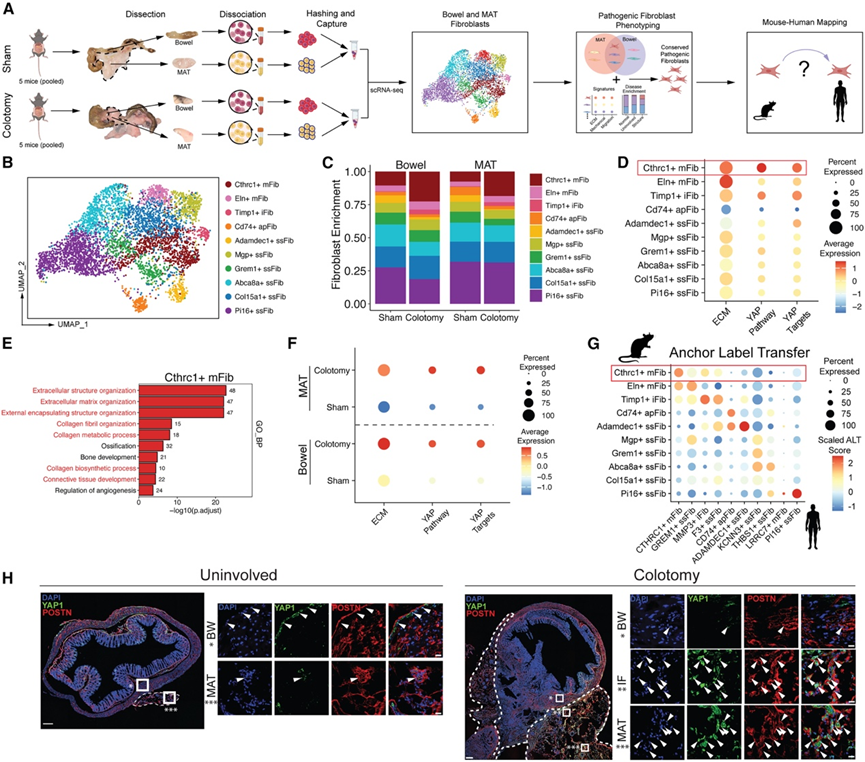
图6. MAT 来源的机械敏感性成纤维细胞在小鼠结肠切开术中得以保留。
(A) 在 POD 14 对假手术和结肠切开术小鼠进行肠道和相关 MAT 的单独解剖和分离的示意图,用于 scRNA-seq 分析。(B)5028 个小鼠成纤维细胞的 UMAP 按样本整合并独立重新聚类。(C) 假手术和结肠切开术肠道(左)和 MAT(右)中成纤维细胞富集的柱状图。(D) 成纤维细胞亚群中 YAP 和 ECM 特征的平均表达的点图。(E) Cthrc1 +成纤维细胞通路分析。(F) 不同条件下肠道和 MAT 中Cthrc1+成纤维细胞中 YAP 特征和 ECM 的平均表达的点图。(G) 小鼠数据集与人类CD图谱参考数据集之间成纤维细胞亚群的特征转移得分的散点图。(H)免疫荧光染色分析。
07
靶向机械敏感性肠系膜成纤维细胞中的YAP/TAZ信号通路可减少肠道纤维化
鉴于MAT结肠切开术肠系膜间质中存在机械敏感性成纤维细胞,他们试图确定其中一些成纤维细胞是否来源于MAT。由于无法通过scRNA-seq鉴定任何MAT特异性成纤维细胞标记物,他们首先采用了一种局部谱系追踪策略来标记MAT来源的成纤维细胞。将4-羟基他莫昔芬封装在脂质体(LiTMX)中,并将LiTMX注射到接受假手术或结肠切开术的Col1a2- CreERT2; ZsGreen+小鼠的肠系膜中。为了确定谱系追踪系统的特异性,他们将LiTMX中Col1a2+细胞的标记与Col1a2- CreERT2; ZsGreen+细胞的标记进行了比较。在POD 14,他们比较了未接受脂质体注射的ZsGreen+小鼠和接受全身性他莫昔芬注射的小鼠,分别在未受累肠段和结肠切开术肠段进行标记。全身性他莫昔芬注射导致未受累肠段和结肠切开术肠段的BW和MAT成纤维细胞广泛标记,从而影响了区分MAT来源和肠源性成纤维细胞的能力。相反,注射LiTMX可显著标记MAT成纤维细胞,而BW成纤维细胞标记较少,且在IF处出现明显的GFP+成纤维细胞扩增。基于这些原因,他们选择使用LiTMX标记小鼠模型中的MAT来源成纤维细胞。
为了评估CF来源的成纤维细胞对肠道纤维化的贡献,他们构建了Col1a2-CreERT2; YAPlox/lox ;TAZlox/lox;ZsGreen+(YAP/TAZ基因敲除[KO])小鼠和Col1a2-CreERT2; YAPlox/+;TAZlox/+;ZsGreen+(YAP/TAZ杂合子[Het])小鼠作为对照。对这些小鼠进行单次LiTMX注射,然后进行结肠切开术,并在POD 14时处取材(图7A)。总体而言,他们观察到与YAP/TAZ Het小鼠相比,YAP/TAZ KO小鼠结肠切开部位周围的MAT包裹减少(图7B-C)。随后,他们分别定量分析了整个肠环以及仅在结肠切开部位或未受累区域由MAT覆盖的肠段的纤维化参数。在整个肠道中,YAP/TAZ Het小鼠和KO小鼠在未受累区域或结肠切开区域,BW和标准化三色染色阳性面积均无显著差异。相反,YAP/TAZ KO小鼠的肠壁厚度和标准化三色染色阳性面积均降低,但在未受累区域则无差异。此外,与YAP/TAZ杂合子小鼠相比,YAP/TAZ KO小鼠的IF处MAT覆盖率降低,纤维化ECM超微结构也较少(图7D-H)。这些结果表明,CF驱动的纤维化作用局限于MAT附近的肠壁,而非整体肠壁变薄所致。
接下来,他们希望确认组织学结果与MAT来源的Cthrc1+成纤维细胞相关。为了排除纤维化减少是由于YAP/TAZ广泛缺失所致的可能性,他们对MAT、MAT-结肠切开IF以及MAT邻近BW中的核YAP进行了定量分析。KO小鼠MAT和IF中的核YAP水平极低,而BW中无显著差异,这进一步证实了脂质体注射定位于MAT。YAP与POSTN的共染色显示,在YAP/TAZ Het小鼠的MAT结肠切开术间质中,存在浸润结肠切开部位的核YAP1+GFP+POSTN+和GFP+POSTN+细胞(图7 I)。相反,YAP/TAZ KO小鼠的浸润性核内YAP1+POSTN+细胞水平降低,且未检测到GFP+YAP1+POSTN+细胞,表明YAP/TAZ KO也减少了MAT来源的机械敏感性成纤维细胞的扩增。这些结果表明,MAT来源的Cthrc1+成纤维细胞以YAP/TAZ依赖的方式促进纤维化,并且抑制MAT成纤维细胞中的YAP/TAZ信号通路足以改善肠道纤维化。
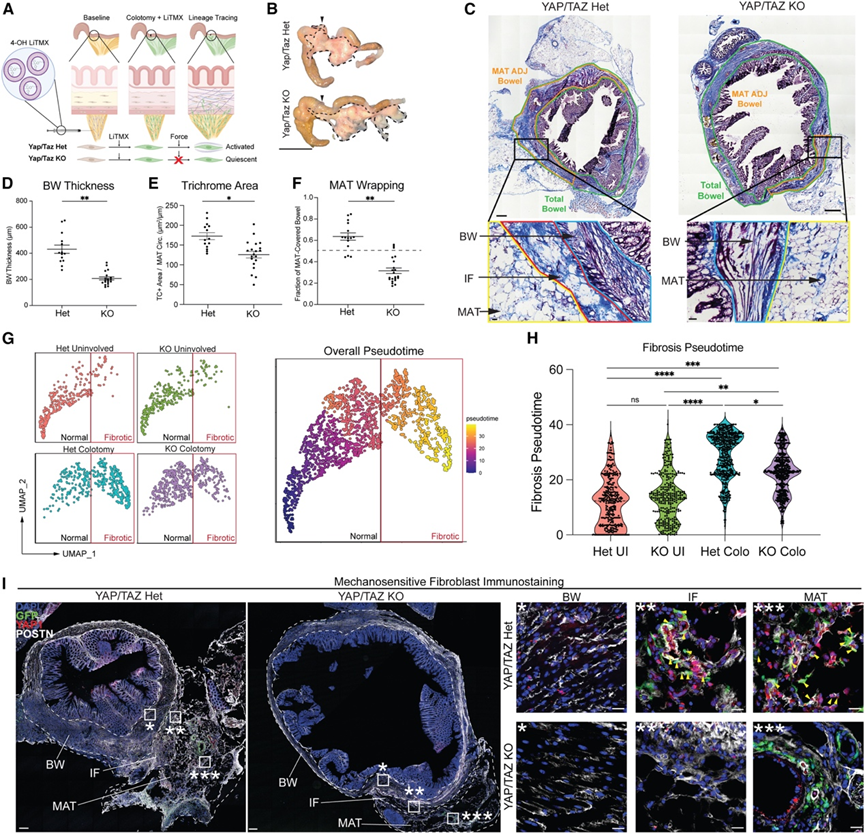
图7. MAT来源的Cthrc1+成纤维细胞通过YAP/TAZ信号通路促进肠道纤维化。
(A)实验示意图。(B) YAP/TAZ杂合子(上图)和YAP/TAZ敲除(下图)的大体组织学图像。(C) YAP/TAZ杂合子(左)和YAP/TAZ敲除(右)的Masson三色染色图。(D-F) YAP/TAZ Het和 KO结肠切开术中,BW MAT-ADJ 的平均 BW 厚度和归一化三色染色阳性面积以及 MAT 覆盖肠段比例的散点图。(G) YAP/TAZ Het和 KO UI 和结肠切开术后 ECM 超微结构的独立 UMAP(左)。以正常 ECM 为原点,使用 Monocle 3 伪时间绘制的 ECM 超微结构总体 UMAP(右)。(H) YAP/TAZ Het和 KO UI 和结肠切开术中 ECM 超微结构伪时间的提琴图。(I) 在Het(左)和KO(右)结肠切开术标本中,对GFP(绿色)、YAP1(红色)和机械敏感性标记物POSTN(白色)进行免疫染色。
+ + + + + + + + + + +
结 论
本研究构建了人类 CD 成纤维细胞单细胞图谱,鉴定出富含YAP/ TAZ特征的 CF 来源的 CTHRC1+成纤维细胞,这些细胞定位于狭窄段内纤维化的 CF 肠壁界面。进一步证明,在肠纤维化的小鼠模型中,类似的 Cthrc1+小鼠成纤维细胞来源于肠系膜脂肪组织基质细胞,能够浸润纤维化肠段,并以 YAP/TAZ 依赖的方式沉积细胞外基质。CF 是促纤维化成纤维细胞的关键来源,并提出了通过不仅针对肠道,而且针对 CF 来改善未来狭窄进展的临床管理的可能性。
+ + + + +



 English
English


