文献解读|Cell(42.5):妊娠和哺乳期间肝细胞代谢适应
✦ +
+
论文ID
原名:Hepatocyte metabolic adaptations during pregnancy and lactation
译名:妊娠和哺乳期间肝细胞代谢适应
期刊:Cell
影响因子:42.5
发表时间:2025.08.25
DOI号:10.1016/j.cell.2025.08.007.
背 景
肝脏是重要的代谢器官,为发育提供营养并维持体内平衡。在妊娠和哺乳期间,母体肝脏,尤其是肝细胞,会发生代谢适应,以满足胎儿和哺乳的需求。了解这些适应性变化对于推进生殖生物学发展以及改进牲畜管理和育种策略至关重要。虽然肝脏适应性改变非常重要,但其驱动机制仍知之甚少。研究表明,妊娠和哺乳期间肝脏会显著肿大,这归因于肝细胞增殖和肥大。人类影像数据同样表明,妊娠期间肝脏体积会增加,断奶后会恢复到基线水平。肝细胞分区沿门静脉 (PV)-中叶 (ML)-中央静脉 (CV) 轴定义了三个代谢区,其中ML 肝细胞是妊娠期间新细胞的主要来源。肝脏在妊娠和哺乳期间会经历代谢适应,以满足不断变化的生理需求,但其确切过程、调控机制和功能仍不清楚。
实验设计
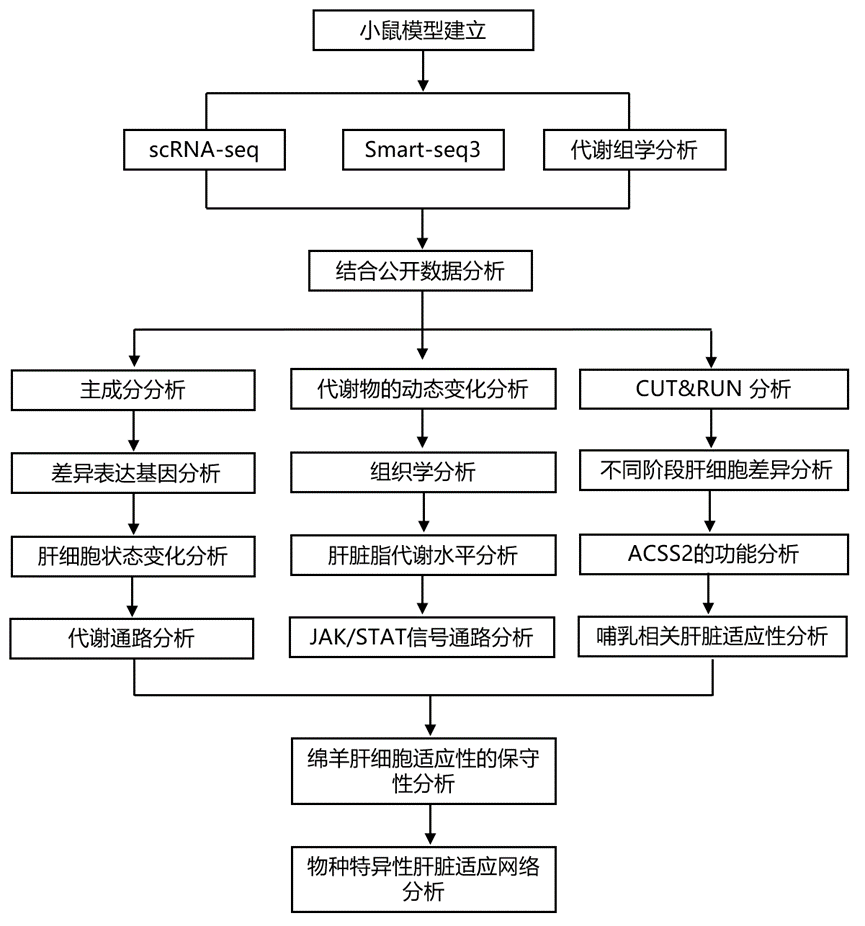
结 果
01
妊娠和哺乳期肝细胞的动态状态
为了研究妊娠期和产后肝细胞状态的转变,研究团队从约8周龄C57BL/6J小鼠中分离了单个肝细胞。对21个生殖阶段(包括哺乳期和非哺乳期)进行了单细胞转录组分析(scRNA-seq)(图1 A)。鉴于10× Genomics等高通量方法在小鼠肝细胞中的基因检测率较低(每个细胞约2000个基因),他们主要使用了Smart-seq3xpress(Smart-seq3)技术,这是一种基础良好、灵敏度高的测序方法,每个细胞可检测到约8000个基因。
三维 (3D) 均匀流形近似和投影 (UMAP) 分析显示,肝细胞状态在妊娠期、产后非哺乳期和哺乳期发生动态变化(图1B)。妊娠期和非哺乳期肝细胞形成的聚类与哺乳期肝细胞不同(图 1B)。虽然肝细胞功能受分区的强烈影响,但分析表明,生殖阶段而不是分区区域主要决定了肝细胞聚集(图 1B-C)。分区模式保持稳定并与状态转换正交,这表明生殖阶段而不是分区驱动代谢适应。为了明确控制与分区相关的转录变异,他们根据从已证实的门静脉周围和中枢周围标记基因计算出的分数回归整合出分区效应,从而鉴别出生物学相关的代谢适应特征。校正后,3D力导向布局 (FDL) 分析显示,妊娠期和产后非哺乳期肝细胞状态呈现圆形轨迹,最终在产后7天非哺乳期 (P7-NL) 恢复到基线G0状态,并在产后0天出现一条明显的分支路径,延伸至哺乳期(图 1D)。这些轨迹对应两种不同的代谢程序:一种引导肝细胞在产后非哺乳期恢复代谢稳态,另一种反映哺乳期特异性重编程以满足哺乳能量需求(图 1D)。总之,这些发现凸显了肝细胞与分区无关的阶段依赖性适应性策略。
他们首先分析了妊娠期和产后非哺乳期小鼠的肝细胞。3D 主成分分析(PCA)揭示了肝细胞状态在这些阶段的动态周期性轨迹,不同区域的细胞遵循相似的路径。校正与分区相关的变异后,肝细胞沿着前两个主成分 (PC) 排列,经历生殖期并返回基线[妊娠第 0 天(G0)]状态(图1E-F)。
PC1 上的细胞呈正态分布,在G14.5 达到峰值,而 PC2 评分在整个妊娠期和产后非哺乳期波动(图1G-I)。PC2相关基因变化出现得早于 PC1,表明 PC2 相关通路的响应速度更快(图1G-I)。为了评估轨迹的统计稳健性和潜在的子聚类,他们进行了敏感性分析,将每个阶段的肝细胞下采样至 150、100 和 50 个,包括 5 个独立的 50 个细胞重复。所有子集均重现了完整数据集的圆形轨迹和 PC 模式,证实了稳定性和可重复性。层次聚类分析显示,425个PC2相关和986个PC1相关的可变表达基因(VEG)之间存在两个不同的聚类,分别称为聚类-1/-2和聚类-1′/-2′(图1 J-K)。基因集变异分析(GSVA)确定了与这些聚类相关的特定生物学途径(图1L-M)。
聚类1基因从妊娠早期开始上升,在G14.5左右达到峰值,并随着分娩逐渐下降(图1 J)。该聚类在与葡萄糖代谢、能量代谢、糖异生和脂质生物合成相关的通路中富集(图1 L)。值得注意的是,脂肪生成酶Fasn在妊娠早期高表达,反映了合成代谢增强以支持胎儿生长。聚类1' 基因主要在妊娠晚期上调,并在产后恢复到基线(图1K)。这些基因在脂质代谢和分解代谢途径中富集,表明脂质利用增加。“Janus 激酶 (JAK)/信号转导与转录激活因子 (STAT) 信号通路”和“细胞因子介导的信号传导”的额外富集表明在此阶段肝脏调节活跃。“急性炎症反应”和“对内质网 (ER) 应激的反应”途径的存在表明妊娠晚期代谢和生理应激增加(图 1M)。凝血酶(F2)等凝血基因的上调意味着在分娩前后肝组织修复中发挥作用(图 1M)。值得注意的是,妊娠期适应的关键转录因子Ascl1在转录本和蛋白质水平均升高(图1 K)。聚类1和聚类1′基因也在细胞增殖途径中富集,反映了妊娠期间肝细胞增殖的增强(图1L-M)。
聚类2 基因从 G3.5 开始逐渐下降,在 G12.5 左右达到最低值,并在产后逐渐恢复(图 1J)。这些基因与内吞作用、自噬和细胞周期的负调控有关,提示其在产后肝脏重塑中发挥作用(图1L)。聚类2′ 基因在整个妊娠期受到抑制,但在产后得到恢复,这些基因在解毒、外来生物代谢和成熟肝脏功能(如细胞色素 P450 活性以及脂质、碳水化合物、氨基酸和胆汁酸的代谢)中富集(图1K-M)。这些发现表明成熟的肝功能在妊娠期间下调,在出生后恢复。为了验证肝细胞状态转变的周期性,他们应用了圆形主成分分析 (CCA),并使用连接肝细胞聚类质心(G0 至 G14.5 和 G10.5 至 P0)的垂直平分线的交点定义了一个中心参考点(“点 O”)。基于此参考,他们分析了沿转录轨迹的细胞顺序指数,定量证实了整个妊娠期和产后恢复过程中的周期性进展(图1N-O)。该框架表明肝细胞转录状态遵循可重复的周期,最终在产后非哺乳期恢复到妊娠前状态。
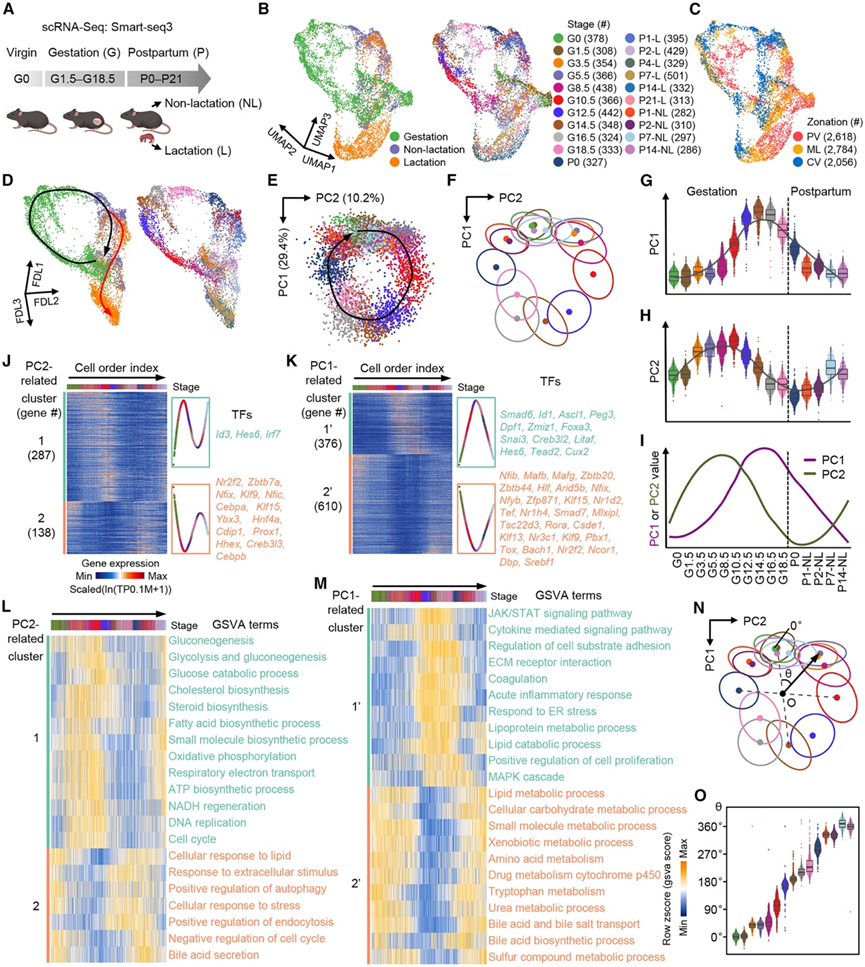
图1. 妊娠期和产后肝细胞状态转变。
(A)对未孕小鼠、妊娠小鼠和产后小鼠肝细胞分析流程。(B) 3D UMAP 图显示肝细胞在不同生物学过程(左)和生殖阶段(右)的分布。(C) 3D UMAP 图根据妊娠期和产后肝脏分区对肝细胞进行分类。(D) 3D FDL 图显示肝细胞运动轨迹,其中圆形(黑色)和分支(红色)路径分别表示有或非哺乳时的代谢转变。(E-F) 经分区回归后的 PCA 图,揭示了周期性轨迹。(G-H) 不同阶段的 PC1和 PC2分布的箱形散点图。(I) Loess 曲线模拟了 PC1 和 PC2 随时间的变化。(J-K) 与 PC2 (J) 和 PC1 (K) 相关的可变表达基因 (VEG) 热图。(L-M) GSVA 热图显示与 PC2和 PC1相关的基因集的富集。(N-O) PCA 图和散点图显示了从 G0 到 P14-NL 的周期性妊娠时钟上的细胞顺序指数。
02
妊娠期肝脏适应的代谢验证
为了验证转录组学结果并阐明妊娠期间肝脏代谢的适应性变化,他们对妊娠和产后多个阶段进行了代谢组分析,定量分析了肝细胞中的糖原、甘油三酯(TG)、总胆固醇(TC)和极低密度脂蛋白(VLDL),以及母体血清中的葡萄糖、TG、TC和酮体(主要为乙酰乙酸和β-羟基丁酸)为了控制饮食的影响,小鼠在取样前进行了标准化的6小时禁食。肝脏样本通过下腔静脉灌注采集,血清样本通过心脏穿刺采集。此外,他们还测量了尾尖血的空腹血糖水平,以评估全身葡萄糖稳态。其他参数包括母体肝脏重量、循环血容量、肝细胞增殖(Ki67 染色)和食物摄入量(图 2 A-M)。
妊娠期间肝糖原呈现双相变化模式,在妊娠3.5天(G3.5)达到峰值,妊娠中期下降,并在妊娠14.5天(G14.5)回升(图2A)。早期峰值反映了葡萄糖摄取、氧化磷酸化和ATP生成增强,而妊娠中期下降则与葡萄糖分解代谢增强相一致。妊娠晚期回升与脂质分解代谢增加和TG分解释放甘油相吻合(图1L-M)。通过PAS染色从组织学上证实了糖原的动态变化(图2N-O)。肝脏TC水平在妊娠第5.5天(G5.5)后显著升高,在妊娠第8.5天(G8.5)达到峰值,随后下降直至分娩(图2B)。早期升高与胆固醇和甾醇生物合成的激活相一致,而后期下降则与类固醇分解代谢的增加相对应。
受孕后肝脏TG水平最初下降,可能反映了早期代谢调整,随后稳步上升,在妊娠第8.5天(G8.5)达到峰值(图2C)。这种积累与脂肪酸合成和脂滴形成相关基因的上调相一致,从而满足了胎儿的能量需求。从妊娠第10.5天(G10.5)开始,随着脂质分解代谢途径的激活增强,TG水平下降。TG动员增强促进了妊娠晚期的酮体生成和糖异生,为母体和胎儿提供了替代能量底物。油红O染色证实了这些脂质动态变化(图2P-Q)。极低密度脂蛋白(VLDL)介导的脂质输出在妊娠晚期也显著增加,与胎儿的能量需求相一致(图2D)。
血清代谢物模式与肝脏代谢趋势密切相关。血清葡萄糖在妊娠早期达到峰值,妊娠中期出现一个较小的峰值,随后在妊娠晚期下降,这与肝糖原动态变化一致(图2A-E)。血清总TC在妊娠5.5天后下降,在妊娠10.5天达到最低点,短暂回升后持续下降(图2F)。肝脏高密度脂蛋白胆固醇(HDL-C)水平并未升高,表明HDL摄取并非血清TC降低的主要驱动因素,提示母体胆固醇在早期胚胎发育中发挥了重要作用。血清TG的变化与肝脏TG的变化平行,在妊娠14.5天达到峰值,反映了脂质动员用于酮体生成(图2G)。酮体水平升高为母体提供了替代能量来源,从而为胎儿保留了葡萄糖(图2H)。
在非哺乳期小鼠中,肝脏重量从妊娠第5.5天(G5.5)开始增加,在妊娠第14.5天(G14.5)达到峰值,然后在产后下降至基线水平(图2 I)。肝细胞增殖在妊娠第5.5天(G5.5)急剧上升,并持续升高至妊娠第14.5天(G14.5),然后在产后恢复至基线水平,这与增殖相关基因的上调相一致(图2K-L)。血容量增加至妊娠第12.5天(G12.5)达到平台期,然后在分娩时下降,并在产后继续减少(图2J)。在非哺乳期雌性小鼠中,按体重标准化的食物摄入量在妊娠和产后保持稳定(图2M),表明总摄入量与体重成正比。这些发现强调了在妊娠晚期,肝脏和全身代谢物对胎儿的大量支持。总的来说,这些分析强调了协调的肝脏和全身代谢适应对于满足整个妊娠期间母胎能量需求至关重要。
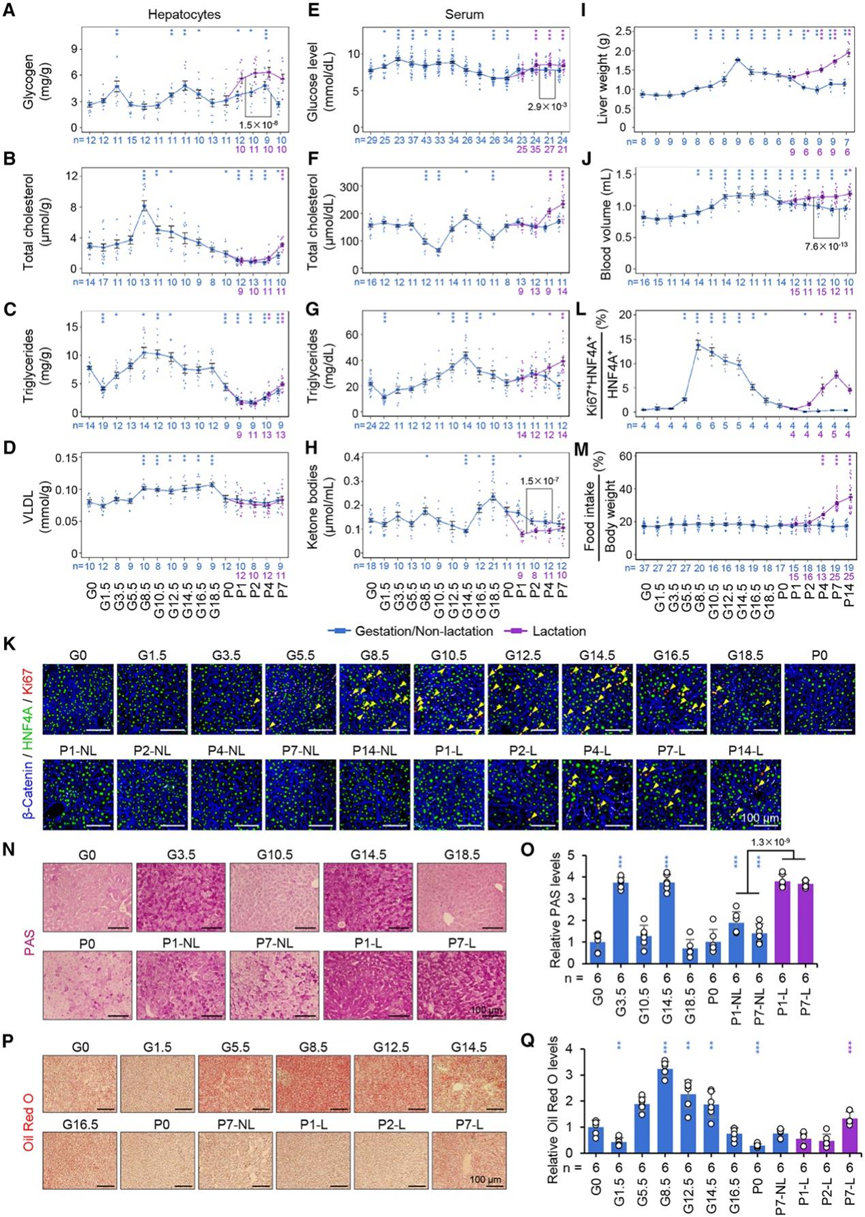
图2. 妊娠和哺乳期间肝细胞和血清中关键代谢物的动态。
(A-D) 妊娠期和产后阶段肝糖原、TC(B)、TG和VLDL的时间变化。(E-H) 相应阶段的葡萄糖、TC、TG和酮体的循环水平。(I) 妊娠期和产后阶段的母体肝脏重量。(J) 通过心脏穿刺测量的最大血容量。(K) Ki67、HNF4A 和 β-catenin 染色的肝切片免疫荧光图像分析。(L) Ki67+HNF4A+细胞占总HNF4A+肝细胞的百分比。(M) 妊娠和哺乳期间的标准化食物摄入量。(N-O) PAS 染色(N)和糖原储存的定量。(P-Q) 油红O染色和肝脏脂质蓄积的定量。
03
肝细胞适应中的JAK/STAT信号通路
为了研究妊娠期间肝细胞状态转变的调控机制,他们重点关注了JAK/STAT通路,该通路在聚类1′基因中富集(图1M)。Stat3、Stat2和Stat6的表达在妊娠期间增加。该通路可由白细胞介素-6(IL-6)等细胞因子激活,IL- 6在妊娠14.5天(G14.5)血清中升高,这与妊娠人和大鼠的研究结果一致。IL-6通过糖蛋白130(gp130)传递信号。为了评估gp130的作用,他们在Il6stfl/fl小鼠交配前,使用重组腺相关病毒(rAAV)载体rAAV8-Tbg-Cre特异性敲除了肝脏中的Il6st基因(编码gp130)(图3A)。在 G14.5 时,Il6st敲除 (KO) 肝细胞与WT对照组相比,gp130 蛋白明显减少(图 3 B)。
scRNA-seq结果显示,在基线期(G0)WT和Il6st KO组肝细胞之间转录差异极小,但在G14.5时出现显著差异。主成分分析(PCA)证实,WT和KO细胞在G0时聚类在一起,但在G14.5时显著分离(图3C)。层级聚类分析揭示了G14.5时相反的表达模式(图3 D),强调了Il6st缺失导致肝细胞适应性受损。在G14.5时,KO肝细胞中Stat3、Stat2和Ascl1的表达显著下调。将KO细胞投射到妊娠期PCA轨迹上显示,与WT相比,KO细胞沿PC1轴的进展延迟(图3E-F)。鉴于 JAK/STAT 通路在 PC1 相关过程中的富集,这些结果突显了 gp130 在妊娠期间肝细胞代谢适应中的关键作用。
GO分析显示,Il6st KO肝细胞中参与脂质分解代谢、脂质稳态和内质网应激反应的基因表达降低(图3G)。生化分析表明,与WT相比,KO肝细胞中脂质含量和TG积累增加(图3H-I)。油红O染色独立证实了KO肝脏中脂质动员受损(图3J-K)。此外,虽然WT小鼠妊娠期间血清TG水平升高,但G14.5 KO小鼠的血清TG水平显著降低(图3L)。KO肝细胞还表现出与ATP代谢、线粒体组织和小分子分解代谢相关的基因表达升高,表明代谢压力和能量需求增加(图3G)。
通过 Ki67 染色和肝脏/体重比评估,野生型 (WT) 小鼠妊娠期间肝细胞增殖增加,但在 G14.5 Il6st KO 小鼠中显著降低(图3M-O)。鉴于母体肝脏增殖和脂质合成在胎儿发育中的关键作用,他们分析了胎儿结局,虽然胎儿数量未受影响,但在胚胎第 14.5 天 (E14.5),母体Il6st基因缺失后胎儿体重显著下降(图 3P-Q)。
生化验证显示,Il6st KO肝细胞中磷酸化STAT3 (pSTAT3) 水平显著降低(图S3 J),表明JAK/STAT信号通路激活受损。为了探究gp130-JAK/STAT信号通路与代谢紊乱之间的机制联系,他们进行了靶向切割和核酸酶释放 (CUT&RUN) 分析,结果显示Il6st KO肝细胞中646个基因组位点的STAT3结合显著减少(图3 R-S)。这些位点主要与脂质代谢和能量稳态相关,验证了JAK/STAT信号通路紊乱驱动KO肝细胞中代谢基因表达改变(图3T-V)。虽然 gp130 可能与其他效应因子相互作用,但整合的转录组学、生物化学和表观基因组学数据有力地支持 gp130-JAK/STAT 信号传导是妊娠期间肝脏代谢转变的关键调节通路。
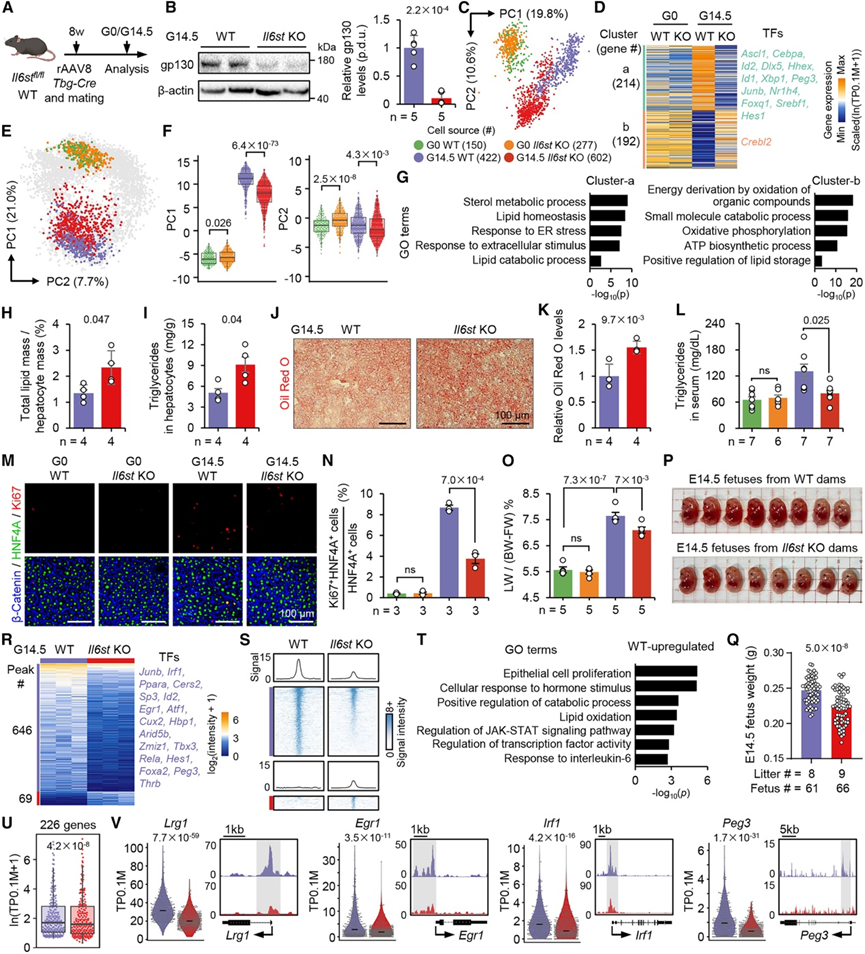
图3. l6st KO损害妊娠期间肝细胞适应和胎儿发育。
(A) 妊娠期间肝脏特异性Il6st KO的实验流程。(B) G14.5 WT 和 KO 肝细胞中 gp130 蛋白水平的免疫印迹(左)并以 β-肌动蛋白为标准化定量(右)。(C) G0和G14.5肝细胞各基因型的PCA图。(D) 四个细胞群中野生型(WT)和敲除型(KO)肝细胞在G14.5时的DEG热图。(E-F) 野生型和敲除型肝细胞在妊娠/产后轨迹上的 PCA 投影及其沿 PC1 和 PC2 的分布。(G) GO分析。(H-I) 肝细胞中总脂质和 TG 的定量。(J-K) G14.5 WT和KO肝细胞的油红O染色和定量。(L) G0 和 G14.5 WT 和 KO 小鼠的血清 TG 水平。(M-N) 免疫荧光染色和定量分析。(O) G0 和 G14.5 时的肝脏与体重比,按所示进行标准化。(P-Q) WT 和 KO 母鼠 E14.5 胎儿的图像和体重量化。(R) 差异富集的 STAT3 峰的热图。(S) 复合图和信号强度图显示代表性的 STAT3 结合区域。(T) GO分析。(U) 相关基因的表达水平以散点箱线图显示。(V)基因表达分析。
04
哺乳期与非哺乳期肝细胞适应性存在差异
鉴于产后哺乳期和非哺乳期肝细胞之间存在显著差异(图1D),他们研究了围产期(G18.5、P0、P1和P2)肝细胞的适应性变化。三维主成分分析(3D PCA)和三维扩散图谱揭示了不同的变化轨迹:P2时期(P2)的哺乳期肝细胞(从哺乳期小鼠中分离)沿着哺乳特异性通路进一步演化,而同一时期(P2-NL)的非哺乳期肝细胞则与P1-NL相似(图4A)。这些结果表明,哺乳驱动了肝细胞状态的进一步转变。
差异表达基因(DEG)分析鉴定出701个基因,其中包括21个转录因子,这些基因与肝细胞轨迹分化为哺乳期和非哺乳期状态相关(图4B)。这些基因形成三个基因聚类:产前(聚类a)、产后非哺乳期(聚类b)和产后哺乳期(聚类c)(图4B)。聚类a基因在产前阶段(G18.5,P0)高表达,富集于内质网应激和细胞外刺激反应,反映了分娩期间的生理应激(图4C)。在聚类b中,与脂质分解代谢、转运和药物代谢相关的通路上调,支持营养物质动员和肝脏稳态恢复(图4C)。值得注意的是,凋亡相关通路显著富集(图4C),这与产后肝细胞凋亡增加相一致(图4D)。非哺乳期肝细胞中caspase-7表达升高以及通过末端脱氧核苷酸转移酶介导的dUTP缺口末端标记(TUNEL)染色检测到的凋亡细胞数量增加证实了这一点,突显了凋亡在肝脏大小恢复中的作用(图4E-G)。
为了评估细胞凋亡在产后肝脏重塑中的功能作用,他们利用rAAV8介导的CRISPR-Cas9系统在妊娠14.5天(G14.5)敲除了肝细胞中的caspase-7(Casp7)基因,并在产后4天(P4-NL)进行分析(图4H-I)。Casp7基因敲除显著减少了TUNEL阳性凋亡肝细胞的数量(图4J-K),并延缓了肝脏体积的缩小,导致肝脏/体重比值增加(图4L)。这些结果表明,细胞凋亡是产后肝脏重塑的主动驱动因素,而非代谢变化的被动结果。
相反,哺乳期肝细胞(聚类c)显著上调了包括甾醇生物合成在内的合成代谢过程,以满足产奶的能量需求(图4C)。虽然哺乳期和非哺乳期肝的细胞均增强了脂质代谢和外源性物质反应,但这些过程可能具有不同的功能:非哺乳期肝细胞可能促进脂质分解代谢和解毒以促进肝脏恢复,而哺乳期肝细胞似乎上调脂质生物合成和外源性物质防御以支持产奶,并可能保护后代免受乳汁传播毒素的侵害。虽然通路存在重叠,但其相关的基因集却有所不同(图4C),这凸显了功能适应性的差异——分解代谢恢复与合成代谢支持哺乳。
为了表征哺乳诱导的肝细胞适应性,他们进行了代谢PCA分析,并使用细胞顺序指数研究了细胞位置。结果显示,从分娩(P0)到哺乳早期(P4-L),肝细胞逐渐发生变化,并在哺乳后期(P21-L)趋于稳定(图4M-N)。P1-L 和 P2-L 代表了从妊娠到哺乳的过渡阶段。与围产期相比,这两个阶段乳汁合成代谢途径的表达增强,但脂质分解代谢活性仍高于后期阶段(P7-L 至 P21-L)(图 4O-P),表明脂质动员逐渐向持续脂质合成转变。
产后早期肝细胞(聚类1)中与蛋白质错误折叠、分解代谢和应激反应相关的基因表达下调——这些基因在分娩时表达升高——表明妊娠应激在哺乳期得到缓解(图4O-P)。细胞周期负调控的富集也提示肝细胞增殖增强(图4P)。相反,聚类2基因在哺乳期显著上调,特别是那些参与氧化磷酸化、ATP合成、乙酰辅酶A(CoA)代谢以及脂肪酸和胆固醇生物合成的基因,反映了肝脏能量产生和脂质合成增加,以促进乳汁分泌(图4O-P)。
为了验证哺乳期代谢活动增强的转录组特征,他们检测了线粒体ATP合酶活性、ATP生成量和脂肪酸合成酶(FAS)活性。这些检测结果显示,与P1-L组相比,P7-L组肝细胞的上述指标显著升高,表明线粒体氧化能力和脂肪酸合成增强(图4Q-S)。Seahorse细胞代谢通量分析[氧消耗率(OCR)和细胞外酸化率(ECAR)]进一步证实了这一点:P7-L组肝细胞的基础呼吸、最大呼吸、储备呼吸能力和ECAR均较高,这与氧化磷酸化和糖酵解通量的增加相一致(图4T-U)。
与功能数据一致,哺乳期肝糖原、TG和TC含量逐渐增加。到哺乳期第7天(P7-L),TG和TC含量恢复至接近基线水平(G0),而糖原含量仍保持较高水平(图2A-C)。油红O染色证实了哺乳期肝细胞中脂质的积累,而非哺乳期肝细胞中则未见脂质积累(图2P-Q)。这些变化伴随着能量摄入的急剧增加。与妊娠期或非哺乳期小鼠相比,P7-L和P14-L小鼠的标准化食物摄入量(按体重计算)分别增加了1.8倍和2.1倍(图2M)。每日绝对摄入量也增加,与非哺乳期对照组相比,P7-L和P14-L小鼠分别增加了2.3倍和2.4倍。这些增长与肝细胞增殖、肝脏重量和血容量的增加平行(图2I-M),反映了系统和肝脏为满足牛奶生产需求而进行的协调适应。
血清代谢物分析结果与肝脏变化相一致,哺乳期血清葡萄糖、TG和TC水平逐渐升高。到产后第7天(P7-L),TG和TC水平升高约1.5至2倍,葡萄糖水平较基线(G0)升高超过10%(图2E-G)。虽然产后肝脏TG和TC水平恢复至基线水平,但哺乳期肝细胞表现出脂质合成和输出增加,而非储存增加(图2B-C),这与脂质合成基因(例如Fasn)的上调相一致。哺乳期血清酮体水平迅速恢复正常,但在非哺乳期小鼠中则维持较高水平更长时间,表明酮体在哺乳早期能量供应中发挥着关键作用(图2H)。胰岛素受体信号传导在妊娠晚期下调,有利于胎儿葡萄糖分配,在哺乳期仍然受到抑制,支持脂质合成、VLDL 分泌和外周脂质动员以促进乳汁生产。
为了评估哺乳诱导的肝细胞状态的逆转,他们对断奶后多个时间点(P7-L + d1-NL、d2-NL、d4-NL 和 d7-NL)采集的肝细胞进行了scRNA-seq。整合到妊娠-哺乳轨迹中(图1 D)显示,肝细胞逐渐偏离哺乳特异性状态,P7-L + d7-NL 肝细胞聚集在 G0 和 P7-NL 细胞附近(图4 V-W),表明其转录水平恢复到妊娠前基线水平。
值得注意的是,断奶后仅1天(P7-L + d1-NL),肝细胞就表现出显著的转录变化,与P7-L组相比,有120个基因上调,354个基因下调(图4 X)。GO分析显示,下调基因富集于脂质代谢相关通路,包括乙酰辅酶A、甘油三酯代谢和脂质/葡萄糖调节。上调基因则与外源性物质解毒、免疫反应、激素和类固醇代谢以及金属离子处理相关。这些结果表明,断奶后脂质生物合成迅速受到抑制,肝脏稳态功能得以恢复。
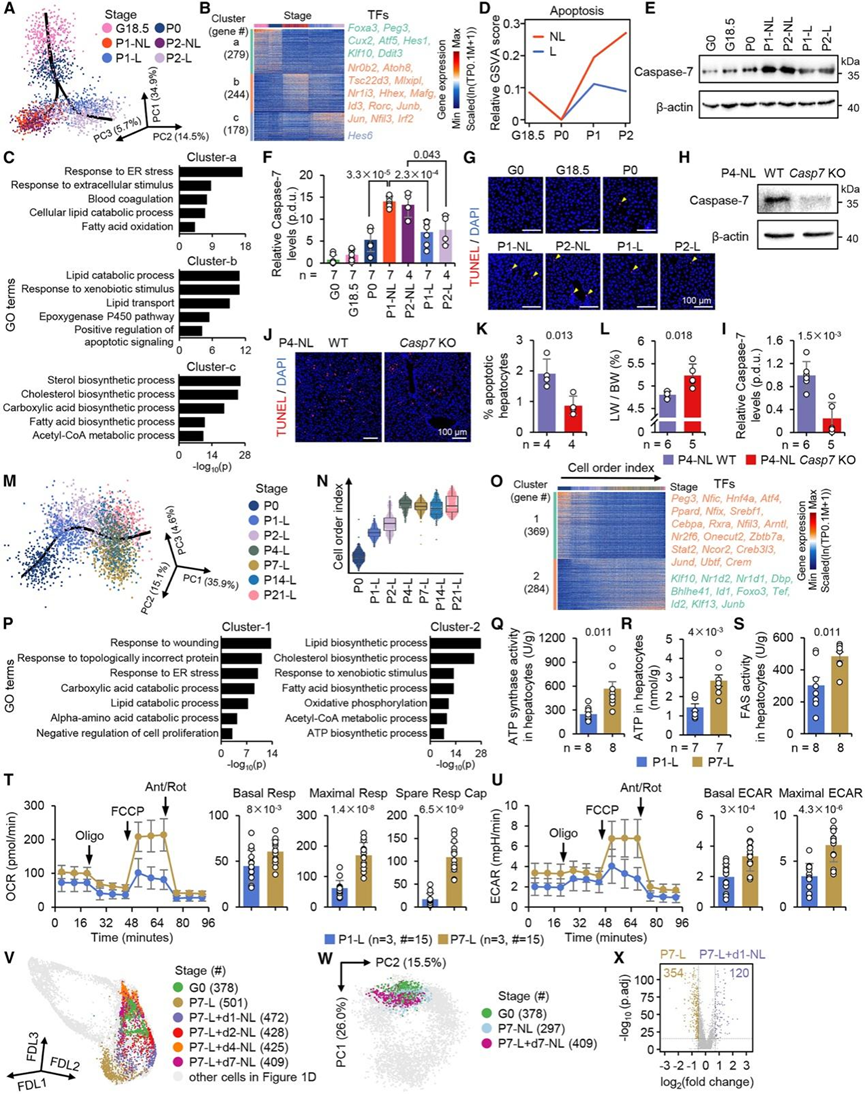
图4. 哺乳期和非哺乳期产后肝细胞轨迹不同。
(A) 3D PCA 图显示围生期肝细胞运动轨迹分为哺乳期和非哺乳期。(B) 围产期DEG热图。(C)GO分析。(D) GSVA 曲线显示围生期“细胞凋亡”通路活性。(E-F) 分析各个阶段的 Caspase-7 蛋白水平,并以 β-actin 进行定量标准化。(G) 不同生殖阶段肝切片的TUNEL染色。(H-I) P4-NL Casp7 KO 小鼠肝细胞中Casp7缺失的免疫印迹验证和定量。(J-K) P4-NL Casp7 KO 与 WT中肝细胞凋亡的 TUNEL 染色和定量。(L) P4-NL Casp7 KO 和 WT 小鼠的肝脏与体重比。(M-N) 沿哺乳特定轨迹的肝细胞 3D PCA 图和箱线图。(O-P) GO分析。(Q-S) 哺乳肝细胞中 ATP 合酶活性、ATP 水平和 FAS 活性的定量。(T-U) Seahorse细胞代谢通量分析。(V) 3D FDL 图显示 P7-L + d1-NL、d2-NL、d4-NL 和 d7-NL 肝细胞整合到妊娠-哺乳轨迹中。(W) PCA 图将 P7-L + d7-NL 肝细胞投射到图 1 E中定义的轨迹框架上。(X) P7-L 和 P7-L + d1-NL 肝细胞之间的 DEG 火山图。
05
ACSS2在哺乳期脂质生物合成和肝脏代谢调节中的作用
他们研究了哺乳期肝细胞状态的转变,重点关注脂肪酸生物合成(图4C-P)。胞质乙酰辅酶A是脂肪酸和甾醇合成的关键碳源。乙酰辅酶A合成酶2 (ACSS2) 在细胞核和细胞质中将乙酸转化为乙酰辅酶A,参与脂质合成和组蛋白乙酰化。免疫印迹分析显示,哺乳期肝细胞中ACSS2表达显著升高(图5A)。为了评估ACSS2在哺乳期的具体功能,他们在妊娠14.5天(G14.5)向Acss2fl/fl和WT小鼠注射了rAAV8-Tbg-Cre,有效降低了产后4天(P4-L)的ACSS2蛋白水平(图5B-C)。
他们对P4-L期野生型(WT)和Acss2敲除(KO)小鼠的肝细胞进行了scRNA-seq。主成分分析(PCA)显示,Acss2 KO小鼠肝细胞的表达谱显著偏离了哺乳相关的适应性变化轨迹,表明其肝脏适应性受损(图5D)。转录组分析鉴定出KO小鼠肝细胞与WT小鼠肝细胞相比有835个DEG(748个下调,87个上调)(图5E)。下调基因主要富集于脂质生物合成、氧化和转运通路(图5F),表明肝脏脂质代谢紊乱。
虽然Acss2敲除肝细胞中胞质乙酰辅酶A水平保持不变,但转录组学和生化分析显示下游脂质生物合成和输出显著受损。这种差异可能反映了糖酵解酶(如G6pc、Pcx、Gapdh、Aldoa、Aldob和Ldha)的代偿性上调,这些酶可能在缺乏ACSS2的情况下部分维持乙酰辅酶A的产生。
ACSS2缺失的一个关键后果是载脂蛋白B (ApoB) mRNA和蛋白水平的表达均显著降低(图5G-H),从而损害了极低密度脂蛋白(VLDL)的组装和脂质输出。因此,Acss2 KO 的肝细胞表现出大量的脂滴积累,油红O染色和肝脏TG含量升高(图5I-K)。值得注意的是,这种脂质滞留并非由于合成增加所致,因为从头脂肪生成减少,表明脂质输出存在特异性缺陷。在系统层面,Acss2基因敲除小鼠循环中的TG和TC水平降低(图5L-M),限制了乳汁合成所需的脂质供应。因此,Acss2 KO小鼠的乳汁中TG和TC水平显著降低,导致总能量密度下降,而蛋白质和碳水化合物含量保持不变(图5N)。这种营养缺乏损害了子代的生长,尽管产仔数正常且乳腺形态完整,但幼崽体重显著降低(图5O-Q)。值得注意的是,Acss2 KO小鼠在出生后第4-10天(P4-L)和第7-10天(P7-L)的食物摄入量减少了约30%(图5R),这可能反映了肝脏合成代谢活性受损和能量需求降低的反馈反应。
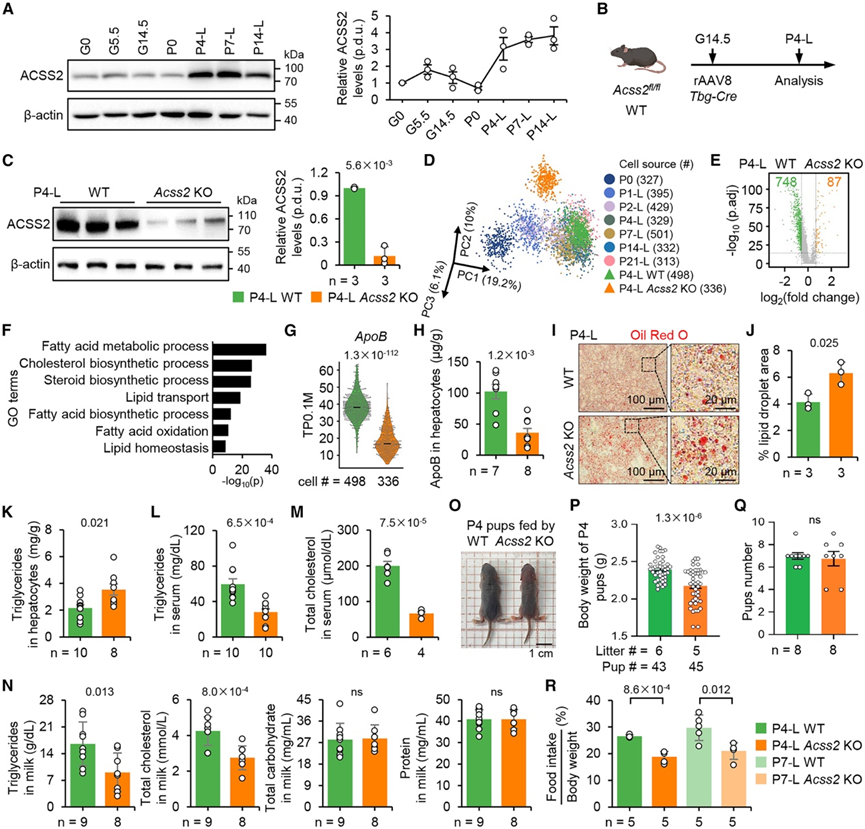
图5. ACSS2缺陷破坏哺乳相关的肝脏适应。
(A) 对妊娠期和产后肝细胞中的 ACSS2 蛋白水平进行免疫印迹分析。(B) 哺乳期小鼠肝脏特异性Acss2 KO 策略示意图。(C) Western blot 验证 P4-L KO 小鼠肝细胞中 ACSS2 的缺失。(D) 3D PCA 图显示 P4-L WT、KO 和过滤的肝细胞。(E) P4-L WT 和 KO 肝细胞之间的 DEG 火山图。(F) GO分析。(G-H) P4-L WT 和 KO 肝细胞(非禁食)中 ApoB 的 mRNA 和蛋白质水平。(I-J) 肝切片中脂滴面积的代表性油红 O 染色和定量分析。(K-M) 非禁食小鼠的肝脏TG水平(K)和血清TG(L)和TC浓度。(N) P4-L WT 和 KO 的肝细胞所含有的成分。(O-Q) 野生型和敲除型母鼠的代表性幼崽图像、体重和产仔数量。(R) P4-L和 P7-L WT 和 KO 小鼠的标准化食物摄入量。
06
绵羊肝细胞适应性的保守性
鉴于肝脏适应性变化对胎儿发育和乳汁质量的重要性,他们将研究对象扩展至绵羊——一种重要的草原家畜。他们从22只母羊的妊娠期(约150天)内采集了肝脏样本(图6A),并根据胎儿头臀长估算妊娠阶段。为了考虑发育变异性,他们将样本分为七个阶段。此外,他们还从四只哺乳期母羊中采集了肝脏样本,其中两只处于妊娠第7天至哺乳期(P7-L),两只处于妊娠第15天至哺乳期(P15-L)(图6A)。与小鼠类似,如肝脏与体重的比值所示,妊娠和哺乳期间肝脏体积显著增大。
他们对这些样本进行了Smart-seq3测序,并去除了低质量细胞和非肝细胞。最终数据集包含3404个肝细胞,平均每个细胞检测到6300个基因。与小鼠类似,在绵羊肝细胞中也发现了保守的区域分布模式(PV、ML和CV)。校正区域分布后,虽然缺乏非哺乳期动物的数据,但3D PCA分析仍揭示了妊娠期和产后肝细胞不同的适应性轨迹,这与小鼠的观察结果一致(图6B-C)。
为了表征妊娠特异性适应,他们在二维PCA空间中可视化了细胞进程,并使用细胞顺序指数分析了细胞位置(图6D)。肝细胞在整个妊娠过程中表现出持续的转录变化(图6E)。对1195个与进程相关的基因进行层次聚类分析,揭示了三个不同的基因聚类(图6F)。基因聚类1在妊娠期间下调(图6F),富集于脂质代谢相关通路(图6G),表明肝功能下降。基因聚类2在妊娠早期达到峰值,随后下降(图6F),变化通路与能量代谢相关——脂质和类固醇生物合成、氨基酸和ATP代谢——提示妊娠早期葡萄糖利用和脂质合成增强(图6G)。聚类3 基因逐渐增加,与脂肪酸氧化和免疫反应相关,反映了妊娠晚期脂质利用率和代谢压力的增加(图 6G)。
在哺乳期,基于主成分分析(PCA)的轨迹分析显示,肝细胞状态从P7-L逐渐转变为P15-L(图6H)。层次聚类分析鉴定出两个基因聚类:聚类a(214个下调基因)和聚类b(421个上调基因)(图6I)。聚类a基因富集于血液凝固和免疫反应通路,反映了妊娠期升高后产后恢复至基线水平(图6J)。与小鼠数据一致,聚类b基因与脂肪酸生物合成和ATP合成相关,表明哺乳期肝细胞脂质生成增加和能量需求增加,油红O染色结果也支持这一结论(图6J-L)。
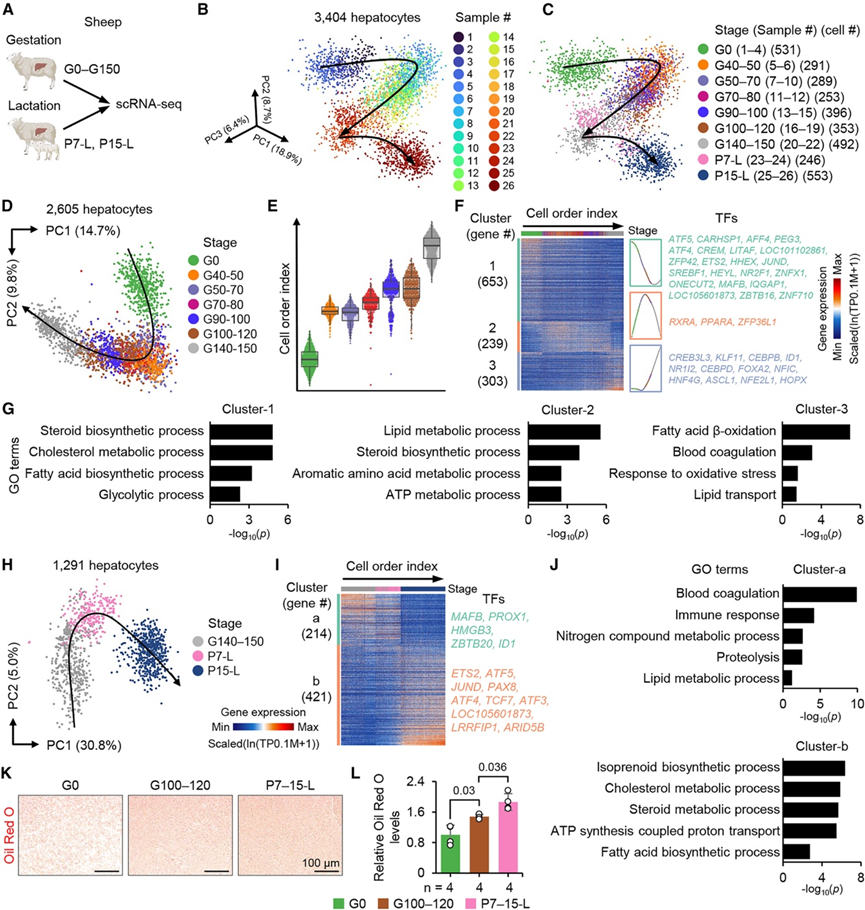
图6. 绵羊妊娠和哺乳期肝细胞适应情况。
(A) 分离不同妊娠和哺乳阶段的绵羊肝细胞的实验流程。(B-C) 3D PCA 图显示肝细胞在不同样本来源和发育阶段的轨迹。(D, H) 妊娠期和哺乳期肝细胞轨迹的 PCA 图。(E) 箱形散点图显示了(D)中沿细胞顺序指数的妊娠阶段特定分布。(F-I) 妊娠期和哺乳期VEG 热图。(G-J) GO分析。(K-L) G0、G100-120 和 P7-15-L 期肝组织切片经油红 O 染色后,并定量分析相应的染色强度。
07
物种特异性肝脏适应网络
为了比较小鼠和绵羊在妊娠和哺乳期肝脏的适应性变化,他们选取了具有代表性的时间段:妊娠期小鼠为G0至G16.5,绵羊为G0至G100-120;哺乳期小鼠为G18.5至P4-L,绵羊为G100-120至P15-L。许多同源基因在不同物种间存在重叠。对于妊娠期,他们基于PCA嵌入(PC1和PC2),并采用与先前分析一致的线性回归阈值,鉴定了轨迹基因(图6F)。
为了可视化妊娠期间保守的转录适应,他们鉴定了两种物种中基于轨迹的基因。在绵羊中,他们发现了982个与妊娠进展相关的基因——其中464个下调(聚类a),518个上调(聚类b)(图7A)。在小鼠中,他们鉴定了1175个此类基因——其中515个下调(聚类a′),660个上调(聚类b′)(图7B)。尽管存在物种特异性差异(图7C-D),但跨物种分析显示,有87个保守基因在妊娠期间持续上调,这些基因富集于有机酸生物合成和脂质分解代谢等通路(图7E)。值得注意的是,转录因子Ascl1高度保守且上调(图7D)。
在产前至哺乳期的过渡阶段,绵羊表现出887个DEG(G100-120时有291个聚类1基因;P15-L时有596个聚类2基因)(图7F)。小鼠则有990个DEG,其中G18.5时有251个聚类1′基因,P4-L时有739个聚类2′基因(图7G)。虽然产前基因聚类(聚类1和聚类1′)之间的重叠有限(图7H),但在哺乳期基因聚类(聚类2和聚类2′)中发现了76个共有基因,这些基因富集于胆固醇和脂质生物合成以及乙酰辅酶A代谢(图7I-J),包括关键的脂肪酸生物合成基因(Acss2、Acly、Acaca和Fasn)。虽然绵羊特异性抗体有限,但通过单细胞 RT-qPCR 验证了妊娠、产前或哺乳期选定的重叠基因。
为了阐明功能差异,他们对在两个物种中显著富集的同源基因进行了GO分析,重点关注与肝脏代谢适应相关的通路。GO网络显示,虽然涉及相似的生物学过程,但在小鼠和绵羊中激活的基因却不同(图7K)。在妊娠期,上调基因富集于脂质分解代谢、胆固醇代谢和核苷酸代谢,反映了妊娠后期脂质利用率的增加。在哺乳期,上调基因富集于类固醇生物合成、代谢物和能量生成、脂肪酸生物合成以及细胞解毒,表明产后脂质生成增强和肝细胞功能恢复(图7K)。
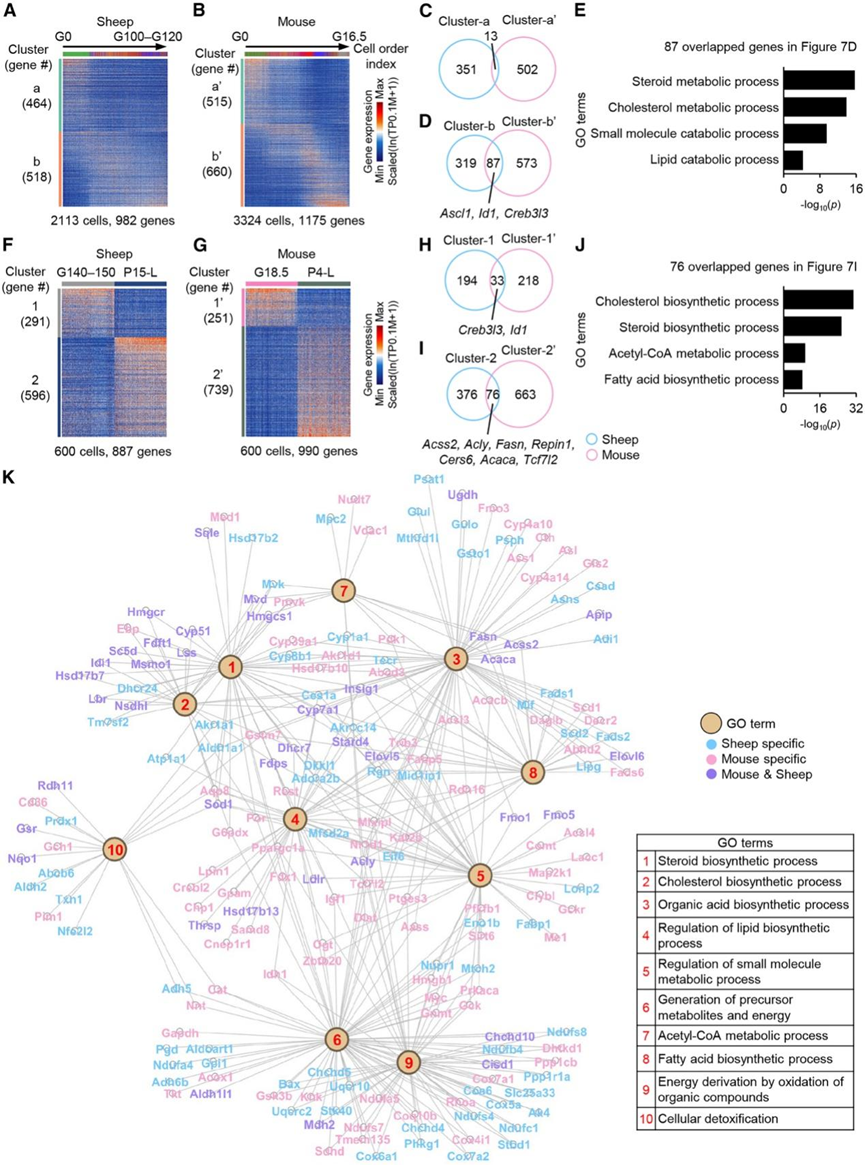
图7. 绵羊与小鼠肝细胞适应性比较分析。
(A-B) 绵羊和小鼠妊娠肝细胞中基因聚类和DEG的热图。(C-D) 维恩图显示不同生殖阶段DEG的重叠情况。(E) GO分析。(F-G) 绵羊和小鼠围产期和哺乳期肝细胞中 DEG 的热图。(H-I) 维恩图显示哺乳期间共有的 DEG。(J) GO分析。(K) 基因-GO网络分析。
+ + + + + + + + + + +
结 论
本研究利用高分辨率多组学技术,系统地表征了小鼠在妊娠和产后阶段肝细胞的适应性变化,发现了一个周期性的肝细胞轨迹(“妊娠时钟”),它调控着妊娠和产后恢复期间的代谢变化,并在非哺乳小鼠中恢复到妊娠前状态。哺乳诱导了一种独特的代谢分支轨迹,其特征是脂质合成和输出增加。糖蛋白130 (gp130) 的缺失会破坏妊娠期间的肝脏适应性变化,损害胎儿生长;而产后ACSS2的缺失则会损害肝脏脂质的生物合成和输出,降低乳汁脂质含量,并损害后代的发育。与绵羊的比较分析突显了物种间存在遗传差异,但肝脏代谢适应通路却高度保守。这些发现阐明了妊娠和哺乳期间肝细胞的可塑性,并确定了优化母胎健康和哺乳性能的潜在治疗靶点,对生殖生物学和畜牧管理具有重要意义。
+ + + + +



 English
English


