文献解读|Sci Adv(12.5):对骨关节炎进展和软骨下骨治疗至关重要的衰老干细胞群的多组学鉴定
✦ +
+
论文ID
原名:Multiomic identification of senescent stem cell populations critical for osteoarthritis progression and therapy in subchondral bones
译名:对骨关节炎进展和软骨下骨治疗至关重要的衰老干细胞群的多组学鉴定
期刊:Sciences Advances
影响因子:12.5
发表时间:2025.07.18
DOI号:10.1126/sciadv.adu2294
背 景
骨关节炎 (OA) 是一种全球流行的慢性退行性关节疾病,目前几乎没有有效的治疗方法可以阻止病情进展。晚期 OA 患者活动受限,生活质量下降,最终需要进行关节置换手术。随着全球老龄化人口和关节损伤的增加,受 OA 影响的人数持续增加,对预防和治疗策略的需求也随之增加,并给公共卫生系统和全球经济带来了沉重的负担。因此,全面了解 OA 进展的潜在机制对于制定有效的治疗策略至关重要。
实验设计
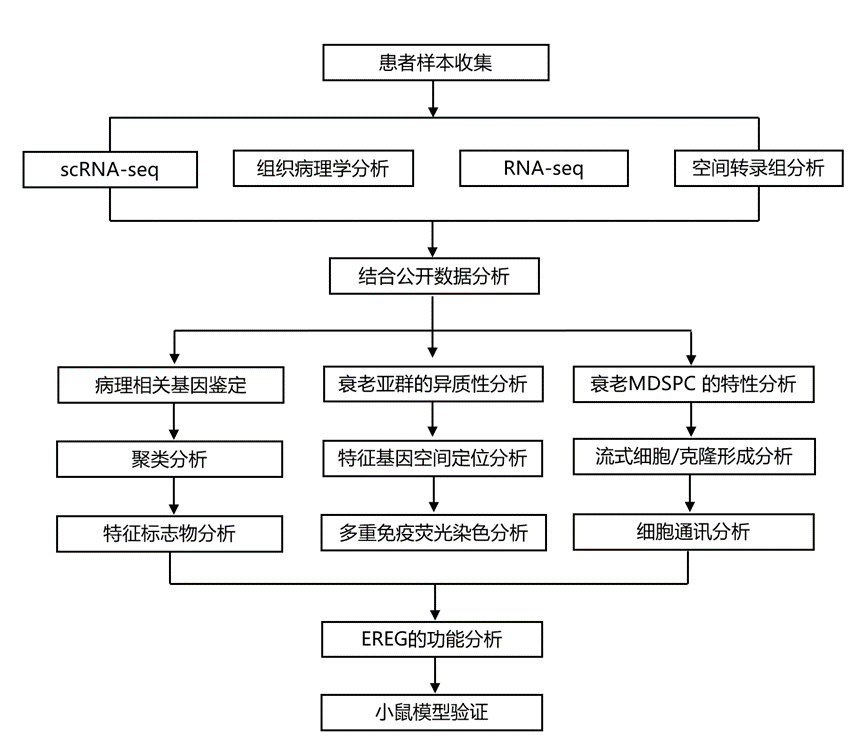
结 果
01
人类OA样本的scRNA-seq分析揭示了参与OA进展的主要病理细胞群
为了全面阐明OA进展的潜在机制,研究团队对OA患者I~II侧(Outerbridge I~II级)和III~IV侧(Outerbridge III~IV级)的胫骨平台全层组织[包括软骨、软骨下骨板(SBP)和软骨下骨小梁(STB)]进行了组织病理学评估和生物信息学分析(图1A)。组织病理学染色显示,III~IV侧骨软骨组织损伤更为严重,以关节软骨广泛破坏和软骨下骨结构异常为特征(图1B)。对每个OA样本的组织病理学评分一致表明,I~II侧样本的Mankin评分较低,骨软骨损伤较轻,而III~IV侧样本的Mankin评分较高,骨软骨损伤更严重(图1C)。
为了研究OA患者关节骨软骨组织中的细胞亚群,揭示与OA进展相关的病理事件,他们从3例OA患者胫骨平台I~II侧和III~IV侧各采集了6个骨软骨组织进行单细胞转录组分析(scRNA-seq)。经过数据质量控制和单细胞整合分析后,共获得38991个单细胞,其中I~II侧组织获得20364个单细胞,III~IV侧组织获得18627个单细胞。全基因表达分析显示,III~IV侧组织表达了更多病理基因,例如SPARC、FN1、IGFBP5和SERPINE2(图1D)。对3例OA患者样本进行定量聚合酶链式反应分析,证实这些差异表达基因(DEG)在III~IV侧组织中的表达显著高于I~II侧组织(图1E)。这些结果表明,I~II侧和III~IV侧组织之间的DEG能够详细地反映OA的进展。
均匀流形近似和投影 (UMAP) 可视化确定了 12 个不同的亚群(图 1F),所有这些亚群都存在于每个样本中,但是它们的比例略有不同。间充质来源的干细胞/祖细胞 (MDSPC)1 表达基质干细胞标志物NGFR和间充质标志物FOXC2;MDSPC2 表达间充质祖细胞标志物FGFR1和间充质标志物EGFR;MDSPC3 表达间充质基质细胞标志物TWIST1和干性标志物FZD7。成骨细胞(OB)表达ALPL、RUNX2和CDH11;软骨细胞表达COL2A1和ACAN;内皮细胞 (EC)表达PECAM1和CDH5;周细胞表达RGS5和ACTA2;T细胞表达CD3D和CD3E;B细胞表达CD79A和MS4A1;单核细胞/巨噬细胞表达CD14;树突状细胞(DC)表达CD80和CD86;破骨细胞 (OC)表达ACP5和CTSK(图1G)。跨聚类差异基因表达分析显示,MDSPC2和MDSPC3表现出与III~IV侧组织相关的DEG(即与进展相关的OA特征基因)的富集(图1H)。OA特征基因集评分进一步显示,MDSPC2和MDSPC3表现出明显的OA进展病理特征(图1I)。此外,I~II和III~IV侧组织之间的MDSPC2和MDSPC3的病理特征存在显著差异(图1J)。总之,这些发现揭示了 OA 进展过程中的细胞异质性,并将 MDSPC2 和 MDSPC3 确定为具有 OA 相关病理特征的亚群。
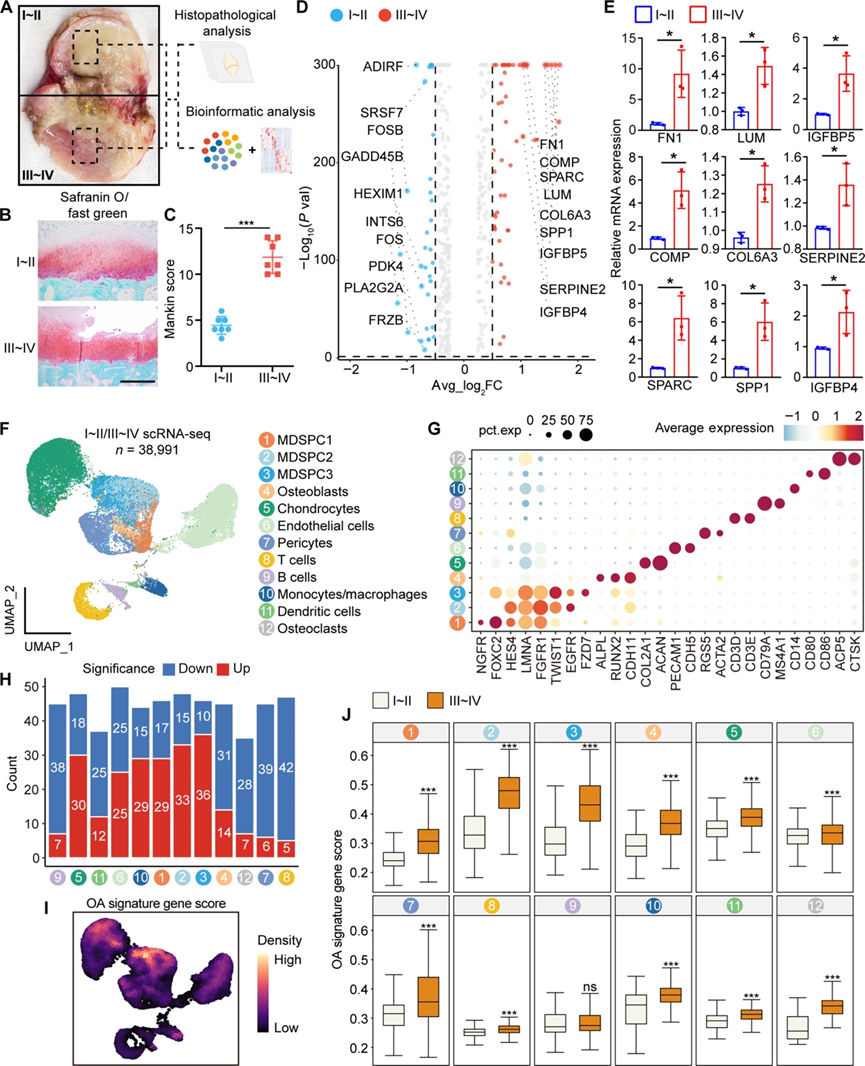
图1. 人类 OA 样本的 scRNA-seq 分析揭示了具有明显 OA 特征的细胞群。
(A) 用于后续组织病理学和生物信息学分析的人 OA 样本取样区域。(B) I~II 和 III~IV 侧组织的番红 O/固绿染色。(C) 基于番红 O/固绿染色的 I~II 和 III~IV 侧组织的 Mankin 评分。(D) I~II 和 III~IV 侧组织之间的整体差异基因表达。(E) 定量聚合酶链式反应结果显示 I~II 和 III~IV 侧组织之间代表性基因表达的差异。(F) UMAP可视化。(G) 点图显示每个聚类中标记基因的表达。(H) 条形图显示每个聚类中 I~II 和 III~IV 侧组织之间的 DEG 计数。(I) 密度图显示具有高 OA 特征基因得分的区域。(J) 箱线图显示每个聚类中 I~II 和 III~IV 侧组织之间的 OA 特征基因得分。
02
在 OA 进展过程中,致病性 MDSPC 中存在衰老亚群
为了进一步探索 MDSPC 亚群在 OA 进展中的致病作用,他们分析了三个 MDSPC 亚群的生物学特征(图 2A)。差异基因表达分析显示这些亚群之间存在显著差异(图 2B)。具体而言,MDSPC1 [增殖性 MDSPC (pro-MDSPC)] 表达干性基因KLF10和HES1;MDSPC2 [5'-核苷酸酶外阳性 (NT5E +)MSC] 表达NT5E和ENG;而 MDSPC3 [podoplanin 阳性 (PDPN+ )SSC] 表达PDPN和CADM1(图 2C)。对每个聚类中的 DEG 进行显示,pro-MDSPC 群体与细胞数量稳态、间充质发育和间充质细胞分化有关。 NT5E+ MSC 群体与内质网应激和对错误折叠蛋白质的反应有关,而 PDPN+ SSC 群体表现出与钙化、矿化和 ECM 降解相关的基因表达特征(图 2D)。
他们进一步使用 RNA 速度和基于分区的图形抽象分析研究了这些 MDSPC 亚群之间的关系。结果表明,NT5E+ MSC 和 PDPN+ SSC 亚群均源自 pro-MDSPC 群体并且相互连接(图 2E-F)。相关性分析显示,NT5E + MSC 与 PDPN+ SSC 亚群之间存在特别强的关系(图 2G )。沿着从 pro-MDSPC 到 NT5E + MSC 和 PDPN + SSC的 RNA 速率轨迹的基因表达谱显示,衰老相关基因(PAPPA、IGFBP6和SERPINE2)和成骨相关基因(PRRX1、COL6A3和COL5A2)在分化轨迹的终端高度表达(图 2H)。此外, CTNNB1、PPP1CA、HMGA1、IGFBP4、MMP14、MMP3等衰老相关基因在NT5E+ MSC和PDPN+ SSC亚群中均富集(图2I)。衰老基因集评分进一步证实这两个亚群均表现出强烈的衰老特征(图2J)。
值得注意的是,NT5E+ MSC 亚群的主要衰老特征是其炎症特征,而 PDPN+ SSC 亚群的主要特征是 ECM 降解和胶原代谢异常。这两个亚群也显示出骨化能力。PDPN+ SSC 群体中 TGF-β 和 WNT 信号通路的激活驱动了 ECM 重塑,而 NT5E+ MSC 中的白细胞介素 6 (IL-6) 信号传导促进了促炎反应并对 PDPN+ SSC 发挥调节作用。此外,PDPN+ SSC主要通过分泌型磷蛋白 1/骨桥蛋白 (SPP1) 的促成骨分泌信号影响 NT5E+ MSC。虽然功能存在差异,但 NT5E+ MSC 和 PDPN+ SSC 亚群之间的衰老评分没有显著差异(图 2J)。
在评估的标志物中,EGFR的表达范围与NT5E + MSC和PDPN + SSC亚群的表达范围重叠性最好(图2K)。因此,他们将这两个亚群统称为“EGFR +衰老MDSPC”(图2K)。OA样本III~IV侧的EGFR +衰老MDSPC表现出升高的衰老评分(图2L),并且显著上调经典衰老基因CDKN1A和CDKN2A的表达(图2M-N),证实EGFR+ MDSPC(即NT5E + MSC和PDPN + SSC亚群)在OA进展过程中经历衰老。
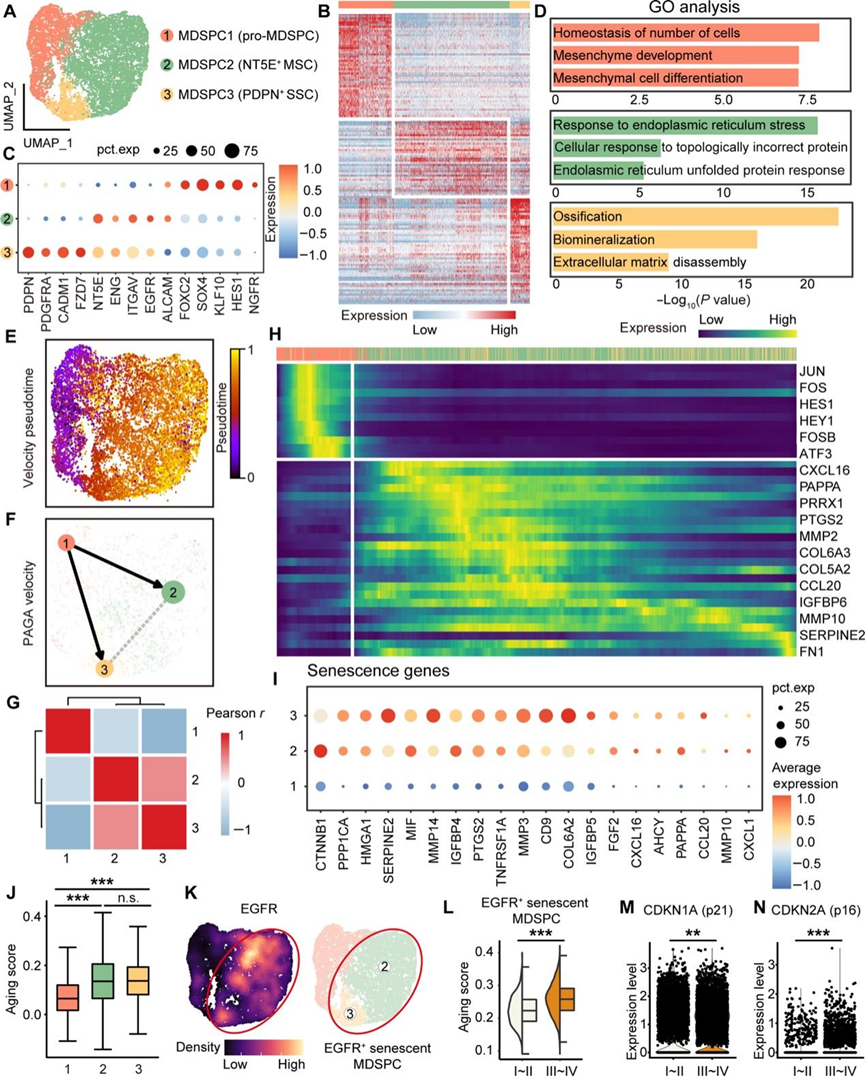
图2. OA患者I~II侧和III~IV侧组织中MDSPC聚类的异质性分析。
(A) UMAP可视化。(B) 热图显示每个 MDSPC 亚聚类中的差异基因表达。(C) 点图显示 MDSPC 每个亚聚类中标记基因的表达。(D) GO分析。(E) UMAP 上 RNA 速度映射的伪时间分析。(F) 基于分区的图形抽象 (PAGA) 分析显示 MDSPC 亚聚类之间的连通性。(G) MDSPC 亚聚类之间的相关性分析。(H) 热图显示伪时间轨迹上的差异基因表达。(I) 点图显示每个 MDSPC 子聚类中衰老基因的表达情况。(J) 箱线图显示每个 MDSPC 亚聚类的衰老评分。(K) 密度图显示EGFR基因的表达,UMAP 显示EGFR表达细胞。(L) 小提琴箱线图显示 EGFR +衰老 MDSPC 中 I~II 侧和 III~IV 侧组织之间的衰老评分。(M-N) CDKN1A和CDKN2A的表达分析。
03
EGFR+衰老的 MDSPC 在 OA 进展过程中主要存在于软骨下骨区域
虽然scRNA-seq 数据显示OA 患者的关节骨软骨组织中存在EGFR + MDSPC,但该亚群的衰老是否与关节软骨或软骨下骨的病理病变有关仍不清楚。因此,他们探索了健康个体和 OA 患者关节骨软骨组织的空间转录组分析(ST) 数据 (GSE254844)。OA 特征基因评分结果显示,关节骨软骨组织的深层区 (DZ),即关节软骨 DZ 与钙化软骨层相邻的区域,表现出最明显的 OA 相关病理特征(图 3A)。此外,DZ 表现出不同的衰老特征,表达多种衰老相关基因(图3B-D)。值得注意的是,只有在 DZ 中,OA 患者的衰老评分高于健康个体(图3E)。随后分析发现EGFR基因在关节骨软骨组织的关节面、浅层、中层及DZ区均有表达(图3F),但OA患者EGFR表达增高仅见于DZ区(图3G)。多重免疫荧光染色进一步显示,在III~IV侧组织中STB周围有更高的EGFR+ MDSPC丰度,且其衰老表型更为明显,以p16和p21的表达增高为特征(图3H-J)。这些结果表明,关节软骨下骨是OA进展过程中病理和衰老特征最为突出的区域,EGFR+ MDSPC在该区域发生衰老。
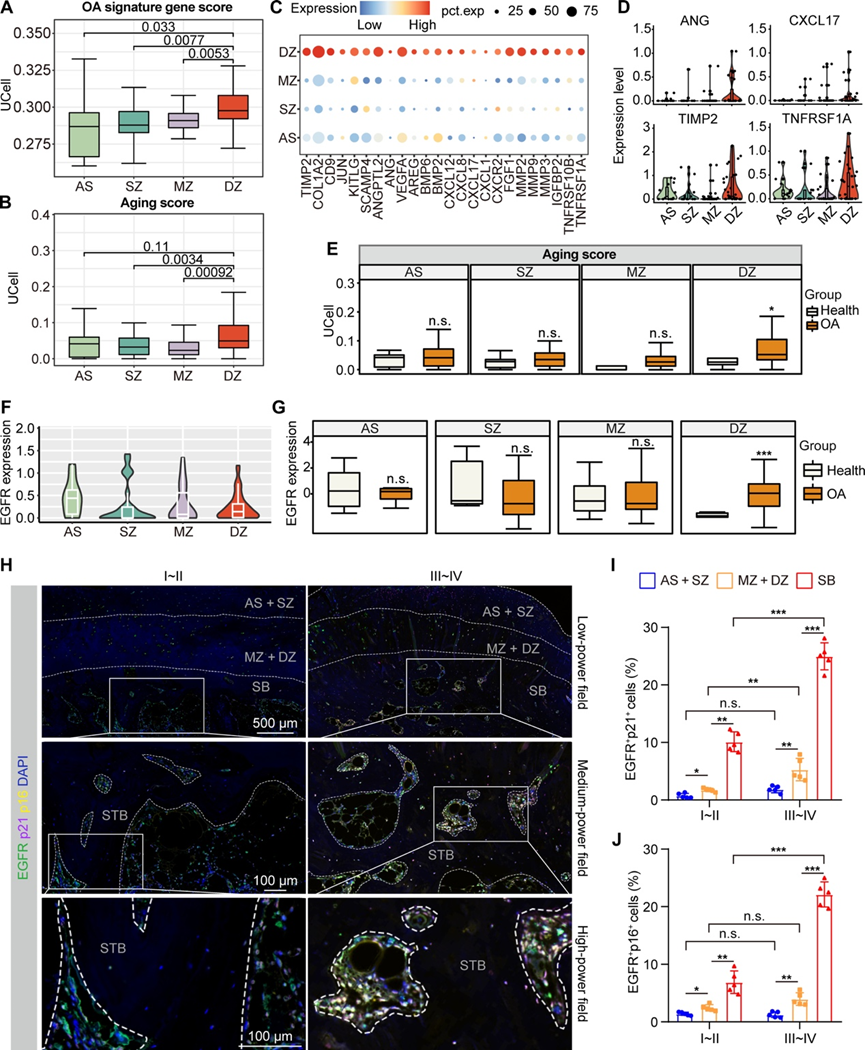
图3. OA患者I~II侧和III~IV侧组织空间转录组分析。
(A) 关节面 (AS)、浅表区 (SZ)、中层 (MZ) 和深层 (DZ) 组的 OA 特征基因评分。(B) AS、SZ、MZ 和 DZ 组的衰老评分。(C) 点图显示 AS、SZ、MZ 和 DZ 组中衰老基因的表达。(D) 小提琴图显示 AS、SZ、MZ 和 DZ 组中代表性衰老基因的表达。(E) 箱线图显示 AS、SZ、MZ 和 DZ 组中健康人和 OA 患者的衰老评分。(F) 小提琴图显示AS、SZ、MZ 和 DZ 组中EGFR基因的表达。(G) 箱线图显示AS、SZ、MZ 和 DZ 组中健康人群与 OA 患者之间EGFR基因表达的情况。(H) 多重免疫荧光染色显示 OA 患者 I~II 侧和 III~IV 侧软骨下骨组织中 p21、p16 和 EGFR 的共同表达。(I) 从随机选择的五个低倍视野进行半定量分析。(J) 从随机选择的五个低倍视野进行半定量分析。
04
EGFR+衰老MDSPC成骨能力增强,自我更新能力下降
为了阐明EGFR +衰老MDSPC在OA进展中的作用,他们通过生物信息学分析和细胞功能实验来检查I~II侧组织和III~IV侧组织中EGFR+ MDSPC的生物学差异。差异基因表达分析显示,III~IV侧组织中的EGFR+衰老MDSPC高表达成骨相关基因,例如COL5A2、BGN和HTRA1(图4A-B)和衰老相关基因,包括IGFBP4、TIMP1和PTGES(图4A-C)。GO分析和基因集富集分析进一步表明,III~IV侧组织中的EGFR+衰老MDSPC表现出衰老表型和更大的骨化倾向(图4D-E)。RUNX2和SPP1的免疫荧光染色证实,III~IV侧组织中软骨下小梁周围的EGFR+ MDSPC具有增强的成骨表型(图4F-G)。
然后,他们根据先前发表的方案(略作修改)对 I~II 侧和 III~IV 侧 OA 组织的软骨下骨组织中的 MDSPC(acMDSPC)进行贴壁培养(47)。流式细胞分析显示,I~II 侧和 III~IV 侧 acMDSPC 细胞群均表达三种 MDSPC 亚群的标志物 [PDPN、NT5E 和活化白细胞粘附分子 (ALCAM)],以及衰老 MDSPC 标志物 EGFR。EGFR +细胞群包括 NT5E+ PDPN−和 NT5E+ PDPN+亚群,这表明 acMDSPC 保留了组织驻留 MDSPC 的关键特征。值得注意的是,在III~IV侧组织中观察到EGFR+ NT5E+ PDPN+亚群比例显著增加(图S5C),提示该亚群可能在晚期OA中起主要的致病作用。因此,从I~II侧和III~IV侧OA患者软骨下骨组织中分离的acMDSPC用于下游功能检测。β-半乳糖苷酶染色显示III~IV侧组织的EGFR+ acMDSPC具有更明显的衰老表型(图4H)。在成骨实验中,I~II侧组织的EGFR+ acMDSPC表现出成骨分化和矿化能力,而III~IV侧组织的EGFR+ acMDSPC成骨能力明显增强(图4I)。此外,克隆形成单位成纤维细胞 (CFU-F) 测定表明,来自 I~II 侧组织的EGFR+ acMDSPC 具有强大的自我更新能力,并能有效调节细胞数量以维持体内平衡。相反,来自 III~IV 侧组织的 EGFR+ acMDSPC 表现出有限的自我更新能力,未能形成可观的细胞克隆(图 4J)。鉴于进行性 OA 的软骨下骨病理特征包括软骨下骨硬化,这些结果提示 EGFR+衰老 MDSPC 通过过度成骨作用促进 OA 进展。
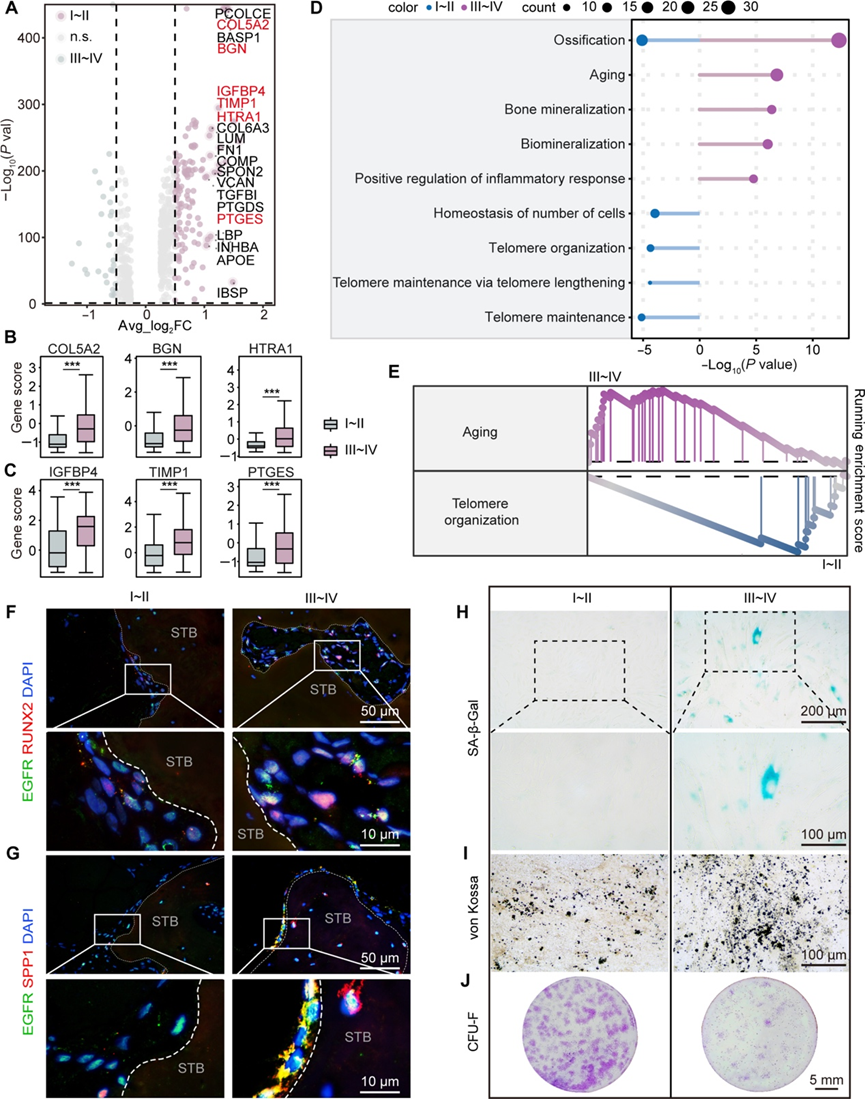
图4. OA患者I~II期和III~IV期侧组织中EGFR+衰老MDSPC的生物学特性。
(A) EGFR+衰老MDSPC中I~II和III~IV侧组织之间的差异表达基因。(B) 代表性成骨基因的表达。(C) 箱线图显示EGFR+衰老MDSPC中I~II和III~IV侧组织之间代表性衰老基因的表达。(D) GO分析。(E) 基因集富集分析。(F) 免疫荧光染色显示 OA 患者的 I~II 和 III~IV 侧软骨下骨组织中 RUNX2 与 EGFR 共同表达。(G) 免疫荧光染色显示 OA 患者的 I~II 和 III~IV 侧软骨下骨组织中 SPP1 与 EGFR 共同表达。(H) 对来自 I~II 和 III~IV 侧组织的 EGFR + acMDSPC进行 β-半乳糖苷酶染色。(I) 对来自 I~II 和 III~IV 侧组织的 EGFR+ acMDSPC进行von Kossa染色。(J) 结晶紫染色。
05
在骨关节炎进展过程中,衰老的骨骼单元主要位于与骨小梁相邻的软骨下骨腔内
干细胞位于称为“微环境”的特定微环境中,该微环境维持和调节干细胞的生物学特性。干细胞及其微环境共同构成再生单位,在组织发育、稳态维持、再生和衰老中发挥至关重要的作用。为了进一步研究EGFR+衰老MDSPC微环境的细胞组成,他们进行了细胞间通讯分析,特别关注EGFR+衰老MDSPC。基于EGFR基因的表达和高衰老评分区(图5A-B),将12个细胞亚群重新分类,得到11个细胞亚群(包括EGFR+衰老MDSPC)(图5C)。随后他们分析了每个亚群的传入和传出相互作用信号。结果表明,EGFR+衰老MDSPC表现出相对较强的传入相互作用信号(图5D)。
为了探索作用于EGFR +衰老MDSPC的生态位信号,他们分析了每个亚群的整体传入信号模式,发现EGFR+衰老MDSPC的主要传入信号是表皮生长因子(EGF)信号通路(图5E-F)。信号网络分析进一步表明,EGFR+衰老MDSPC接收来自多种细胞类型的EGF信号,包括OB、软骨细胞、EC、MDSPC1亚聚类、DC和单核细胞/巨噬细胞(图5G)。值得注意的是,通路富集定量表明单核细胞/巨噬细胞是EGF通路激活的主要细胞贡献者(图5G-H)。该分泌信号轴将单核细胞/巨噬细胞群体确定为通过微环境信号调节调节EGFR+衰老MDSPC的关键生态位成分。EGF 通路的进一步受体-配体相互作用分析表明,“EREG-EGFR”的相互作用信号强度大于“肝素结合 EGF 样生长因子 (HBEGF)-EGFR”,表明“EREG-EGFR”代表 EGFR+ 衰老 MDSPC 的主要受体-配体相互作用模式 (图 5I)。接下来他们分析了该信号轴中受体 EGFR 和配体 EREG 的主要细胞来源。信号通路网络和基因表达数据显示,EGFR 在 EGFR+衰老 MDSPC中表达,而EREG在单核细胞/巨噬细胞聚类中表达,表明单核细胞/巨噬细胞衍生的 EREG 特异性靶向 EGFR +衰老 MDSPC(图 5J-K)。
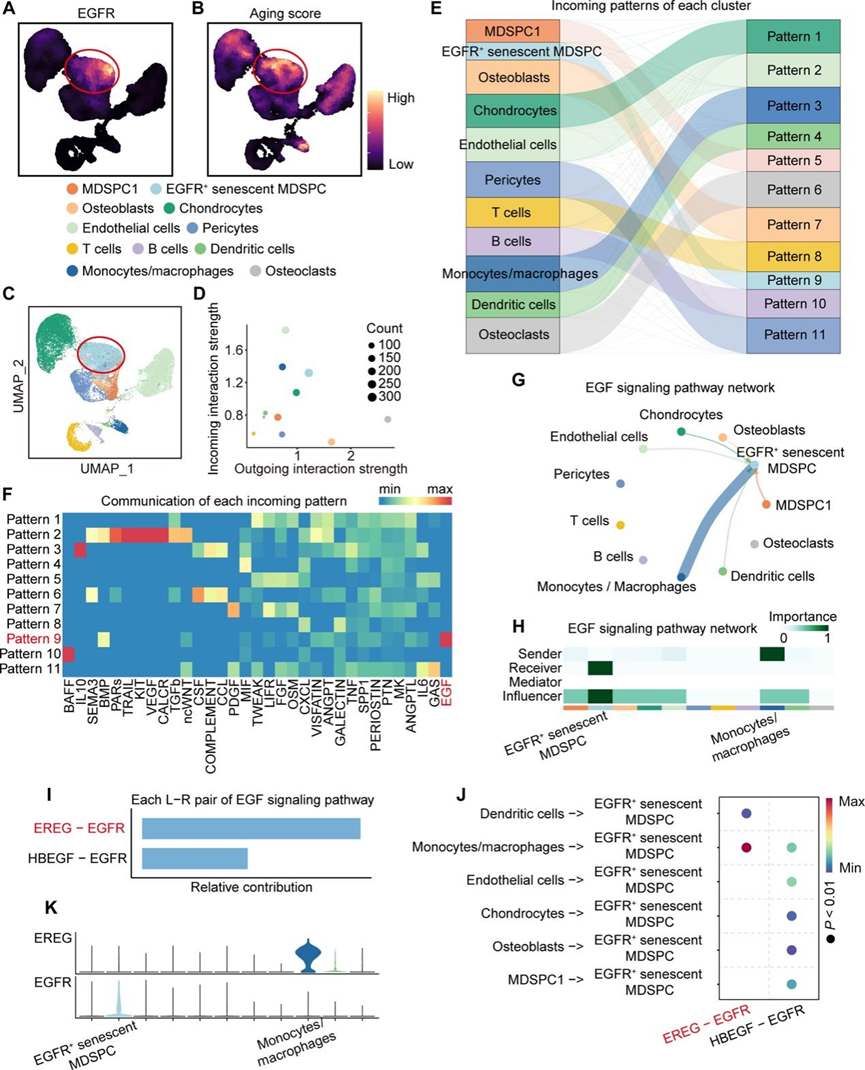
图5. 以 EGFR+衰老 MDSPC 为重点的细胞通讯分析。
(A) 密度图显示EGFR基因的表达。(B) 密度图显示衰老评分。密度图的颜色代表评分水平。(C) 来自I~II期和III~IV期侧组织的38991个细胞的UMAP可视化。(D) 每个聚类的传入和传出相互作用强度。(E) 桑基图显示每个聚类的传入模式。(F) 热图显示每个传入模式的通信。(G) 网络图显示所有聚类之间的EGF信号通路。(H) 热图显示所有聚类之间的EGF信号通路。(I) 条形图显示EGF信号通路中每对受体-配体的贡献。(J) 每对EGF信号受体-配体的发送者和接收者。(K) 每个聚类中的EREG和EGFR基因表达。
06
细胞聚类的异质性分析
鉴于单核细胞/巨噬细胞衍生的 EREG 在调节 EGFR+衰老 MDSPC中的特殊作用,他们进一步剖析了单核细胞/巨噬细胞亚群的细胞异质性。单核细胞/巨噬细胞聚类重新分组为四个不同的亚聚类:巨噬细胞 1 (Ma1)、巨噬细胞 2 (Ma2)、树突状细胞 (DC) 和 OC(图 6A),每个聚类的 DEG 用于功能注释(图 6B)。Ma1 的特征是表达CD68、CD14和TLR2;Ma2 表达C1QA、FGFR1和FGL2;树突状细胞表达CD86、CD80和CCR7;而 OC 表达TRAP1、CTSK和TNFRSF11A(图 6C-D)。 DEGs 的 GO 分析表明,Ma1 参与慢性炎症反应并促进炎症细胞因子的产生,例如干扰素-γ和肿瘤坏死因子;Ma2 主要通过抑制白细胞活化和维持髓系细胞稳态在抗炎过程中发挥作用;DC 表现出强大的主要组织相容性复合物 II 类活性和抗原呈递能力;而 OC 参与骨吸收(图 6E)。值得注意的是,Ma1 表现出与衰老相关的生物学特征,并特异性表达与衰老相关的基因(图 6E-F)。衰老评分分析显示高衰老评分区域与 Ma1 聚类重叠,后者也特异性表达EREG(图 6G)。因此,他们将 Ma1 巨噬细胞定义为 EREG +衰老巨噬细胞。EREG+巨噬细胞的衰老特征在 I~II 侧和 III~IV 侧有所不同,其中 III~IV 侧表现出经典衰老基因CDKN1A (p21) 的表达明显较高,但是CDKN2A (p16) 的表达没有显著差异。
他们随后验证了OA患者软骨下骨组织中存在由EGFR+ MDSPC和EREG +巨噬细胞组成的衰老骨骼单元。多重免疫荧光染色显示,与I~II侧组织相比,III~IV侧组织中骨小梁附近的EGFR+衰老MDSPC和EREG+衰老巨噬细胞的聚集显著增加(图6H-I)。这些细胞聚集体在晚期OA的软骨下骨区域内形成了独特的“衰老骨骼单元”,可能有助于骨关节炎软骨下骨的病理性骨重塑。
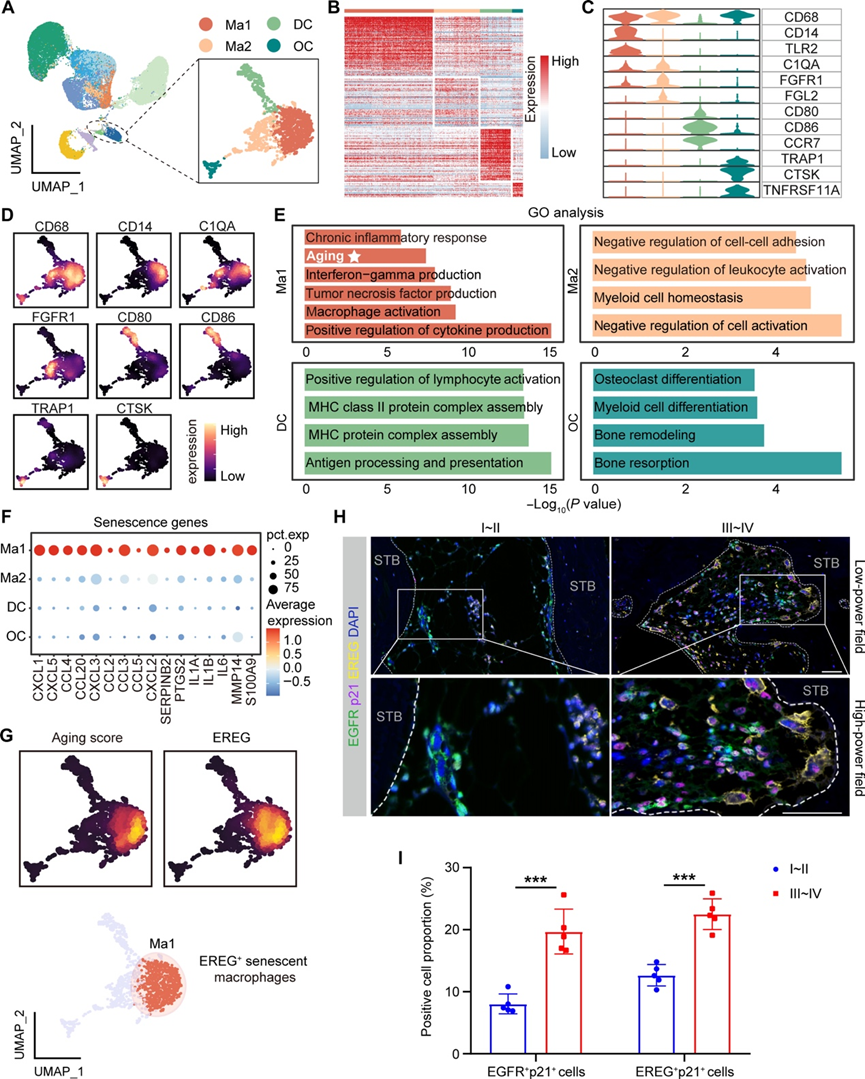
图6. OA患者I~II侧和III~IV侧组织中单核细胞/巨噬细胞聚类异质性分析。
(A)UMAP可视化。(B) 热图显示每个亚聚类中的差异基因表达。热图的颜色代表基因表达水平。(C) 小提琴图显示每个亚聚类中标记基因的表达。(D) 密度图显示每个亚聚类中代表性标记基因的表达。(E) GO分析。(F) 点图显示每个亚聚类中衰老基因的表达。(G) 密度图显示衰老评分和EREG基因表达,UMAP 显示 EREG 表达的衰老细胞(EREG+衰老巨噬细胞)。密度图的颜色代表基因表达水平。(H) 多重免疫荧光染色显示 OA 患者 I~II 和 III~IV 侧软骨下骨组织中 EGFR、p21和 EREG的共同表达。(I) 从五个随机选择的低倍视野进行半定量分析。
07
EREG 是一种 SASP 成分,与 OA 患者的年龄以及 OA 进展过程中的成骨能力有关
为了充分阐明EREG与OA进展之间的关系,他们对OA患者I~II侧和III~IV侧关节骨软骨组织进行了转录组分析(RNA-seq)。差异基因表达分析显示,虽然OA患者之间存在一些个体差异,但I~II侧与III~IV侧组织之间整体基因表达仍存在明显差异(图7A)。III-IV侧组织的DEG与衰老基因列表的重叠基因包括EREG、MMP2、MMP9和PLAU(图7B),其中EREG的表达量明显高于其他基因(图7C),表明EREG既是衰老基因,也是OA进展的特征基因。随后,收集无其他疾病的OA患者外周血清样本,按不同年龄和不同的Kellgren和Lawrence分级分层,采用酶联免疫吸附试验(ELISA)对EREG蛋白进行定量分析。ELISA结果显示,血清中EREG水平较高与OA患者的年龄呈正相关,且OA病情较重患者血清EREG浓度升高(图7D)。GO分析显示,OA样本的III~IV侧组织参与了与骨化、胶原纤维组化和组织重塑相关的生物学过程(图7E)。蛋白质-蛋白质相互作用(PPI)网络分析显示,EREG通过EGFR和SMAD3通路调控成骨分化(图7F)。这些结果提示EREG是OA进展过程中与骨化相关的SASP成分之一。
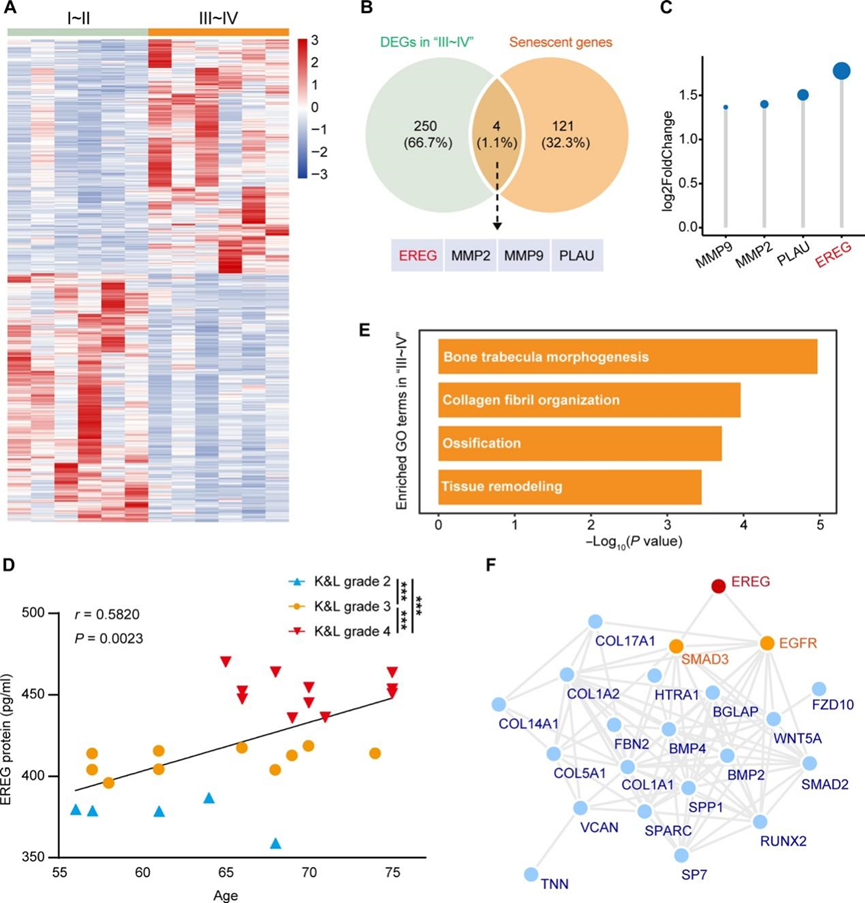
图7. OA患者I~II侧和III~IV侧组织的RNA-seq数据的分析和验证。
(A) 热图显示I~II侧和III~IV侧组织之间的差异表达基因。(B) 维恩图显示III~IV侧组织上调的DEG与衰老基因共同的基因。(C) III~IV侧组织上调的DEG与衰老基因共同的基因。(D) 血清中EREG的含量。(E)GO分析。(F) 蛋白质-蛋白质相互作用(PPI)网络图显示EREG与OA相关骨化基因的相互作用。
08
抑制EREG可阻止 EGFR+MDSPC衰老,从而缓解小鼠 OA 进展
为了进一步研究 EREG 干预能否在体内延缓OA进展,他们在创伤性骨关节炎 (PTOA) 诱导后 2 周(软骨下骨微损伤期),通过关节内注射腺相关病毒 5 (AAV5) 介导的EREG敲低。所有 AAV 载体均能有效转导软骨下骨组织,在关节软骨中观察到的转导极少。此外,局部递送EREG敲低的 AAV5 对小鼠肝脏或脑组织无不良影响。EGFR、p21 和 p-EGFR 的多重免疫荧光染色表明,在 OA 进展过程中,关节软骨和软骨下骨 EGFR+细胞均出现细胞衰老。然而,关节内注射 AAV5- EREG敲低选择性地抑制了软骨下骨中细胞衰老和 EGFR+细胞的磷酸化激活,而不影响关节软骨中的 EGFR+p21+p-EGFR+细胞。这表明关节内 AAV5-EREG抑制特异性地靶向了软骨下骨中 EGFR+衰老的 MDSP。随后,多重免疫荧光分析显示,AAV5 介导的EREG敲低显著降低了软骨下小梁附近EGFR+ p21+和 EREG+p21+细胞的比例(图 8A-C)。EGFR、p21 和 SPP1 的共染色进一步表明,AAV5-EREG干预显著减弱了 EGFR+衰老 MDSPC的成骨分化能力。Micro-CT 和组织病理学分析显示,AAV5-EREG抑制显著降低了内侧软骨下 BV/TV 和 SBP 厚度(图 8D-F),改善了软骨退变(图 8G-H),减少了骨赘形成(图 8I),雄性和雌性 OA 小鼠之间没有观察到明显的性别差异。此外,行为学分析显示,AAV5介导的EREG抑制显著延长了创伤后骨关节炎(PTOA)小鼠后爪的热反应潜伏期,并提高了机械缩足阈值,表明OA相关疼痛得到有效缓解(图8J-K)。总之,这些结果表明,关节内AAV5介导的EREG抑制可减轻软骨下骨中EGFR+ MDSPC的衰老和过度成骨,从而部分改善软骨下骨重塑并减缓OA进展
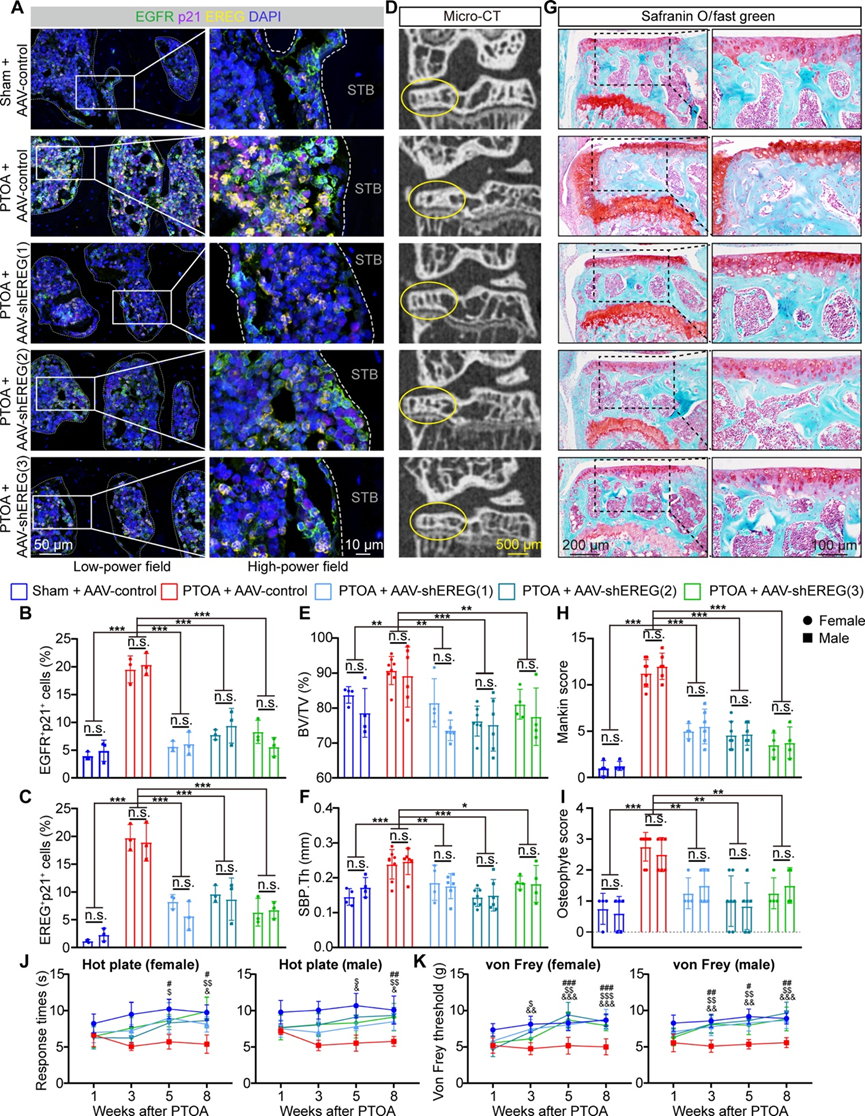
图8. 局部EREG抑制对EGFR、衰老MDSPC和骨软骨损伤的治疗评价。
(A) 多重免疫荧光染色显示 8 周时不同组别的 PTOA 小鼠关节软骨下骨组织中 EGFR、p21 和 EREG 的共同表达。(B-C) 从三个随机选择的低倍视野进行半定量分析,显示软骨下骨中EGFR+ p21+细胞和EREG+p21+ 细胞的细胞比例。(D) 每组的代表性微型计算机断层扫描 (micro-CT) 图像。(E) 每组的骨体积分数 (BV/TV)。(F) 每组的软骨下骨板 (SBP) 厚度 (SBP.Th)。(G) 8 周时每组的番红 O/固绿染色。(H) 基于番红 O/固绿染色的每组 Mankin 评分。(I) 通过番红O/固绿染色确定各组的骨赘评分。(J) PTOA建模后1、3、5和8周进行的热板测试,显示各组小鼠的疼痛反应时间。(K) PTOA建模后1、3、5和8周进行的von Frey测试。
+ + + + + + + + + + +
结 论
本研究探索了MDSPC的衰老在 OA 进展中的作用,旨在寻找潜在的治疗靶点。对人类和小鼠 OA 样本的组织病理学评估和生物信息学分析表明,EGFR+ MDSPC 和 EREG+巨噬细胞在骨关节炎关节软骨下骨中构成了一个衰老的骨骼单元。体外和体内实验表明,EREG 促进 EGFR+ MDSPC的衰老和过度成骨。此外,通过腺相关病毒介导的EREG基因敲低或敲除,干扰小鼠体内EREG的表达,显著抑制了软骨下骨中EGFR+ MDSPC的衰老,并减轻了OA小鼠的病理性硬化和疼痛。本项研究结果表明,软骨下骨中MDSPC的衰老是驱动OA进展的关键事件,这为开发创新的OA治疗策略提供了宝贵的参考点。
+ + + + +



 English
English


