文献解读|Cell(42.5):蛋白质限制重塑小鼠衰老过程中多器官的蛋白质组图谱
✦ +
+
论文ID
原名:Protein restriction reprograms the multi-organ proteomic landscape of mouse aging
译名:蛋白质限制重塑小鼠衰老过程中多器官的蛋白质组图谱
期刊:Cell
影响因子:42.5
发表时间:2025.10.24
DOI号:10.1016/j.cell.2025.10.004.
背 景
衰老是癌症和神经退行性疾病等多种疾病的主要风险因素。2013年,研究人员提出了分子、细胞和系统层面的9项衰老标志,2023年又将其扩展至12项。这些新增标志凸显了衰老过程的复杂性,并表明仍有大量领域有待探索和补充。为了延长寿命,人们提出了多种饮食干预措施,蛋白质限制(PR)是一种有效且实用的方法。随机临床试验表明,PR 可以改善代谢健康,降低血糖和胰岛素水平,提高胰岛素敏感性,并促进脂肪减少。PR延缓衰老的潜在机制包括通过系统性调节胰岛素样生长因子 1(Igf1,小鼠)信号通路、雷帕霉素靶蛋白激酶 (mTOR) 通路、胰岛素水平以及成纤维细胞生长因子 21 (Fgf21) 水平。然而,其益处似乎与年龄相关,对 ≤65 岁的人群具有保护作用,但对老年人则无此作用,而且可能具有器官特异性,因此在更广泛地实施之前,需要确定最佳时机和组织特异性反应。
实验设计
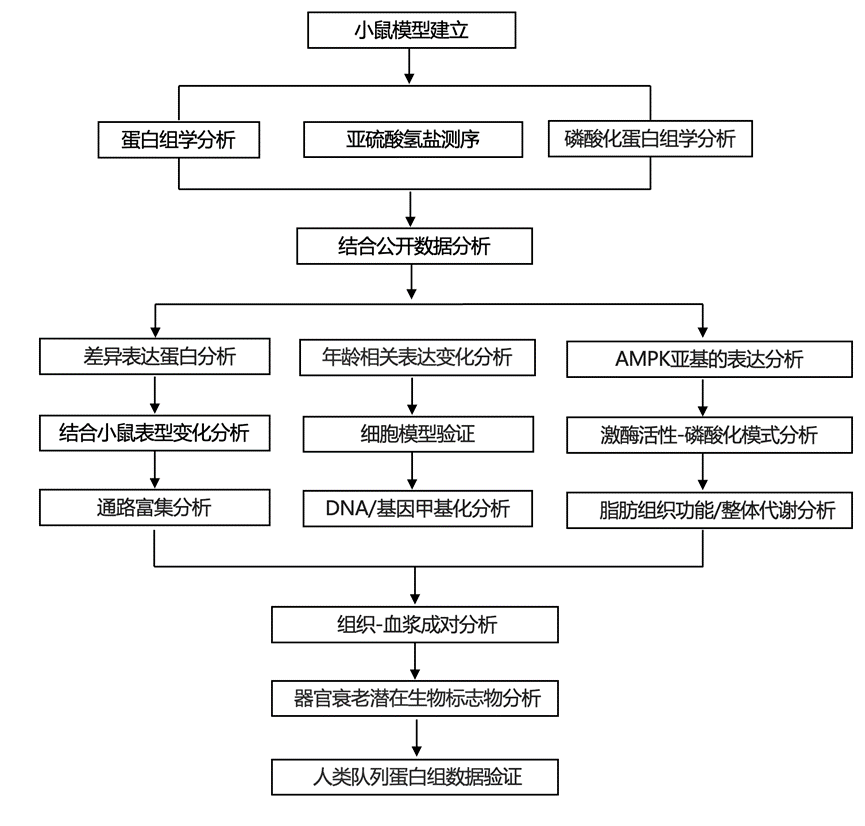
结 果
01
构建小鼠衰老和PR的多器官蛋白质组图谱
为了研究衰老,研究团队在8个时间点(1、4、7、10、13、17、21和24个月)收集了41个小鼠器官(图1A),每个时间点设置4个重复(图1B)。他们对另一组小鼠进行了为期3个月的干预,干预分别在三个不同的年龄阶段(干预开始于7、12或20个月):采用三种不同的蛋白质供能比(千卡百分比):高蛋白(HP)饮食(40.0%蛋白质、16.5%脂肪和43.5%碳水化合物)、中蛋白(MP)饮食(20.7%蛋白质、16.5%脂肪和62.8%碳水化合物)和低蛋白(LP)饮食(5.0%蛋白质、16.5%脂肪和78.5%碳水化合物)。干预前,所有小鼠均饲喂MP饮食。三个月后,收集组织样本进行分析(图 1C)。构建了一个包含 156168 个肽前体(来自 13042 个蛋白质)的全小鼠光谱库,其深度超过了之前的数据集,用于后续的 DIA-MS 数据分析(图1B)。一些器官,如十二指肠 (DDN)、胆囊 (GB)、食管 (ESO) 和精囊 (SMV) 的 CV 值略高,表明这些器官的异质性更大。在衰老和饮食干预期间,他们对 2565 个小鼠组织样本中的 11000 多种蛋白质进行了定量分析(图 1B-C)。 t分布随机邻域嵌入(t -SNE)分析表明不同器官之间存在高度异质性,其中脑区和免疫器官形成了两个不同的聚类,这与之前的观察结果一致。晶状体和下颌腺在全蛋白质组水平上随年龄显著变化,表明它们在衰老过程中发生了明显改变。免疫、生殖和代谢器官在衰老过程中差异表达蛋白(DEP)数量最多,其中淋巴结表现出区域特异性变化。例如,腹股沟淋巴结(ILN)、腘窝淋巴结(PLN)和下颌淋巴结(MLN)在衰老相关DEP中分别排名第1、第3和第10位。
除老年雄性小鼠外(图 1D),MP 和 HP 饮食均使各组小鼠的体重略有增加。相反,LP 饮食降低了小鼠的体重,这与之前的研究结果一致,虽然在雌性和老年雄性小鼠中这种降低不太明显(图 1D)。LP 饮食增加了雄性小鼠的食物摄入量,这归因于“蛋白质杠杆效应”,而雌性小鼠受到的影响较小。组织学分析显示,LP 饮食减轻了 HP 饮食诱导的脂肪组织变化,包括白色脂肪细胞增大和棕色脂肪组织形态改变(脂滴增大,多房性脂肪细胞减少)(图 1E),表明代谢健康状况得到改善。衰老相关 β-半乳糖苷酶 (SA-β-gal) 染色显示,PR 可以减轻老年小鼠和 HP 饮食喂养小鼠肾脏中衰老细胞的积累(图 1E)。然而,也观察到了对肝脏的潜在不良影响。总体而言,膳食蛋白质干预引起的体重和食物摄入量的变化与之前的研究结果一致,雌性和老年小鼠的敏感性降低。尽管存在一些肝脏风险,但蛋白质储备仍对多种器官的健康产生广泛益处。
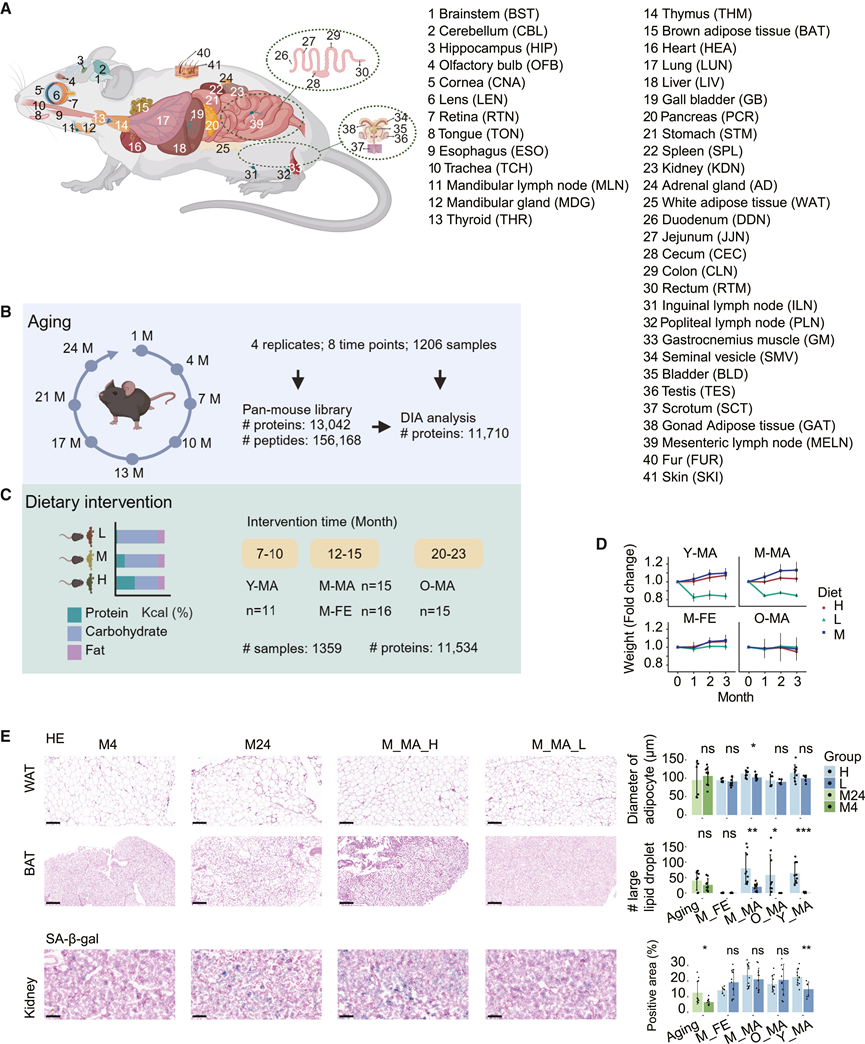
图1. 研究设计及PR对衰老的影响。
(A) 四十一种器官类型。(B) 衰老过程中的时间点和蛋白质组学工作流程。(C) 膳食分组。(D)饮食引起的体重变化。 (E) 代表性的H&E染色(白色脂肪组织/棕色脂肪组织)和SA-β-半乳糖苷酶染色(肾脏)图像。
02
PR逆转了衰老过程
他们通过分析在多个器官(n ≥ 5)中表现出显著变化的蛋白质,鉴定出普遍表达的衰老相关蛋白(图S2A)。通路分析揭示了与多个衰老标志相关的变化。例如,肽代谢过程、蛋白质分解代谢的调控以及蛋白水解与蛋白质稳态的丧失相关。细胞外基质的组织与细胞间通讯相关,而小分子分解代谢过程和含核碱基的小分子代谢与营养感知相关(图S2B)。基于衰老相关DEP对每个器官进行通路富集分析也表明,这三个衰老标志以及慢性炎症在 28-32 个器官中广泛存在。相反,表观遗传改变、端粒缩短和巨自噬功能障碍仅在2至10个器官中富集。共有36种蛋白质在超过9个器官中持续发生改变(图2A),包括免疫球蛋白链,例如Igh-3(n =24)、Igkc(n =23)和Ighm(n =22),以及丝氨酸蛋白酶抑制剂,例如Serpina1e(n =16)和Serpinh1(n =14)(图2B)。先前的研究表明,衰老大鼠的五个器官中Igkc转录本均上调,这凸显了免疫球蛋白在衰老过程中保守的作用。值得注意的是,这些变化最早在大鼠1个月龄时就已出现,表明衰老的发生时间比之前认为的要早(图2B)。
接下来,他们检测了PR是否能够逆转这36种蛋白质的表达趋势,在衰老过程中表达下调的36种蛋白质中,有22种可以通过PR在相应的器官中上调(图S2C),例如热休克蛋白HSP90-β(Hsp90ab1)和90 kDa热休克蛋白ATPase激活因子同源物1(Ahsa1),这些蛋白质在衰老过程中在多个脑区和其他器官中表达下调(图2 C-D,图S2D)。此外,他们还观察到小鼠不同脑区中Ahsa1的转录水平随年龄增长而降低。Ahsa1和Hsp90ab1均能调节Hsp90分子伴侣的活性,从而影响蛋白质折叠和细胞蛋白质稳态。鉴于Hsp90ab1和Ahsa1是两种主要的PR拯救型衰老相关蛋白,且二者可能存在功能重叠,在人星形胶质细胞系SVG p12中构建了Hsp90ab1和Ahsa1敲除(KO)细胞系(图S2 E)。Hsp90ab1-KO细胞的DEP数量多于Ahsa1-KO细胞,且34%的Ahsa1-KO DEP与Hsp90ab1-KO DEP重叠(图S2 F)。通路分析显示,溶酶体相关通路在Hsp90ab1-KO细胞中异常最为显著,而Ahsa1-KO细胞则表现出中间丝组织紊乱(图S2 G)。两种KO细胞系的增殖速率均降低(图S2 H)。值得注意的是,Hsp90ab1-KO(而非Ahsa1-KO)细胞表现出衰老(图S2 I-J)、细胞凋亡(图S2 K-L)以及细胞周期失调(图S2 M-N)的增加。这些结果表明,与Ahsa1相比,PR介导的Hsp90ab1调控发挥了更广泛的衰老相关作用,尽管两者可能都有助于减轻星形胶质细胞的衰老相关应激。
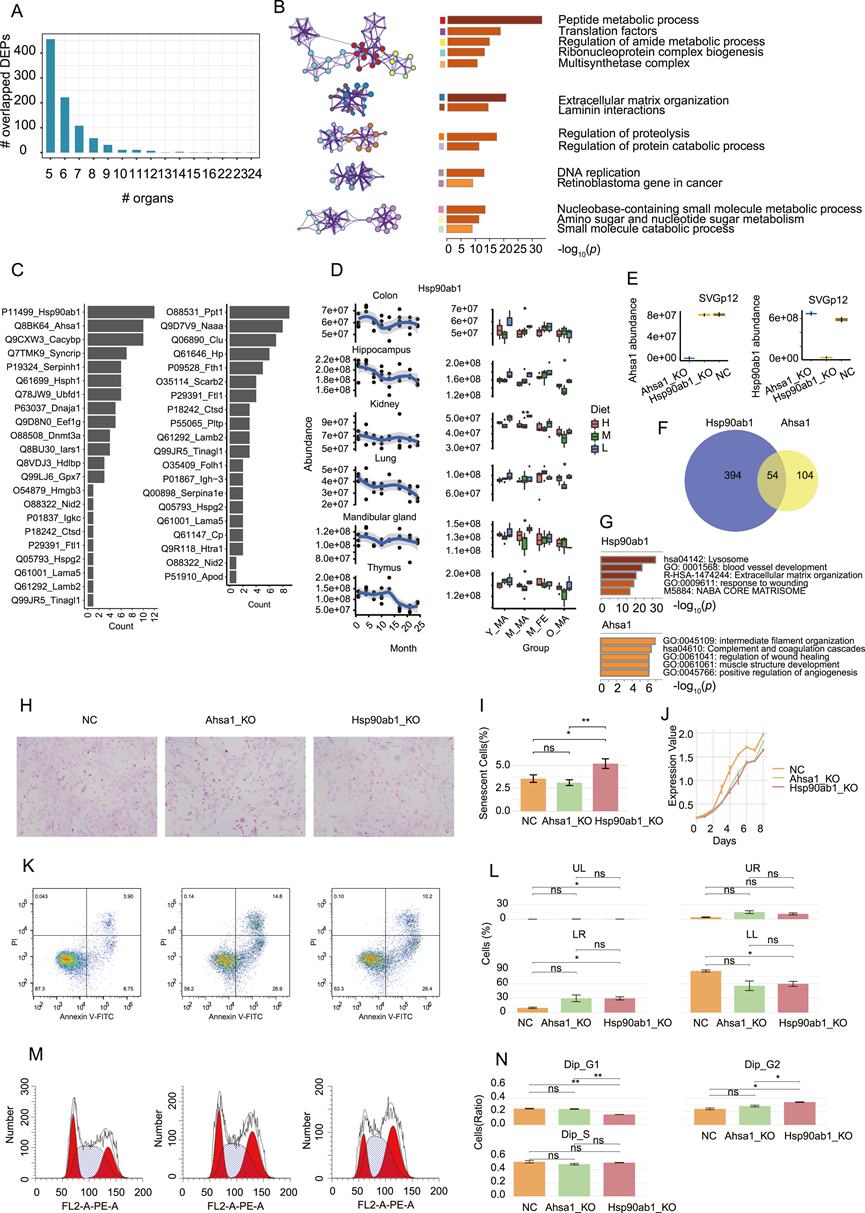
图S2. SVG p12中核心老化差异表达蛋白(DEP)及Hsp90ab1和Ahsa1敲低情况。
(A) 不同器官间重叠的DEP数量。(B) 利用 Metascape 对在五个以上器官中差异表达的蛋白质进行通路分析。(C) 蛋白质分布。(D) 衰老过程中 Hsp90ab1 的表达趋势和PR。(E) Ahsa1(左)和 Hsp90ab1(右)在 Ahsa1-KO、Hsp90ab1-KO 和 NC SVGp12 细胞中的丰度。(F) Hsp90ab1-KO SVG p12 细胞与 NC SVG p12 细胞(蓝色)和 Ahsa1-KO SVG p12 细胞与 NC SVG p12 细胞(黄色)的重叠 DEP。(G) 基于 Hsp90ab1-Ko DEP 和 Ahsa1-Ko DEP 的通路富集。(H) NC、Ahsa1-KO 和 Hsp90ab1-KO SVG p12 细胞的代表性 SA-β-gal 染色结果。(I) 三组细胞中 SA-β-gal 染色阳性面积的定量结果。(J) 通过细胞计数试剂盒-8(CCK8)实验测定 NC、Ahsa1-KO 和 Hsp90ab1-KO SVG p12 细胞的细胞增殖率。(K) Ahsa1-KO、Hsp90ab1-KO 或 NC-KO SVG p12 细胞的凋亡。(L)细胞死亡情况。(M)流式细胞分析。(N) G1、G2 和 S 期细胞比例的定量结果。
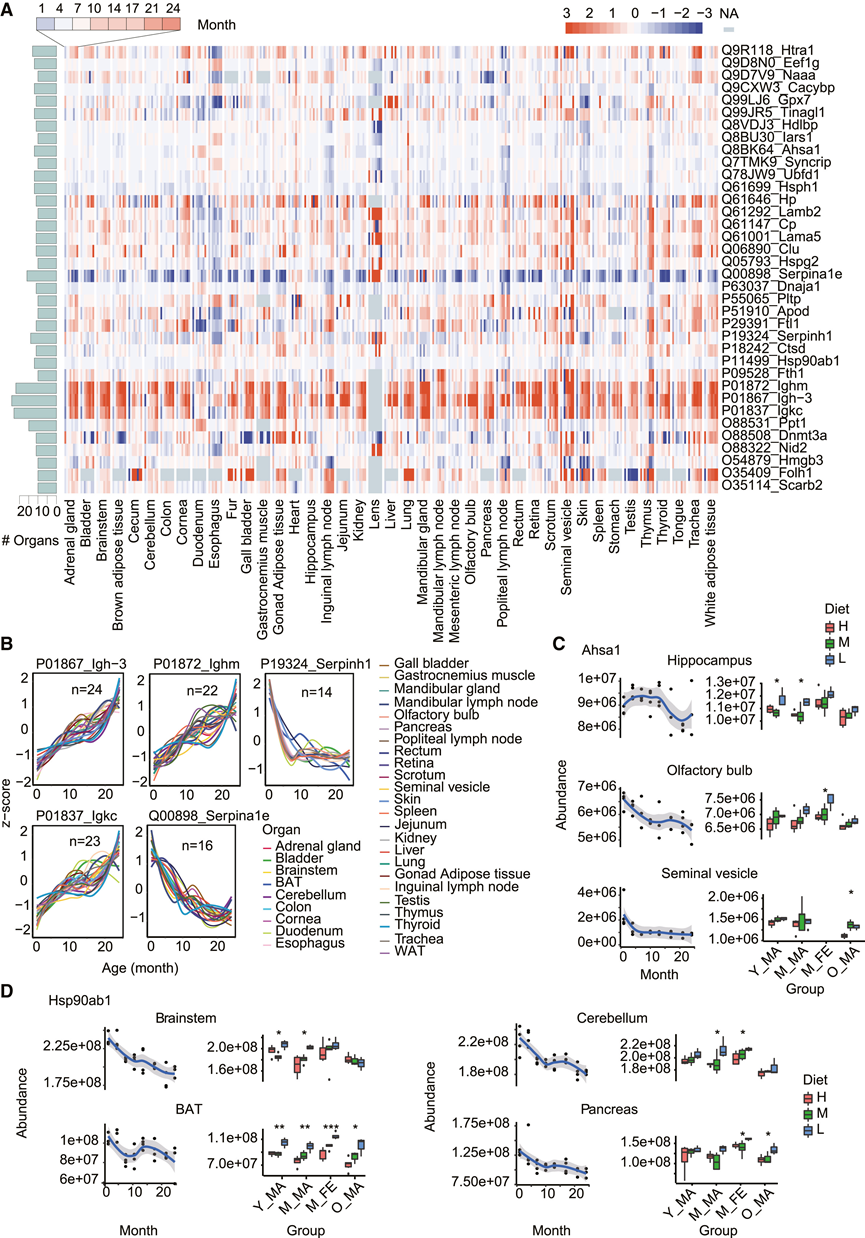
图2. 衰老和PR过程中关键蛋白的组织特异性表达。
(A) 36种蛋白质在≥9个器官中的年龄相关表达变化。(B) 按组织划分的 Igh-3、Igkc、Ighm、Serpinh1 和 Serpina1e 的 Z 变换平滑轨迹。(C-D) Ahsa1 和 Hsp90ab1 的年龄(折线图)和 PR(箱线图)趋势。
03
PR可以减弱衰老过程中泌尿系统表观基因组调控的改变
DNA甲基转移酶3α (Dnmt3a) 是一种关键的DNA甲基化酶,虽然其表达水平不如Hsp90ab1或Ahsa1显著,但对膀胱和肾脏有显著影响(图3A),提示其可能通过尿液成分进行调控。同样,在低蛋白饮食的M-FE小鼠膀胱中,DNA甲基转移酶1 (Dnmt1) 的表达上调(图3B),表明PR可能调节雌性泌尿系统的DNA甲基化模式。他们对年轻(M4)和年老(M24)小鼠以及M-FE高蛋白组和低蛋白饮食小鼠的膀胱进行了亚硫酸氢盐测序(RRBS)分析(图3C),各组小鼠的整体甲基化水平保持稳定(图3D),这与先前报道的DNA甲基转移酶表达变化而整体甲基化水平未发生改变的结果一致。基于启动子和差异甲基化区域(DMR)的通路分析揭示了衰老和 PR 改变的通路重叠,特别是与增殖和癌症相关的通路(图 3 E)。
接下来,他们探讨了衰老和PR是否会激活或抑制细胞增殖和癌症。肿瘤抑制基因(TSG)启动子区域的高甲基化与基因沉默和癌症相关。他们利用已发表的TSG数据集,鉴定了衰老组与青年组以及高蛋白饮食组与低蛋白饮食组之间甲基化改变的TSG(图3F)。衰老导致9个TSG中的7个发生高甲基化,而高蛋白饮食导致14个TSG中的8个发生高甲基化。因此,衰老和高蛋白饮食都可能增加癌症风险。值得注意的是,一些TSG,例如Ndn,在两种条件下均表现出高甲基化(图3G)。利用已发表的癌症DNA甲基化生物标志物数据集,他们分别在衰老组与年轻组以及高蛋白组与低蛋白组的比较中鉴定出81个和74个癌症DNA甲基化生物标志物,其中78个和70个基因的高甲基化与较高的癌症风险相关。在这些高甲基化基因中,衰老组和高蛋白组分别有61/78和42/70个基因处于高甲基化状态(图3 F),且两种条件下共有13个基因处于高甲基化状态(图3 H),这进一步证实了衰老和高蛋白均具有促进癌症发生的潜在作用。
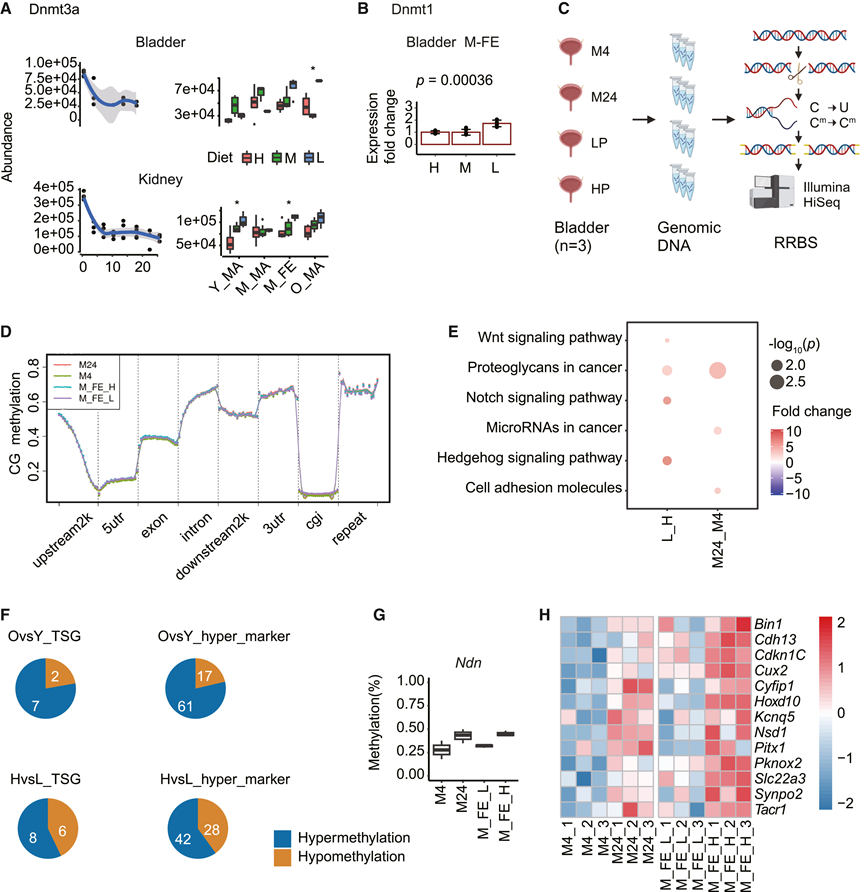
图3. 衰老和PR对膀胱RRBS的影响。
(A) 衰老过程中 Dnmt3a 表达趋势。(B) PR 条件下 M-FE 膀胱中 Dnmt1 的表达。(C) RRBS 工作流程。(D) 功能基因组元件的DNA甲基化水平。(E) 膀胱 DEP 的 KEGG 通路富集。(F) 高甲基化基因和低甲基化基因的计数。(G) Ndn启动子处的PR拯救的DMR。(H) 不同年龄和饮食组癌症相关标志物的甲基化。
04
磷酸化蛋白质组学揭示了衰老和PR过程中激酶的广泛调控
AMP激活蛋白激酶(AMPK)通路是能量代谢中公认的寿命调控因子,但PR对AMPK亚基及其靶器官的影响尚不明确。他们评估了六个AMPK亚基(例如Prkag1、Prkaa1),发现PR逆转了这些亚基的年龄相关性下调,尤其是在棕色脂肪组织(BAT)和胰腺中,且这种逆转作用在不同性别和年龄组均有观察到)。此外,PR还上调了Prkag1和Prkaa1在其他多种器官中的表达。
对这些器官的磷酸化蛋白质组学分析显示,在低蛋白饮食条件下,AMPK 基序表达上调(图 4A),表明AMPK 的激活。例如,在低蛋白饮食小鼠BAT中,含有糖原合成酶 2 (Gys2) AMPK 识别基序的前体显著上调(图 4B-C)。翻译后修饰(PTM)定位评分进一步证实了磷酸化发生在该基序内(图4B)。对该肽段进行平行反应监测(PRM)分析进一步验证了其在低蛋白饮食(LP)条件下的丰度增加。
在脑干中,PR上调了星形胶质细胞磷蛋白PEA-15 (Pea15)的AMPK基序磷酸化(图4D-E),PEA-15是反应性星形胶质细胞的标志物。然而,这种现象的功能意义仍存在争议。在SMV、肝脏和睾丸中,虽然观察到AMPK亚基的上调,但并未观察到预期的AMPK基序调控,这可能是由于检测深度或信号复杂性的限制所致。在SMV中,他们分别鉴定出衰老和PR处理过程中63个和29个差异表达的磷酸化肽,其中51个(80.9%)和24个(82.7%)分别来自SMV分泌蛋白(SVS)。有趣的是,他们观察到SVS4和SVS5中显著改变的磷酸化肽的丰度在衰老过程中上调(图4F)。在PR条件下,SVS4和SVS5中大多数发生显著变化的磷酸化肽表达下调(图4G),提示PR可能在生殖系统中发挥保护作用。他们研究了衰老和PR过程中其他差异表达的小鼠激酶(图4H-I)。衰老过程中最普遍失调的激酶包括:双特异性丝裂原活化蛋白激酶6(Map2k6),其在应激和炎症中起关键作用;丝氨酸/苏氨酸蛋白激酶D3(Prkd3),其调节囊泡运输、细胞存活和迁移;以及cAMP依赖性蛋白激酶催化亚基α(Prkaca),其介导代谢、基因表达和细胞增殖。在PR条件下,失调的激酶主要转变为非典型激酶,包括参与线粒体电子传递的非典型激酶COQ8A(线粒体)(Coq8a)和非典型激酶COQ8B(线粒体)(Coq8b),以及功能尚未明确的未表征的含aarF结构域的蛋白激酶5(Adck5)。然而,他们也发现了其他一些恢复的激酶,例如膀胱中的表皮生长因子受体(Egfr),它们是癌症治疗的主要靶点。总之,这些数据揭示了衰老和PR条件下激酶活性和蛋白质磷酸化模式的显著改变。
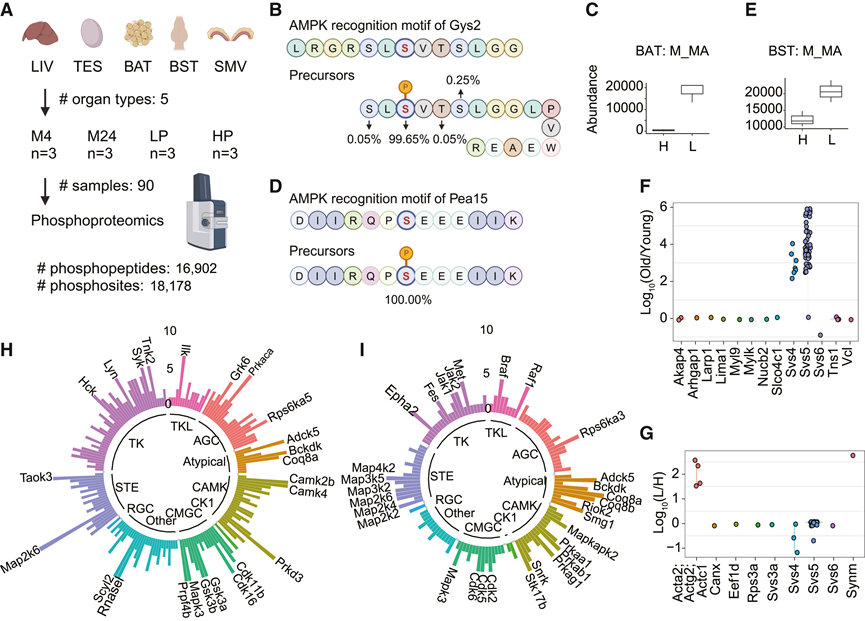
图4. 多器官磷酸化蛋白质组学分析。
(A) 磷酸化蛋白质组学分析流程。(B-E) Gys2 和 Pea15 中的 AMPK 基序分析。(F-G) 磷酸肽的散点图。(H-I) 衰老和 PR期间差异调节的激酶。
05
PR可能通过AMPK磷酸化改善脂肪组织功能
BAT中Gys2磷酸化水平升高以及BAT的PET/CT扫描结果提示BAT功能激活。所有PR组BAT中线粒体棕色脂肪解偶联蛋白1(Ucp1)的显著上调进一步支持了这一结论,其中低蛋白饮食小鼠的Ucp1表达量是高蛋白饮食小鼠的3倍(图5A)。白色脂肪组织(WAT)中Ucp1也上调,表明WAT发生褐变。Ucp1的免疫染色结果与蛋白质组学数据相符(图5B)。此外,BAT中脂质代谢调控相关的蛋白Cidec和Cidea的表达也上调(图5C),WAT褐变标志物Cox8b在WAT中也呈上调表达。值得注意的是,这些标志物的上调在中年雄性(M-MA)小鼠中最为显著。他们还观察到BAT中脂质代谢关键酶的显著上调,包括脂肪酸合成酶(Fasn)、乙酰辅酶A羧化酶2(Acacb)和单甘油酯脂肪酶(Mgll)(图5C)。油红O染色显示LP组中脂滴较小,这验证了脂质代谢的加速。有趣的是,他们观察到PR组所有组的胰岛素受体(Insr)和Slc2a4表达均显著增加(图5C),表明葡萄糖摄取增强。脂质代谢的加速和葡萄糖利用率的增加也可能促进产热。既往研究观察到PR下循环Fgf21水平的上调与产热增强相关。值得注意的是,大脑中Fgf21信号的缺失会完全消除这种产热反应。其他研究表明,PR诱导的Fgf21信号靶向谷氨酸能神经元,调节蔗糖摄入并诱导脂肪组织中Ucp1的表达。在PR条件下,Fgf21的受体Fgfr1在海马和小脑中显著上调。相反,他们观察到在高蛋白饮食条件下,BAT中与活性氧合成相关的蛋白质表达水平升高,这表明HP可能造成损伤(图5D)。
许多器官的脂质代谢和糖代谢均得到改善(图5E-I),因为这些过程中的关键酶发生了显著变化。有趣的是,这些变化影响的器官数量各不相同(图5 E-I)。例如,O-MA小鼠中Acacb的改变仅限于BAT、阴囊和甲状腺,而M-MA小鼠中Acacb的改变则扩展到肝脏、胰腺和肾上腺,这表明中年男性的代谢反应更为广泛。Apoa1、Lcat、Fabp4和Pck1也观察到了类似的模式(图5 F-I)。M-MA小鼠在食物摄入量、体重和脂肪组织功能改善方面也表现出最大的变化。有趣的是,PR增加了雌性小鼠的Apoa1水平,但降低了雄性小鼠的Apoa1水平(图5F),这表明雌性小鼠可能获得更大的心血管益处。此外,PR可能通过DNA甲基化对雌性泌尿系统产生更深远的影响(图3A-B)。总体而言,PR的影响因时间和性别而异,其中中年雄性小鼠表现出最显著的影响。
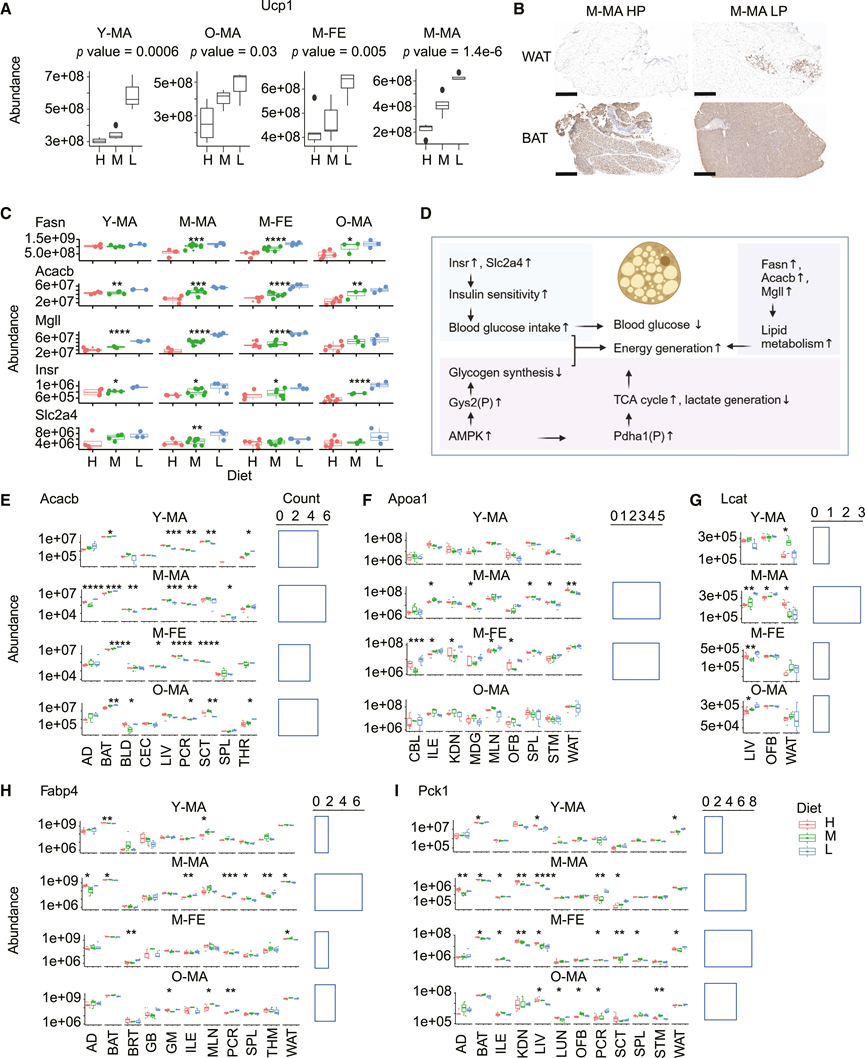
图5. PR条件下的脂肪功能和脂质代谢。
(A) 各组 Ucp1 表达。(B) 代表性的 Ucp1 免疫染色。(C) 在 PR 条件下 Fasn、Acacb、Mgll、Insr 和 Slc2a4 上调。(D) 改变的蛋白质总结。(E-I) Acacb、Apoa1、Lcat、Fabp4 和 Pck1 的器官表达趋势。
06
PR通过调节Lep、Igf1和心血管健康发挥全身性益处
接下来,他们分析了42只小鼠的血浆蛋白质组,这些小鼠经历了不同阶段的衰老(图6A)。在总蛋白质组水平上,均匀流形近似和投影(UMAP)分析显示出区分不同年龄组和饮食模式的中等能力。使用与年龄和饮食相关的差异蛋白进行UMAP可视化时,观察到各组之间有明显的分离。他们观察到PR组小鼠的瘦素受体(Lepr)水平升高,而瘦素(Lep)水平降低。由白WAT分泌的Lep会随着脂肪量的减少而减少,进而增加食欲,这与PR组小鼠体重减轻和食物摄入量增加的现象一致。值得注意的是,Igf1信号通路是小鼠血浆中与不同蛋白质摄入量相关的最显著富集的通路,而LP组小鼠的Igf1和生长激素受体(Ghr,小鼠)水平较低。已知Gh/Igf1轴的下调可以延长寿命,但Igf1也会随着年龄的增长而降低。在PR条件下,海马和膀胱中Igf1受体Igf1r表达下调,而衰老过程中未见显著变化。相反,许多其他器官在衰老过程中Igf1r表达显著上调,这可能是维持Igf1信号传导的一种代偿性表达。
除此之外,血浆中的DEP主要包括尿蛋白Mup2、Mup3和Mup20(图6B),这些蛋白能够结合雄性尿液中释放的信息素,从而影响雌性的性行为。此外,在PR条件下,Apoa4表达上调,Apoc3表达下调(图6B),这与预防心血管疾病的作用相关。既往研究也报道了孕期反应对心血管健康的益处,表现为葡萄糖耐量改善、高密度脂蛋白胆固醇(HDL-C)升高以及低密度脂蛋白胆固醇(LDL-C)和总胆固醇降低。
他们对衰老过程中小鼠的组织和血浆样本进行了成对分析,以发现器官和血浆中表达变化一致的蛋白质(图 6C)。简而言之,将 121 种与衰老高度相关的血浆蛋白(Pearson 相关系数,p < 0.05)与 99 种在不同器官中表达发生差异变化的蛋白质进行交集和相关性分析(图 6C-D)。其中 16 种与细胞间通讯相关,包括64 种细胞黏附分子 (CAM) 和表面受体。血浆骨膜蛋白 (Postn) 水平与其在WAT、膀胱、舌头和角膜中的蛋白表达水平呈正相关(图 6D),而骨膜蛋白在细胞黏附中发挥作用。据报道,衰老小鼠血浆中Postn蛋白水平与其在WAT、BAT和肌肉中的转录水平呈正相关。其他CAM,如Bcam、Pecam1、Ncam1、Nrcam和Glycam1,在衰老过程中也表现出显著的血浆-器官相关性(图6E)。有趣的是,血浆中Glycam1的表达与收集的所有四个淋巴结的变化高度相关(图6D)。另一种CAM,血管细胞黏附分子1(Vcam1),据报道其在衰老过程中血浆蛋白表达与其在肾脏和心脏中的相应转录水平呈正相关。Vcam1是通过衰老血浆介导大脑衰老的关键因子。与Vcam1类似,这些CAM也可能具有通过血液调节多器官衰老的潜力。许多细胞表面受体,例如 Cspg4、Lifr、Pigr 和 Egfr,也包含在这 28 种蛋白质中(图 6D-F)。有趣的是,在不同的蛋白质摄入条件下,血浆中 Bcam(在细胞黏附和迁移中起关键作用)和 Cspg4(参与细胞增殖和迁移)的表达与WAT和脑组织中的表达保持良好的相关性,表明它们具有作为器官健康循环标志物的潜力(图6H)。PR 可以逆转衰老过程中这些蛋白的表达变化(图6E-H),提示它们可能是PR发挥抗衰老作用的潜在靶点。综合分析,在血浆和器官蛋白质组中鉴定出28对高度相关的蛋白质,包括Bcam和Cspg4,这些蛋白质也显示出作为PR介导的抗衰老靶点的潜力。
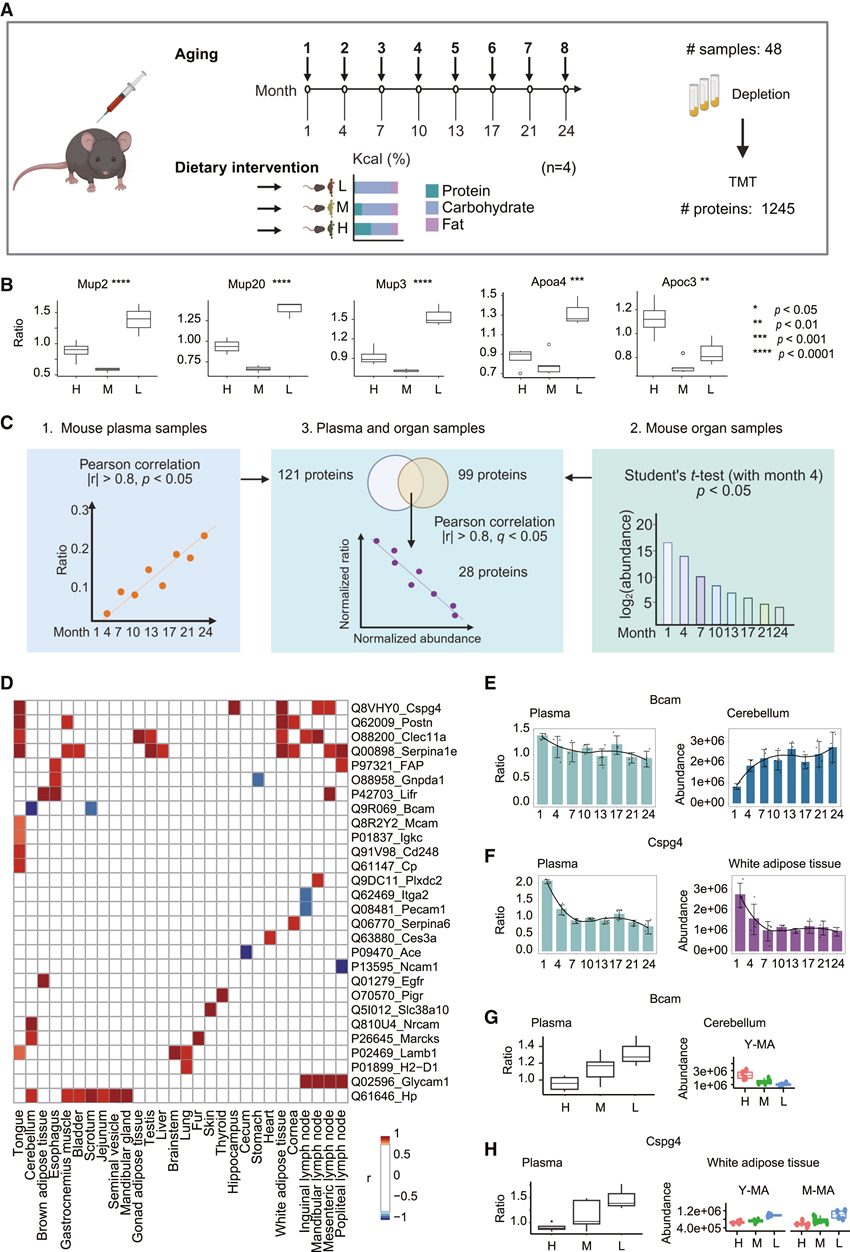
图6. 组织-血浆成对分析。
(A) 衰老和 PR期间小鼠血液样本采集的研究设计。(B) 不同饮食条件下血浆中 Mup2、Mup20、Mup3、Apoa4 和 Apoc3 的水平。(C) 潜在指标选择。(D) 前 28 种血浆蛋白在各个器官中的相关系数热图。(E-F) Bcam和 Cspg4在血浆和相应器官之间显示出高度表达相关性。(G-H) 血浆中的 Bcam和 Cspg4在 PR 期间表现出较高的血浆-组织相关性。
07
适度的蛋白质摄入可起到代谢和心血管保护作用
他们在 2015 年和 2018 年分别收集了 272 名年龄在 26 至 88 岁之间的个体的配对血浆样本和问卷数据(包括饮食信息和临床指标),基于 TMTpro 16plex 获得了 544 个人类血浆蛋白质组谱(图 7 A)。在进行进一步分析之前,已确认数据质量较高。该人群队列及其基本健康指标的分布在各年龄组中均较为均匀。人群中蛋白质能量摄入比例及其在2015年至2018年间的变化均近似呈正态分布。中位数分别为14.0%和0.4%,范围分别为4.9%至23.5%和-9.2%至12.6%。该队列的临床特征表明,低蛋白饮食与较低的胰岛素和糖化血红蛋白(HbA1c)水平相关(图7 B),提示代谢状态更健康,这与之前的研究结果一致。他们还从蛋白质组学数据中发现了代谢健康改善的证据,表现为谷丙转氨酶(GPT)水平降低(图7 C),提示肥胖、糖尿病和肝功能损害的风险降低。在低蛋白摄入的情况下,人类血浆中也发现了显著富集的胰岛素样生长因子 1 (IGF1, 人类) 信号通路以及较低水平的 IGF1 和生长激素受体 (GHR, 人类)(图 7 C),这与在小鼠血浆中观察到的情况类似。
在人体血浆中也观察到蛋白质摄入量与低密度脂蛋白胆固醇(LDL-C)呈正相关(图7B),提示低蛋白饮食可降低心血管风险。有趣的是,收缩压与蛋白质摄入量呈显著正相关,而舒张压与蛋白质摄入量无显著相关性(图7D)。此外,收缩压与总热量摄入或脂质摄入量均无显著相关性(图7D)。因此,在人体血浆中,他们进一步验证了低蛋白饮食对心血管的益处。然而,在人体数据中,DEP中最显著的是PTX3和硒蛋白P(SELENOP),它们仅与蛋白质摄入量呈显著相关(图7E)。PTX3的上调和SELENOP的下调提示炎症反应增强,暗示极低蛋白摄入可能存在潜在的副作用。
他们进一步研究了在人和小鼠血浆中衰老过程中呈现相似趋势,但在PR条件下发生逆转的蛋白质(图7 F-G),例如Notch1、Notch2、Ncam1、Nrcam和Pecam1。Notch1对细胞命运决定和组织发育至关重要, Notch2在维持组织稳态和调节细胞间相互作用方面发挥关键作用。在小鼠衰老过程中,Ncam1、Nrcam和Pecam1与多个器官表现出高度相关性(图6 D)。这些相关性是否在人类中仍然一致,还需要进一步验证。然而,这五种蛋白质与Bcam和Cspg4类似,都与细胞黏附和通讯密切相关,也可能是PR延缓衰老的潜在靶点。总之,人体和小鼠数据揭示了相似的调控模式,包括代谢改善、IGF1信号通路减弱和心血管风险降低,同时也提示极低蛋白摄入可能引发炎症。
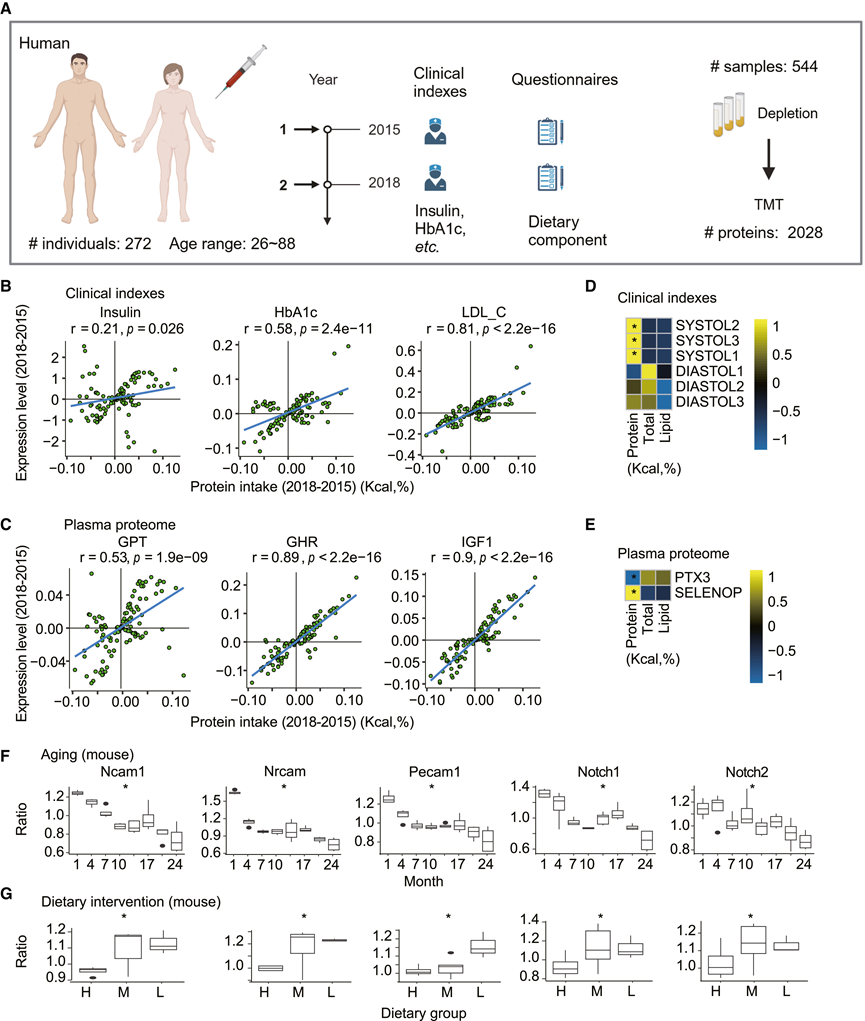
图7. 人血浆验证和 PR 相关信号。
(A) 队列:2015 年和 2018 年从 272 名个体(年龄 26-88 岁)收集的血液样本、临床数据和问卷。(B-C) 蛋白质摄入量变化与临床指标(胰岛素、糖化血红蛋白、低密度脂蛋白胆固醇)和血浆蛋白(谷丙转氨酶、生长激素释放激素受体、胰岛素样生长因子1)之间的关系。(D-E) 线性混合模型斜率显示膳食因素(蛋白质、总热量和脂质摄入量)对收缩压和舒张压以及血浆中 PTX3 和 SELENOP 蛋白表达的影响。(F-G) PR 挽救的蛋白质与小鼠-人类血浆的协调变化
+ + + + + + + + + + +
结 论
本研究对雄性小鼠衰老和PR期间的41种小鼠组织进行了全面的蛋白质组学分析,揭示了组织特异性的衰老标志,包括多种组织中免疫球蛋白和丝氨酸蛋白酶抑制剂的广泛变化。PR减轻了与年龄相关的组织特异性蛋白质表达、表观基因组状态和蛋白质磷酸化模式,并显著改善了脂肪组织功能。此外,对小鼠和人类血浆样本的分析证实了PR对心血管的益处,PR的影响存在性别和时间差异,中年是最佳干预时期。总而言之,本研究描绘了多器官衰老过程,并为PR的抗衰老潜力提供了宝贵的见解。
+ + + + +



 English
English


