文献解读|Nat Genet(29.0):发育中人类心脏的时空基因表达和细胞动力学
✦ +
+
论文ID
原名:Spatiotemporal gene expression and cellular dynamics of the developing human heart
译名:发育中人类心脏的时空基因表达和细胞动力学
期刊:Nature Genetics
影响因子:29.0
发表时间:2025.10.29
DOI号:10.1038/s41588-025-02352-6.
背 景
心脏是心血管系统的核心器官,负责将血液输送到全身。其功能依赖于四个心腔的协调收缩和两组心脏瓣膜的协同运作,并受到内在起搏传导系统以及内分泌和自主神经系统的严格调控。心脏的这种结构和功能复杂性在宫内发育的早期(妊娠早期)就已经形成。心源性中胚层在受孕后第三周出现,并演化成线性心管,随后经历广泛的空间重组和细胞分化,最终在受孕后第八周形成多层四腔心脏,其成熟和生长持续到胎儿期和出生后。除了心脏前体细胞外,心外膜原细胞和神经嵴细胞也参与心脏的形成。总体而言,早期心脏发育遵循精确的时空进程,其紊乱会导致先天性心脏异常,这凸显了理解其调控分子机制的重要性。
实验设计
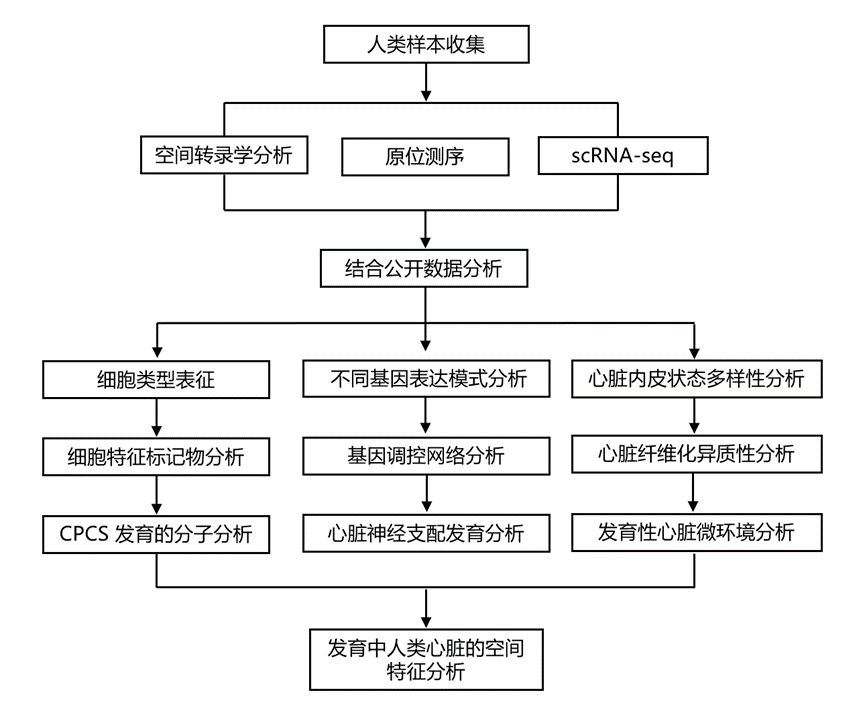
结 果
01
早期人类心脏发生的空间和细胞图谱
为了全面了解早期心脏发育过程中的空间分子模式,他们对16颗处于第6至12周原始心包腔[妊娠后第5.5周至第12周(PCW 6至12)]的心脏进行了空间转录组学分析,并对另外4颗心脏中的150个选定转录本进行了原位测序(ISS)分析。他们构建了一个包含来自38个心脏切片的69114个组织点的数据集,涵盖了发育中器官的所有主要结构成分(图1a)。为了研究区域性的分子决定因素,他们选择了至少包含三个心腔的17个切片,并对相应的25208个组织点进行了无监督聚类,结果得到了23个在空间上基本一致的空间聚类,这些聚类具有不同的空间转录组特征(图1a-d)。该分析突出了主要心肌隔室的侧向特异性富集标记物以及乳头肌中与应激相关的分子特征(图1e-f)。此外,对整个空间转录组数据集进行非负矩阵分解,划分出20个空间基因模块。
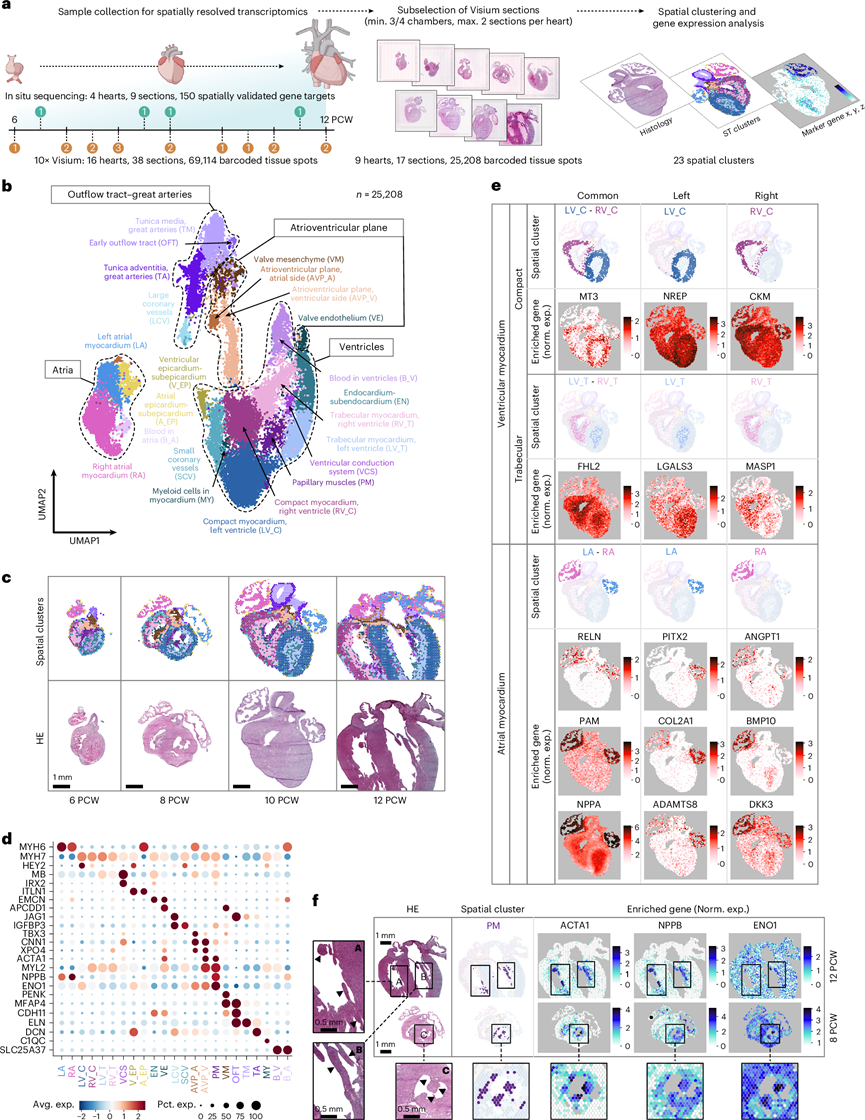
图1. 发育中人类心脏的空间分布图。
(a) 空间分辨转录组数据集生成概览。(b) 发育中心脏的23个空间聚类,对应于主要的心脏结构成分。(c) 空间聚类分布的时间演变,分别在6、8、10和12个PCW心脏切片中呈现。(d) 23个空间聚类中共有细胞类型标记和选定的DEG的相对富集情况 。(e) 选定DEG的侧向特异性富集情况。(f) 空间特征图展示了乳头肌中与应激相关的基因特征,并突出了相应空间聚类(PM)中选定的DEG。
02
人类早期心脏发生的细胞图谱
接下来,他们对15个处于妊娠第5.5周至第14周的心脏样本进行单细胞转录组分析(scRNA-seq),以探索发育中心脏组织的细胞组成。对76991个高质量心肌细胞进行无监督聚类,定义了31个大细胞亚群和72个精细粒细胞亚群,这些状态具有不同的转录组特征,为整个研究期间的后续分析构建了通用框架。利用这些聚类对空间转录组数据集进行反卷积,以绘制它们在心脏切片中的位置,从而构建了一个空间感知的细胞状态图谱(图2a)。通过预测的空间定位、典型细胞类型标记的表达以及差异表达基因谱的分析,他们鉴定了主要的心肌细胞(CM)、内皮细胞(EC)和壁层非心肌细胞(MC)及成纤维细胞(FB)群体,以及数量较少的神经母细胞和神经元(NB-N)群体、雪旺细胞祖细胞和胶质细胞(SCP-GC)群体。此外,他们还通过精细聚类分析进一步研究了这些细胞群体,以及其他核心心脏细胞类型(图2b-d)。粗粒度聚类分布的时间变化与早期心脏发育的关键事件相对应(图2e-f)。他们还鉴定并表征了壁细胞,例如周细胞 (PC) 和两种空间上不同的平滑肌细胞群(OFT_SMC 和 CA_SMC),以及两个富含胸腺素转录本的细胞聚类 (TMSB10high _C_1–2),这两个细胞聚类此前已证实与冠状动脉发育有关。此外,他们检测到了髓系细胞 (MyC) 和淋巴系细胞 (LyC) 群,以及两个以红细胞为主的细胞聚类,这两个细胞聚类排除在后续分析之外,并鉴定了一种心外膜细胞 (EpC) 群。
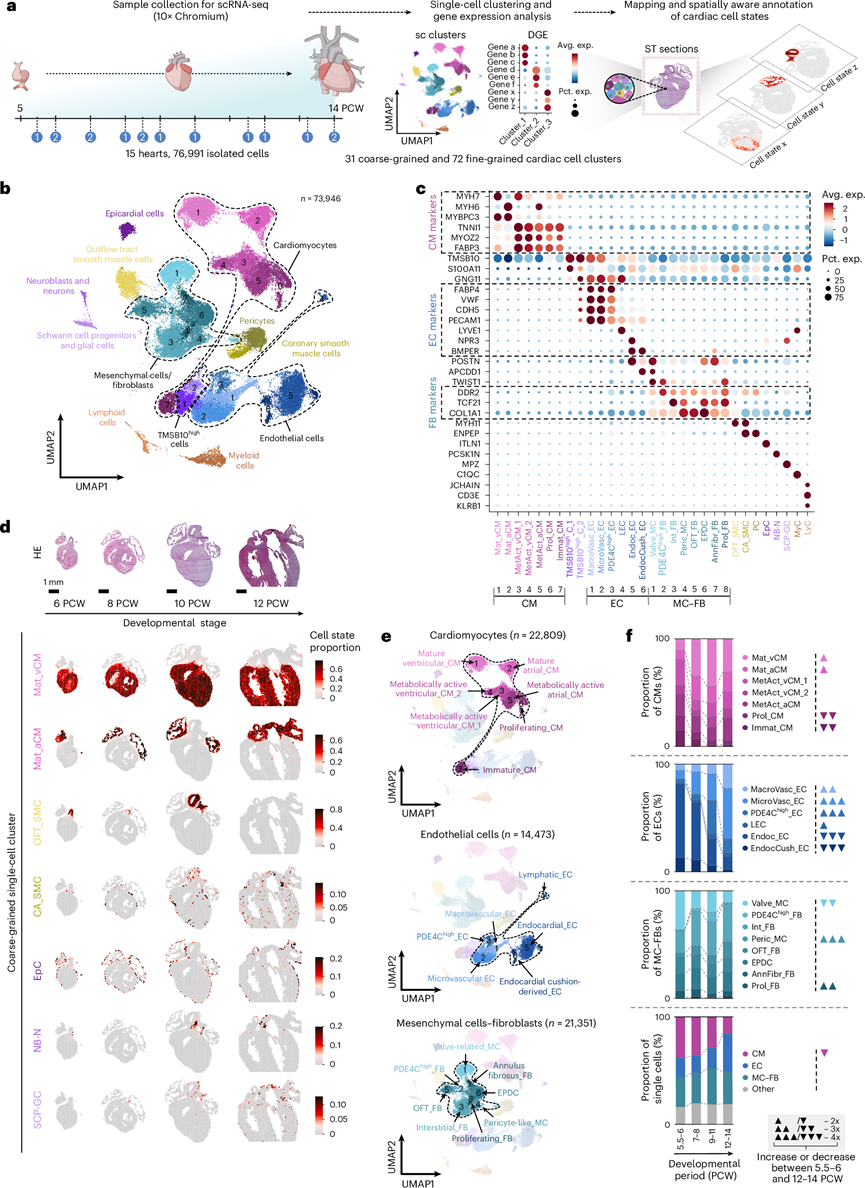
图2. 人类早期心脏发生的细胞图谱。
(a) Chromium单细胞数据集生成及心肌细胞状态的空间信息注释概述。(b) UMAP图展示了31个粗粒度心肌单细胞聚类,对应11种主要细胞类型。(c) 粗粒度单细胞聚类中典型细胞类型标记的富集情况。(d) 在6、8、10和12个PCW心脏切片中选取的粗粒度聚类的时空映射。(e) 粗粒度CM、EC和MC-FB聚类的空间感知注释。(f) CM、EC 和 MC-FB 聚类中粗粒度聚类比例随时间的变化。
03
发育中的起搏传导系统的分子图谱
CM是心肌的基本收缩单位,但它们的协调运作依赖于心脏起搏传导系统(CPCS)的特殊细胞,从而实现内在的自律性和及时的电脉冲传导。CPCS细胞的分子特征此前已在动物模型和成人心脏中进行过研究,但在人类发育过程中仍未阐明。他们通过对心肌细胞群进行聚类分析,鉴定了19种不同的细胞状态,证实了其高度的转录多样性(图3a-b)。其中,他们观察到一些细胞聚类对先前报道的CPCS标记物具有强表达。空间定位将这些细胞聚类追踪到与窦房结(SAN_CM)、房室结(AVN_CM)、房室束及其分支(AVB-BB_CM)和浦肯野纤维(PF_CM)位置一致的组织区域(图3c)。值得注意的是,他们观察到另一个心室聚类,它具有共同的转录特征,并且与 PF_CM有密切的空间关联,推测代表过渡性 PF (TsPF_CM)。
CPCS CM显示出显著的转录组特征重叠。SAN_CM和 AVN_CM表达在起搏细胞中特异性或高度富集的转录因子(SHOX2、TBX18、PRRX1、ZNF385B),以及轴突导向分子(TENM2、TENM3、TENM4、GDF10、SLIT2),表明这些节点是发育中心脏神经支配的关键靶点(图3d)。他们还发现轴突导向分子伴侣LRRC4C在 SAN_CM 中特异性表达。AVN_CM中高度富集的基因反映了房室结在房室平面上的位置(BMP2、RSPO3、ADAMTS19)以及这些细胞的神经元特征(NRXN3、ZNF536)。PF_CM表达几个特征性标记物(CSMD1、BRINP3、SGCD、NTN1、SEMA3A),部分与TsPF_CM共有(图3e)。虽然最近报道的房室束标记物CNTN5和CRNDE42在本研究的数据集中分布更广泛,但AVB-BB_CM中富集的几个基因(RCAN1、HS3ST3A1)特异性地集中在室间隔上缘,可能标记了该结构(图3e)。有趣的是,vCM_1 聚类的CNTN5表达最高,并且与 CPCS(TBX3、HS3ST3A1、BRINP3、TENM3)和收缩性 vCM 状态(PRDM16、NLGN1、SORBS2、MYL2)均共有富集基因。此外,其转录组谱(XPO4、MYL2、TNFRSF19、SORBS2、ZFP36L1)以及在瓣膜根部和房室区域的预测定位与难以捉摸的 AVP_V 空间聚类相匹配,表明其可能具有过渡性特征,有助于房室传导组织的形成。
CPCS 成分的电生理特性受其离子通道库的影响(图3f),正如最近在成人心脏中研究的那样。在本研究的数据集中,发育期窦房结心肌细胞 (SAN_CM) 和房室结心肌细胞 (AVN_CM) 具有典型的结细胞离子通道谱,其中超极化激活阳离子通道(HCN1、HCN4)以及几种 L 型和 T 型钙通道基因(CACNA1C、CACNA1D、CACNA1G、CACNA2D2、CACNB2)显著富集,这些通道均参与结动作电位的去极化阶段。与成人不同,CACNA1G在 AVN_CM 中富集程度最高,而 SAN_CM 和心室 CPCS 细胞状态的表达较低。CM的复极化主要由钾通道驱动,也表现出细胞类型特异性模式。SAN_CM高表达G蛋白偶联内向整流钾通道亚基KCNJ3,KCNJ3是已知的成人PF细胞标志物,而在本研究的数据集中的发育对应细胞中则未见表达。相比之下,PF_CM富集KCNJ2和KCNH7。AVN_CM高表达KCNQ1(此前已报道其与房室传导阻滞相关),以及与收缩性心肌细胞共有的离子通道亚基(例如CACNA1C、KCNQ3、KCNQ5),提示其具有混合的电生理特征。尽管在成年房室束中富集的KCND2及其功能相关的KCND3在本研究的数据集中表达量较低,但它们已知的互作蛋白KCNIP4在vCM_1细胞中高度富集,这进一步支持了该细胞状态在房室传导组织发育中可能发挥的作用。缝隙连接基因的表达模式与成年细胞相似,低电导Cx45(GJC1)在窦房结心肌细胞(SAN_CM)和房室结心肌细胞(AVN_CM)中富集,而高电导Cx40(GJA5)则在盆底心肌细胞(PF_CM)中富集。
除了几个氯离子通道、体积调节阴离子通道和瞬时受体电位通道(其在 CPCS 功能中的作用尚不明确)之外,他们还观察到 SAN_CM中几个离子型谷氨酸受体基因(GRID2、GRIK1)的富集,这支持了在谷氨酸能信号传导机制,以及 PF中 GABA 受体离子通道GABRB2基因的富集,该基因特异于发育阶段(图3f)。
为了研究起搏器表型特化的分子驱动因素,他们推断了窦房结心肌细胞(SAN_CM)的基因调控网络(图3g)。关键转录因子(SHOX2、PRDM6、THRB、FOXP2)和离子通道靶点(HCN1、CACNA1D、KCNT2、CACNB2)与近期对成年SAN_CM的分析结果存在显著重叠。其他在SAN_CM中富集的已知起搏器调控因子包括TBX18、BNC2和TBX3,其中TBX3在房室结心肌细胞(AVN_CM)、房室传导阻滞伴血小板增多症心肌细胞(AVB-BB_CM)和vCM_1细胞中表达显著更高。TBX3抑制心房收缩基因程序;因此,其在CPCS组分中的广泛表达与其在小鼠中先前描述的渐进性命运限制相一致。值得注意的是,SAN_CM 调控网络还包括转录因子BHLHE41和RORA,它们是哺乳动物昼夜节律钟的调节因子,与心律失常易感性的昼夜变化有关。
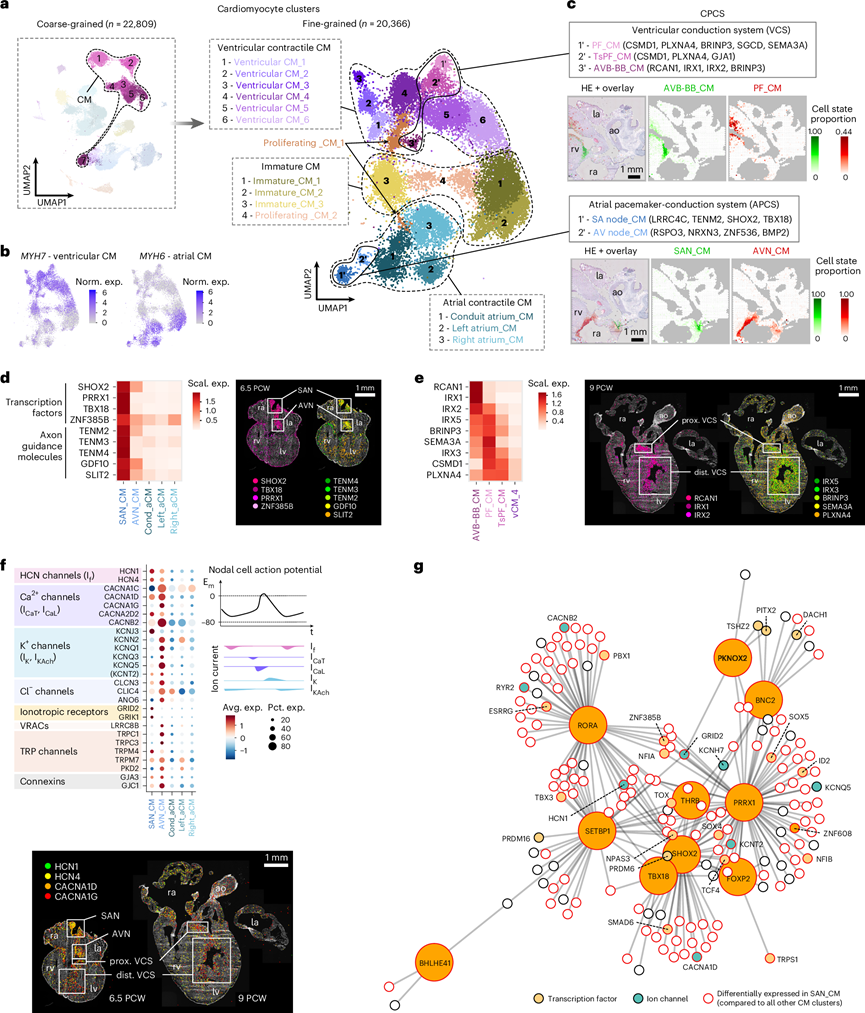
图3. CPCS 发育的分子图谱。
(a) UMAP图显示了7个粗粒度和19个细粒度的心肌细胞聚类。(b) MYH7和MYH6的特征图分别勾勒出心室和心房的特征。(c) CPCS的心肌细胞组成部分及其特征标记和在11个PCW心脏切片中的预测定位。(d) 热图可视化了SAN_CM和AVN_CM中转录因子和轴突导向分子的基因尺度表达。(e) 热图展示了AVN-BB_CM、PF_CM、TsPF_CM和vCM_4细胞中CPCS标记基因的单基因表达水平。(f) 散点图展示了SAN_CM和AVN_CM中特定离子通道相对于收缩性心房心肌细胞聚类的相对表达水平(左上图)。结细胞动作电位的离子电流示意图(右上图)。通过ISS检测6.5 PCW和9 PCW心脏切片中HCN和T型Ca2+通道转录本的空间分布模式(下图)。(g) SAN_CM的基因调控网络,包括与所有其他CM状态相比差异表达最显著的十个转录因子及其相关靶基因。
04
心脏神经支配和嗜铬细胞的形成
为了探索早期心脏神经支配的形成,他们将粗粒度的 NB-N 和 SCP-GC 群体重新聚类为 10 个细粒度的聚类,其中包括 5 个 SCP(SOX10、FOXD3)、1 个髓鞘化雪旺细胞(My_SC;MPZ、PMP22、MBP)、1 个中间桥接状态(ASCL1)、2 个自主神经母细胞-神经元聚类(Aut_Neu_1-2;PRPH、STMN2),以及值得注意的是,1个富含CHGA、CHGB和PENK的聚类,该聚类标志着局部神经内分泌嗜铬细胞群(Chrom_C)(图4a-b)。与嗜铬细胞在缺氧反应中的关键作用相一致,心脏嗜铬细胞(Chrom_C)表现出分子缺氧传感器的强表达,例如EPAS1(编码HIF2α)、COX4I2和HIGD1C,这些传感器最近在颈动脉体的氧感知机制中发现(图4b)。这是首次在发育中的心脏内原位观察到嗜铬细胞,因为在小鼠模型中它们并不存在,因此这似乎是人类特有的心脏特征。RNA速率和拟时序分析证实了从早期SCP到神经元-嗜铬细胞和胶质细胞谱系两条平行轨迹的叉状转变(图4c-d)。
Chrom_C和 Aut_Neu_2 细胞占据大动脉心房和外膜中相邻但不同的区域,这反映了它们共同的起源和不同的功能(图4e)。同时,SAN_CM附近的 Aut_Neu_2 富集区域可能代表直接支配结节组织的神经元(图4e)。大多数 SCP 状态呈分散分布,但 SCP_5 细胞和 My_SC则集中在神经结构周围。
他们发现生长抑素(SST)是Aut_Neu_1和Aut_Neu_2细胞群中表达的主要神经递质基因,而胆碱能标记物CHAT则在这些细胞中表达较少(图4b-f)。同时,Chrom_C强烈表达TH,并少量表达DBH和PNMT,它们编码儿茶酚胺合成的关键酶(图4b-f)。这表明,发育中的心内神经节丛神经元主要利用肽能传递,胆碱能传递较少;而局部嗜铬细胞是早期胎儿心脏组织中去甲肾上腺素(以及少量肾上腺素)的主要来源。
有趣的是,他们在数据集中几乎未发现生长抑素受体的表达;同时,β1肾上腺素能受体(ADRB1)在窦房结心肌细胞(SAN_CM)和房室结心肌细胞(AVN_CM)中显著富集,而M2乙酰胆碱受体(CHRM2)在CPCS心肌细胞中表达更为广泛(图4f-g)。基于关键酶(TH和CHAT)和受体(ADRB1和CHRM2)的协同表达水平,计算了Chrom_C、Aut_Neu_2和SAN_CM状态之间的配体-受体评分,进一步证实了肾上腺素能和胆碱能介导窦房结功能的不同来源。
基于这些发现,他们提出一种机制:在早期胎儿心脏中,副交感神经信号由局部神经元传递,而交感神经调节则由驻留嗜铬细胞通过旁分泌信号介导,以响应组织缺氧。这些相互作用可能调节CPCS CM中的离子通道,从而使心率和传导速度适应环境条件(图4h)。此外,心内嗜铬细胞的存在也可能解释罕见心脏嗜铬细胞瘤的起源。
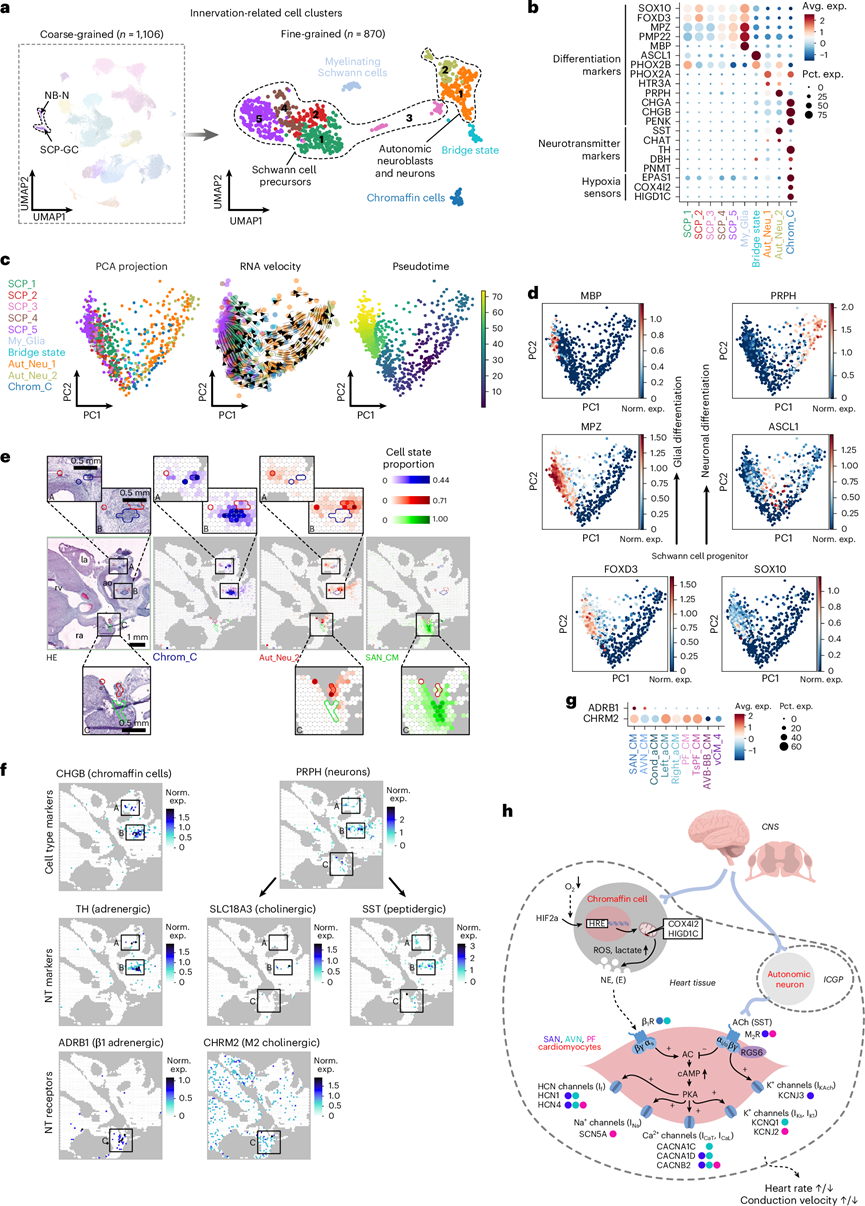
图4. 自主心脏神经系统和常驻嗜铬细胞的早期形成。
(a) UMAP图显示了与心脏自主神经支配相关的粗粒度NB_N和SCP-GC细胞聚类以及十个细粒度细胞聚类。(b) 散点图展示了所有细粒度神经支配相关细胞聚类中神经胶质细胞、神经元和嗜铬细胞分化标志物、神经递质相关基因以及急性氧感知机制组分的相对表达。(c) RNA速度和伪时间分析揭示了神经支配相关细胞聚类中两条平行的发育轨迹。(d) 神经胶质细胞和神经元分化标志物的表达。(e) 细胞的空间分布图。(f) 神经递质(NT)代谢相关基因和受体的空间特征图。(g) 点图展示了起搏传导系统心肌细胞中β1肾上腺素能受体和M2胆碱能受体转录本的富集情况。(h) 胎儿心脏功能自主控制的模型示意图。
05
心内膜垫衍生结构中的内皮状态
在合并的粗粒度内皮细胞 (EC) 和TMSB10高表达_C_2 的细胞聚类中,他们定义了 18 个细粒度细胞状态(图5a),涵盖了来自大动脉和冠状血管以及心内膜的多种内皮细胞群体。他们还观察到三个细胞聚类,它们共同富集了对心内膜垫形成至关重要的内皮-间质转化调节因子(NFATC1、APCDD1和TWIST1),但同时也具有截然不同的转录谱。空间定位追踪到发育中心脏瓣膜两侧的两种细胞状态,在胎盘发育第6周(PCW 6)起,房室瓣和半月瓣中就已稳定存在流入和流出瓣膜内皮细胞(分别为IF_VEC和OF_VEC),表明它们早期就已分化(图5b)。IF_VEC中高度富集的基因包括WNT信号通路中的一些组分(WNT2、WNT4、WNT9B、DKK2、PTHLH),其中一些在瓣膜闭合区表现出空间富集(图5c)。OF_VEC表现出高表达 BMP 配体(BMP4、BMP6)、WNT 信号调节因子(LGR5)和内源性大麻素受体CNR1,在半月瓣纤维侧有显著的空间富集,在房室瓣心室侧有中等程度的富集(图5c)。同时,聚类3在心房隔膜内表现出高度独特的空间定位(AtrSept_EC),标志着一种此前未曾描述的心脏内皮细胞状态(图5d)。除了更具体的标记(NEGR1、ALCAM、SEMA3A、CCDC80、MSX1)外,AtrSept_EC与心内膜细胞群(Endoc_EC_4)共有几个高度富集的基因(LRRC4C、LSAMP、OPCML),该细胞群勾勒出光滑壁的心房。
基因调控网络和调控子富集分析进一步揭示了这三种细胞状态之间的分子差异(图5e-f)。他们发现MSX1和LEF1——已知在心内膜垫形成过程中介导内皮-间质转化的因子,近期在小鼠心房隔膜中也检测到了它们,并且与人类心房隔缺损有关——是AtrSept_EC中富集程度最高的转录因子。在OF_VEC中,他们发现PROX1和FOXC2转录因子富集,已知它们在响应振荡剪切应力时协同作用,维持细胞外基质结构并防止心脏瓣膜的黏液样变性。 IF_VEC 中富集的几种转录因子在调节 WNT 信号通路中发挥着已确立的作用,包括KLF4和SMAD6,它们是已知的内皮细胞层流剪切应力的转导因子。重要的是,早在 PCW 5.5-6 时,IF_VEC 和 OF_VEC 之间这些转录因子的调控子富集就存在显著差异,这表明血流动力学力是胚胎期 VEC 多样化的核心因素。
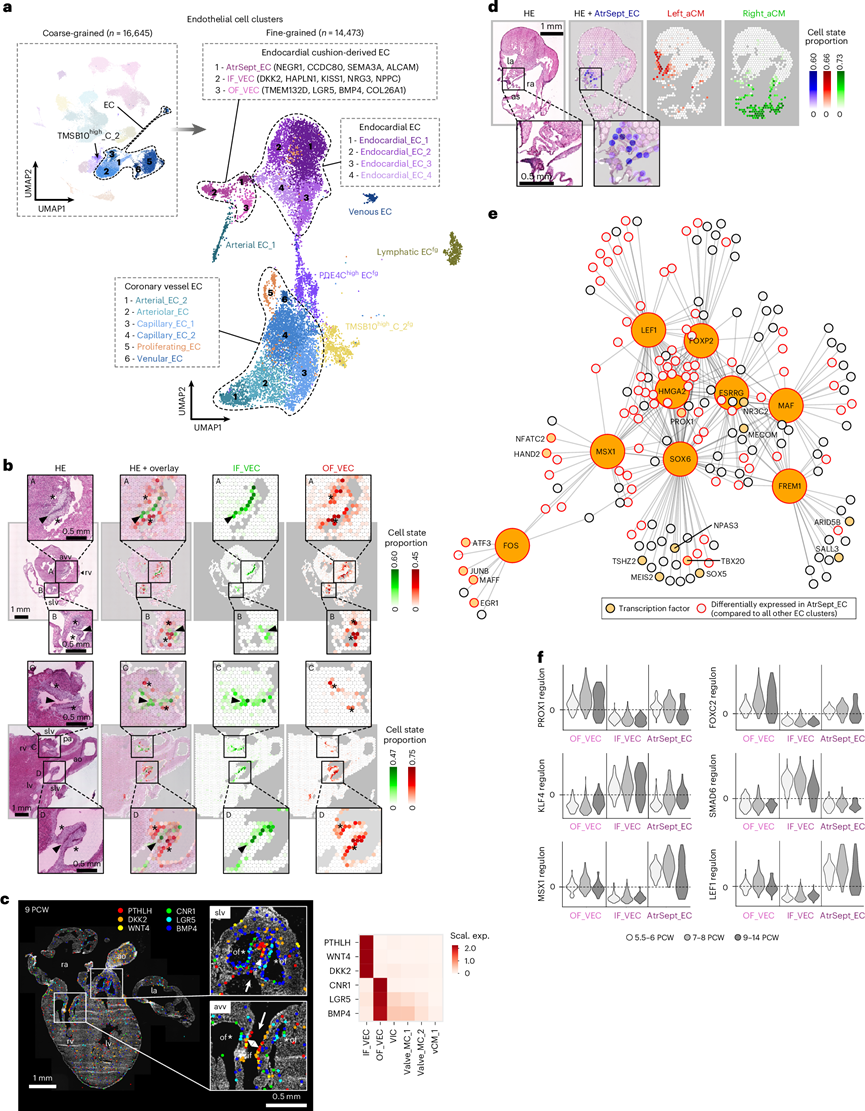
图5. 心内膜垫衍生结构中位置依赖性EC多样性。
(a) UMAP可视化。(b) 在 8 PCW(上图)和 12 PCW(下图)心脏切片中,IF_VEC(绿色)和 OF_VEC(红色)在房室瓣(ROI A)和半月瓣(ROI B–D)两侧的空间分布图。(c) 通过 ISS 检测到 9 PCW 心脏切片中房室瓣和半月瓣中特定 IF_VEC 和 OF_VEC 标记物的侧向空间富集(左图)。热图显示了瓣膜中富集的相同基因在 EC、MC 和 CM 状态下的单基因表达水平(右)。(d) 在 8 PCW 心脏切片中,AtrSept_EC(蓝色)在以 Right_aCM 为主(绿色)和 Left_aCM 为主(红色)区域之间的心房隔膜上的空间映射。(e) AtrSept_EC 的基因调控网络,包括与 IF_VEC和 OF_VEC相比富集的转录因子及其相关靶基因。(f) 小提琴图展示了 AtrSept_EC、IF_VEC 和 OF_VEC中选定转录因子在三个年龄组(5.5–6、7–8 和 9–14 PCW)中的调控子富集情况。
06
发育性心脏纤维化的空间异质性
由于其显著的转录异质性和缺乏明确的分子标记,成纤维细胞(FB)和心肌细胞(MC)构成发育中心脏细胞的一个模糊亚群。空间因素,反映了其祖细胞的位置和与微环境相关的环境信号,在定义该细胞群的细胞身份方面起着核心作用。为了探索这种拓扑多样性,他们将18个心脏FB和MC聚类空间映射到特征性组织位置(图6a),包括大动脉和冠状动脉的外膜(图6b)、心外膜下层(图6c)和心肌(图6d)。值得注意的是,他们在房室沟和心肌中发现了一种具有类似于纤维脂肪生成祖细胞标记特征的细胞状态,这可能对心外膜脂肪形成和致心律失常性右室发育不良的发病机制具有潜在意义(图6e)。
聚类分析还鉴定出发育中心脏瓣膜的三种不同的MC状态(图6e-f),进一步阐明了它们的细胞多样性。表达APCDD1、LEF1、TMEM132C和ADAMTS19的瓣膜间质细胞(VIC)定位于两组瓣膜的游离段,而Valve_MC_1细胞(FGF14、HDAC9、PLCXD3)似乎富集于半月瓣瓣叶的根部和纤维环周围的节段,但在房室瓣中则基本缺失。同时,Valve_MC_2细胞(PENK、FMOD、TIMP3)存在于半月瓣和房室瓣的根部及其周围,以及纤维环的内部区域,这与AnnFibr_FB形成对比,后者主要分布于心外膜下区域,可能构成该结构的外缘。重要的是,Valve_MC_2细胞特异性且强烈表达PENK,PENK是先前报道的小鼠心脏中间充质神经嵴衍生物的标志物(图6f)。他们在发育中的半月瓣和房室瓣及其周围观察到强烈的PENK空间信号,这支持了长期以来关于神经嵴细胞对人类这两种瓣膜结构贡献的观点。事实上,他们在胎龄第6.5周(PCW 6.5)就观察到房室瓣内侧瓣叶中存在PENK表达,到胎龄第9周(PCW 9)时,PENK表达似乎向外侧瓣叶扩散,同时在两个取样的主动脉瓣瓣叶中均检测到半月瓣相关的PENK信号(图6g)。综上所述,神经嵴来源的间充质对人类心脏瓣膜的贡献比之前认为的更为显著。基于这些结果,他们构建了胎儿心脏中MC和FB细胞状态的空间模型,这些细胞状态参与构成纤维骨架和嵌入的瓣膜结构(图6h)。
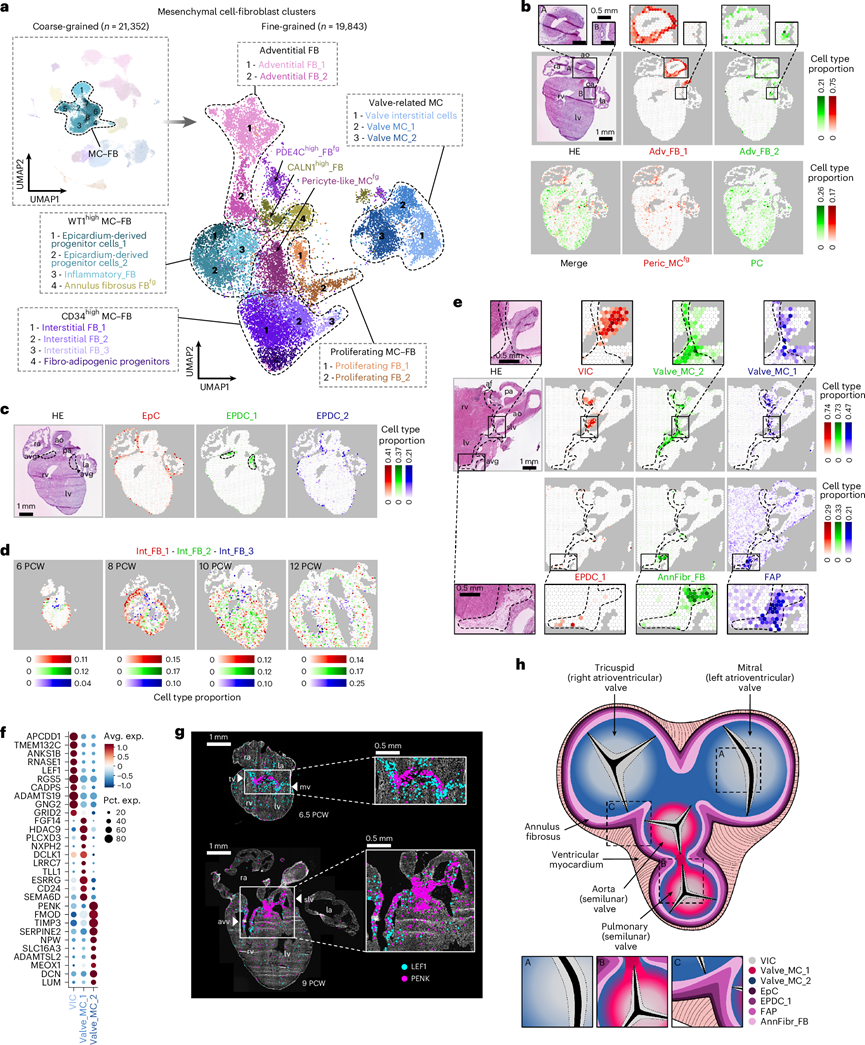
图6. 发育中心脏中 FB 和 MC 异质性的空间分解。
(a) UMAP图显示了8个粗粒度和18个细粒度的FB和MC聚类。(b) 心脏结构的空间映射。(c) 在10周心脏切片中,心外膜细胞(EpC)(红色)、EPDC_1(绿色)和EPDC_2(蓝色)细胞在心脏表面、心内膜下层和房室沟(虚线)的空间分布图。(d) 在6、8、10和12周心脏切片中,Int_FB_1(红色)、Int_FB_2(绿色)和Int_FB_3(蓝色)细胞的空间分布图。(e) 在12周心脏切片中,MC和FB状态在房室平面(虚线)和心脏瓣膜中富集的空间分布图。(f) 点图显示了 VIC、Valve_MC_1和Valve_MC_2聚类之间差异表达最显著的十个基因。(g) 在6.5 PCW和9 PCW心脏切片中,利用ISS技术检测心脏瓣膜中的PENK和LEF1。(h) 胎儿心脏纤维骨架和心脏瓣膜中FB和MC状态排列的空间模型。
07
基于空间信息的发育性心脏微环境分析
细胞微区室在早期心脏发育过程中发挥着关键作用,它们决定着引导细胞行为的环境信号。他们利用深入的空间分析,勾勒出主要发育组织区室和精细微环境的细胞组成,从而实现对其的靶向分析。通过计算基于成对相关性的共检测得分并可视化其拓扑关系(图7a),研究了72个精细单细胞状态的空间重叠情况,结果在三个发育年龄组中均表现出高度一致性。
在CPCS模型中,他们发现CALN1high_FB、SAN_CM和AVN_CM的预测位置存在显著重叠,这支持了CALN1high_FB代表发育中结节组织的间充质成分的假设。值得注意的是,AVN_CM与AtrSept_EC状态的空间共检测得分最高,表明胎儿心脏心房隔膜中存在传导性心肌细胞(图7b)。他们还鉴定了SAN_CM与其周围细胞之间的几个潜在配体-受体对,包括从起搏细胞指向紧密定位的静脉内皮细胞(Ven_EC)的配体-受体对,以及可能参与与自主神经元形成接触的配体-受体对(Aut_Neu_2)(图7c)。值得注意的是,CALN1high_FB与SAN_CM的相互作用谱与最近在成年心脏中发现的一种神经胶质细胞状态存在显著重叠,这提示该细胞群可能具有正在发育的混合功能。心室CPCS组分彼此之间以及与心室富集的内膜Endoc_EC_1和Endoc_EC_2细胞状态的关联最为密切,PF_CM的共检测在时间上从Endoc_EC_1向Endoc_EC_2发生转变,并且与小梁形态发生和PF特化相关的配体-受体相互作用也存在差异。
通过识别五种空间上不同的瓣膜EC和MC状态,以及在瓣膜根部和心室肌房室区富集的 vCM_1 细胞群,他们研究了以前所未有的空间和细胞分辨率绘制了发育中的人类心脏瓣膜结构图(图7d)。因此,进一步绘制了这些细胞群中 WNT、BMP 和 TGFβ 信号通路成分的分布图,这些成分是瓣膜形成的关键调节因子,也是先天性和获得性瓣膜疾病的致病因素(图7e)。 IF_VEC显示出 WNT 配体(WNT2、WNT2B、WNT4、WNT9B、WNT11)、拮抗剂和信号抑制剂(ZNRF3、DKK2、DKK3)的显著富集,而 OF_VECs 则表达更高水平的 WNT 受体(FZD10、ROR1、ROR2)和信号增强剂(LGR5),以及多种 BMP 配体(BMP4、BMP6)和拮抗剂(SOST、FST、FSTL4)。这些模式与流体动力在调节 WNT 激活和 BMP 抑制中的作用相一致,流体动力此前已描述为由 KLF2介导。虽然在动物模型中已报道了 WNT 和 BMP 信号的侧向特异性分布,但本研究研究首次系统地绘制了它们在发育中的人类瓣膜中的区室化分布图。
心脏瓣膜在先天性和后天性心脏病中均常受累,但这些病理的具体细胞驱动因素通常仍未明确。本研究分析了与两种主要瓣膜异常—二叶式主动脉瓣和二尖瓣脱垂—相关的基因在不同瓣膜细胞状态下的表达模式(图7f)。虽然二尖瓣脱垂相关基因表达广泛,但一些与非综合征型二叶式主动脉瓣疾病相关的基因在IF_VEC和VIC中显著富集,表明这些细胞状态特别脆弱。
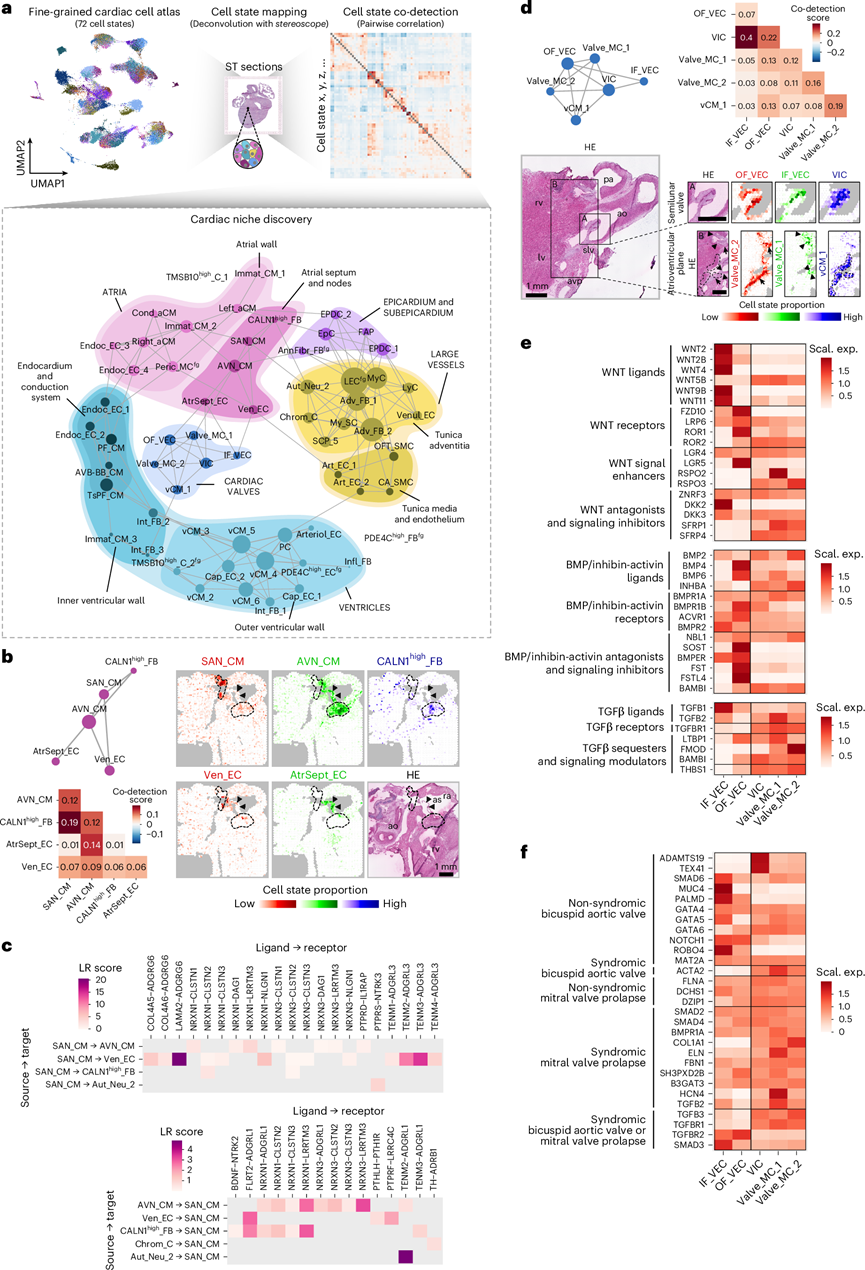
图7. 发育中心脏微环境的空间信息分析。
(a) 应用微环境发现策略的示意图。(b) 心房隔膜和CPCS微环境网络图和空间映射。(c) 基于空间信息的SAN_CM、其细胞邻域和Chrom_Cs之间的细胞间通讯分析。(d) 心脏瓣膜微环境网络图及其对应的共检测得分,以及空间映射。(e) 热图展示了瓣膜EC和MC状态下WNT、BMP和TGFβ信号通路成分的基因尺度表达。(f) 热图显示瓣膜EC和MC状态下二叶式主动脉瓣疾病相关基因和二尖瓣脱垂相关基因的基因表达水平。
+ + + + + + + + + + +
结 论
本研究结合了非靶向空间组学和单细胞转录组学以及基于成像的验证方法,对受孕后5.5至14周的人类早期心脏发育进行了分析,揭示了人类早期心脏发生的分子图谱。构建了人类发育心脏的高分辨率转录组图谱,揭示了31种粗粒度和72种细粒度细胞状态的空间排列,这些细胞状态组织成不同的功能微环境。本研究的发现为心脏起搏传导系统、心脏瓣膜和心房隔膜的形成提供了关键见解,并揭示了心脏间充质细胞中意想不到的多样性。此外,本研究还追踪了自主神经支配的出现,并首次提供了胎儿心脏中嗜铬细胞的空间分布图谱。本研究借助一个开放获取的、以空间为中心的交互式查看器,为探索人类心脏发育的细胞和分子蓝图提供了一个独特的资源,并有助于揭示心脏病的遗传病因。
+ + + + +



 English
English


