文献解读|Cell Rep Med(10.6):蛋白质基因组学特征分析揭示了晚期分化型甲状腺癌的临床相关亚型
✦ +
+
论文ID
原名:Proteogenomic characterization delineates clinically relevant subtypes of advanced differentiated thyroid cancer
译名:蛋白质基因组学特征分析揭示了晚期分化型甲状腺癌的临床相关亚型
期刊:Cell Reports Medicine
影响因子:10.6
发表时间:2026. 03.06
DOI号:10.1016/j.xcrm.2026.102661
背 景
甲状腺癌的全球发病率迅速上升,每年全球约有60万例新发病例。其中,超过50万例(占95%以上)为分化型甲状腺癌(DTC),包括乳头状甲状腺癌(PTC)、滤泡状甲状腺癌(FTC)及其病理变异型。虽然DTC的总体预后良好,但仍有部分患者不幸进展至晚期,出现局部晚期或转移性疾病。与早期患者相比,这些患者的治疗选择有限,预后明显较差,给社会、家庭和个人带来沉重负担。这凸显了更好地了解治疗脆弱性背后的分子异质性的迫切需求,而这对于制定最佳治疗方案或合理组合至关重要。
实验设计
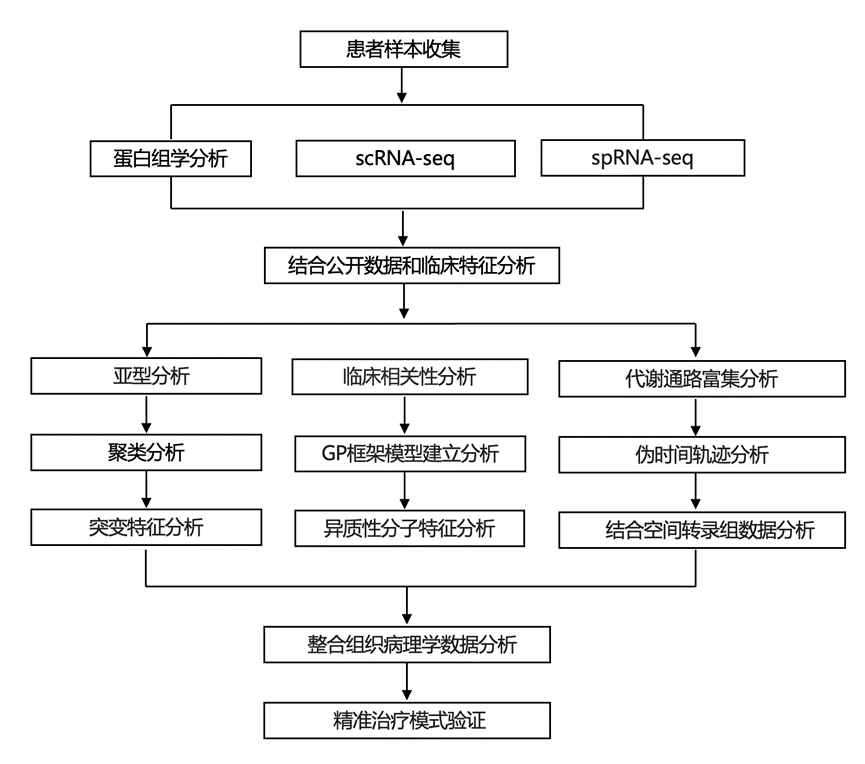
结 果
01
基于蛋白质组学的晚期分化型甲状腺癌分子亚型
研究团队收集了113例晚期DTC患者的手术切除肿瘤组织,所有患者术后均接受了放射性碘(RAI)治疗。对所有样本进行全基因组蛋白质组学分析,以表征蛋白质水平的分子异质性;同时采进行二代测序(NGS),以鉴定驱动基因突变和融合(图1)。为了建立晚期DTC的分子分型,他们对113例患者的蛋白质组学数据进行了聚类分析(CC),生成聚类结果。然后,他们确定了最佳聚类数。基于对 k = 2 至 k = 5 的分析,累积分布函数曲线下面积在 k = 3 和 k = 4 时显著增加,且 k = 3 的聚类边界比 k = 4 的更清晰。此外,与 k = 4 相比,k = 3 时模糊聚类对的比例更低,并且在基于蒙特卡罗参考的共识聚类分析的相对聚类稳定性指数 1 图中,k = 3 处出现拐点,这支持了选择 k = 3 作为最佳聚类数。结果产生了三种 CC 亚型(CC1、CC2 和 CC3),分别包括 43 例(38.1%)、40 例(35.4%)和 30 例(26.5%)患者(图 2 A)。
随后,他们分析了CC亚型的组织病理学和基因组特征。虽然RAS突变患者数量较少,但CC1亚型中RAS突变的发生率高于CC2亚型。这一发现与CC1亚型中两种公认的RAS驱动组织学类型——乳头状甲状腺癌(PTC)的滤泡变异型(FV)和滤泡状甲状腺癌(FTC)——的增加相一致(图2B)。从CC1到CC3,BRAFV600E和TERT启动子突变的频率逐渐增加,尤其以二者共存最为显著(图2C)。这种分子特征与RAIR和不良预后密切相关,这在本研究的数据和既往研究中均得到了证实(图2D)。TP53突变是DTC去分化过程中的晚期基因改变,主要见于低分化和未分化型甲状腺癌,较少见于高分化滤泡细胞来源的甲状腺癌。本研究队列中TP53突变的发生率为7.1%(8/113),与既往研究的结果相似。尽管TP53突变的分布在三个亚型之间没有显著差异,但值得注意的是,在两例病例中观察到了与 RAIR 相关的TP53/TERT共突变模式,这两例病例均属于CC3亚型。与这些基因型结果一致,CC1-CC3亚型对放射性碘(RAI)治疗的反应逐渐变差。具体而言,RAIR疾病的比例从CC1到CC3显著增加,同时生化反应和结构反应均显著下降(图2E-F)。因此,RAI治疗后的无进展生存期(PFS)在不同亚型间存在显著差异(图2 G)。
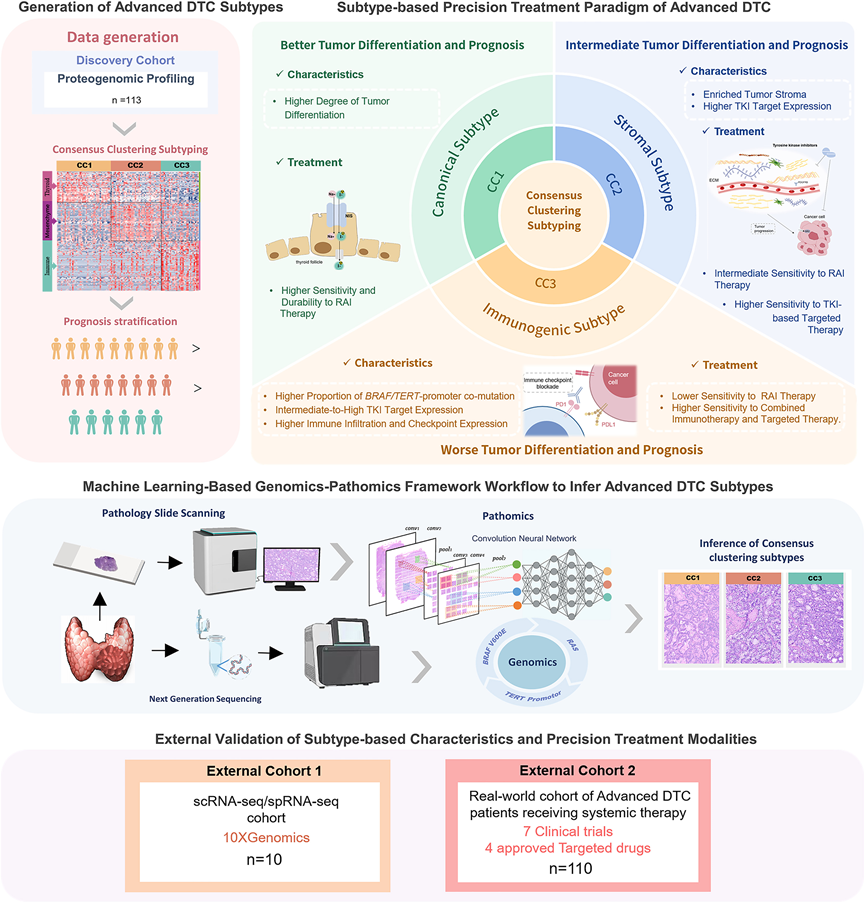
图1. 研究概览示意图。
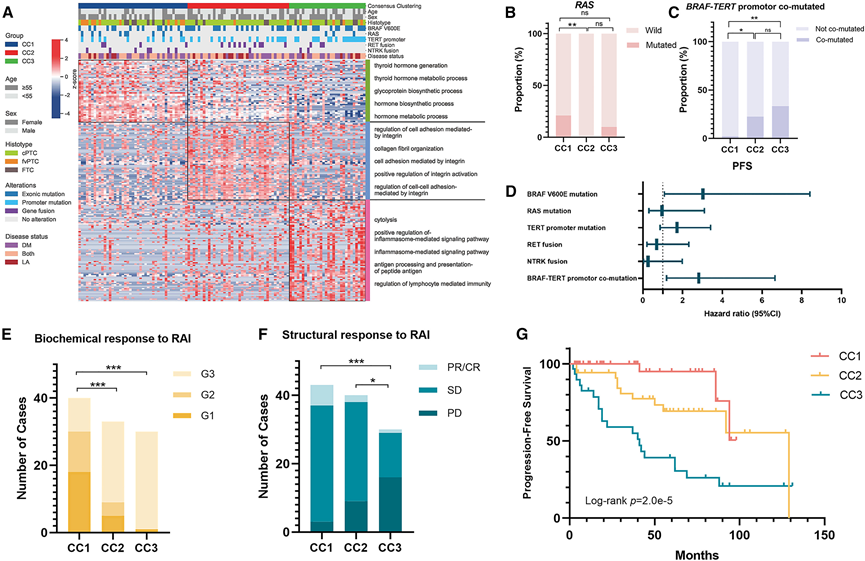
图2. 晚期分化型甲状腺癌的蛋白质组学亚型及其基因组和临床相关性。
(A) 热图显示了全球蛋白质组数据的 CC亚型。(B) 柱状图比较发现队列中各 CC 亚型RAS突变的比例。(C) 柱状图比较发现队列中CC 亚型中BRAF-TERT启动子共突变的比例。(D) 森林图总结了 Discovery 队列中不同基因改变状态的 RAI 后 PFS 的多变量 Cox 比例风险模型中的风险比和 95% 置信区间 (CI) ,并根据病理亚型进行了调整。(E) 柱状图比较了发现队列中三种CC亚型对RAI治疗的生化反应。(F) 柱状图比较了发现队列中不同CC亚型对RAI的结构反应。(G) 探索队列中不同CC亚型接受RAI治疗后的PFS的Kaplan-Meier生存曲线。
02
适用于临床的基因组学-病理学框架,用于推断CC亚型
由于基于质谱的蛋白质组学分析成本高昂、分析周期长且技术要求复杂,因此该蛋白质组学分类的直接临床应用面临诸多挑战。为了克服这些局限性并提高分子分类的临床适用性,他们开发了一种快速、经济且便捷的工作流程,该流程利用了两种易于获取的临床数据:(1) 数字病理全切片图像 (WSI) 和 (2) 来自基于 NGS 的基因检测panel的基因突变数据,从而能够对三种蛋白质组学 CC 亚型进行稳健的预测。探究了三种甲状腺癌亚型的肿瘤是否表现出不同的病理模式,以及卷积神经网络(CNN)模型能否通过数字病理分析区分它们。他们利用全部113例入组患者的WSI,构建了一个深度学习流程,用于训练CNN模型以对三种甲状腺癌亚型进行分类。然后,他们将三种最常见的致病基因改变(BRAFV600E突变、RAS突变和TERT启动子突变)与基于CNN的病理组学模型相结合,并使用随机森林算法在遗传规划(GP)框架内构建了一个分类器(图3A)。交叉验证结果表明,该GP框架对所有三种亚型均具有较强的预测性能,CC1、CC2和CC3的曲线下面积(AUC)值分别为0.754、0.804和0.895,显著优于仅使用基因组或病理组学数据的模型(图3B)。
利用本研究开发的GP框架,他们回顾性地分析了三种GP推断的CC亚型的病理特征是否与其蛋白质组学特征相符,并通过可视化代表性图像块进行验证。各CC亚型对应的图像块的形态学特征如下:CC1显示部分保留的甲状腺形态;CC2显示丰富的肿瘤间质;CC3显示免疫细胞浸润增多(图3C)。总而言之,这些发现揭示了CC亚型之间不同的病理模式,反映了晚期DTC的异质性分子特征。
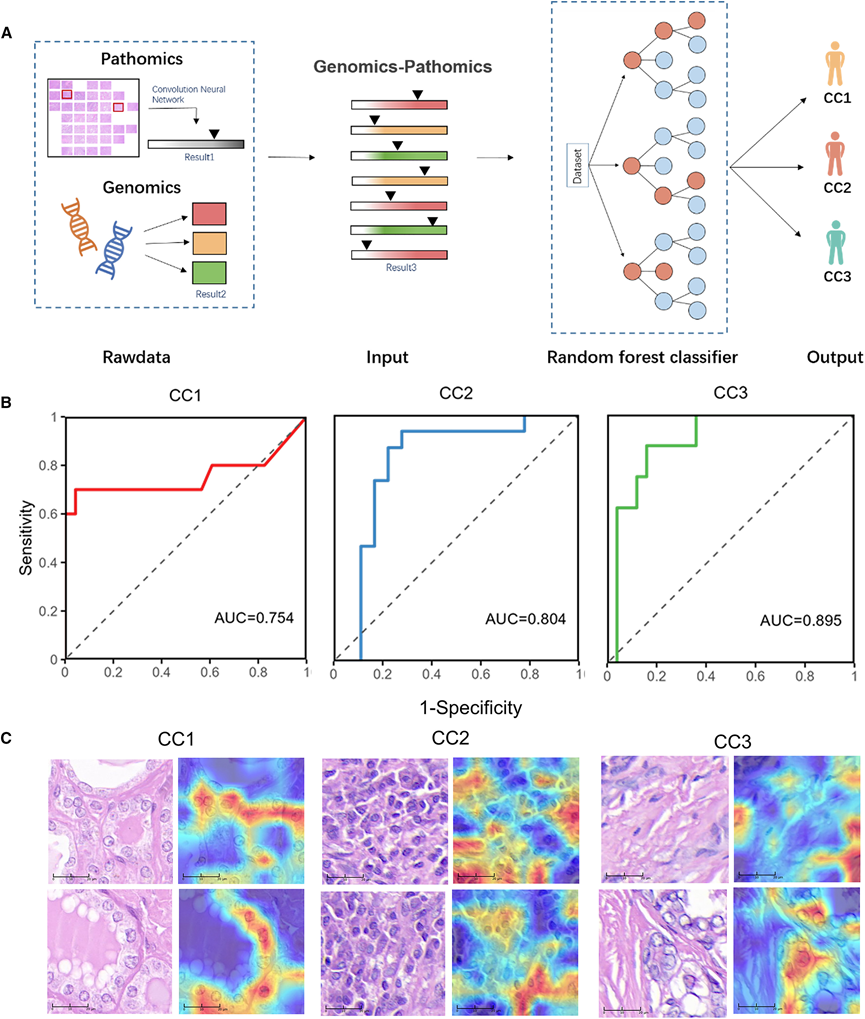
图3. 构建 GP 框架以推断晚期 DTC 的 CC 亚型。
(A) 示意图,说明 GP 集成框架的开发,以推断高级 DTC 的 CC 子类型。(B) 推断具有稳健区分性的晚期 DTC CC 亚型的受试者工作特征曲线。(C) 代表性图像图,取自预测得分最高的各CC亚型病例。
03
CC1亚型对应于分化程度较高的典型肿瘤
接下来,他们深入研究了各亚型的内在分子机制。他们发现CC1亚型中甲状腺激素合成和代谢相关通路显著富集,提示CC1肿瘤可能总体上保留了更多正常甲状腺滤泡细胞的功能。为了分析分化程度,他们计算了各亚型的甲状腺分化评分(TDS)。结果显示,CC1肿瘤的TDS评分显著高于CC3亚型(图4A),尤其体现在与甲状腺激素合成密切相关的两种蛋白——甲状腺球蛋白(TG)和甲状腺过氧化物酶(TPO)的表达水平升高(图4B-D)。此外,CC1 肿瘤中MAPK和PI3K/AKT/mTOR 通路中的大多数关键蛋白均下调,同时细胞周期和细胞增殖相关蛋白的水平也降低(图4E-F)。
接下来,他们使用包含10例晚期分化型甲状腺癌(DTC)肿瘤的单细胞转录组分析(scRNA-seq)队列进行验证,其中4例还进行了空间转录组测序(spRNA-seq)分析(scRNA/spRNA-seq队列,外部队列1)。总共分析了来自10个肿瘤的95578个细胞,并鉴定出7个不同的主要细胞聚类,包括甲状腺细胞(也称为甲状腺滤泡细胞)、B细胞、T细胞、巨噬细胞、肥大细胞、内皮细胞和成纤维细胞(图4G)。细胞类型的分配基于表达谱聚类、拷贝数变异推断和经典标记注释的一致性。GP框架推断,该scRNA/spRNA-seq队列中的2例、4例和4例患者分别分类为CC1、CC2和CC3亚型。在本队列中,CC1 肿瘤中甲状腺细胞的比例高于其他两个亚型(图 4H)。他们使用先前开发的甲状腺细胞恶性肿瘤分类器对scRNA-seq数据进行分类,成功区分了恶性甲状腺细胞和良性甲状腺细胞。在 scRNA-seq 数据中,他们观察到 CC1 恶性甲状腺细胞的 TDS 评分高于其他两个亚型中的相应细胞(图4I-J),这一结果也得到了本队列中四例患者的 spRNA-seq 分析的进一步支持(图 4K)。此外,对恶性甲状腺细胞的拟时序分析进一步表明,CC1肿瘤细胞倾向于位于肿瘤演化动力学的起始点(图4L-M)。这些发现也与临床数据相符,即该队列中的两例CC1患者均表现出对RAI治疗的强烈适应性(图4N)。
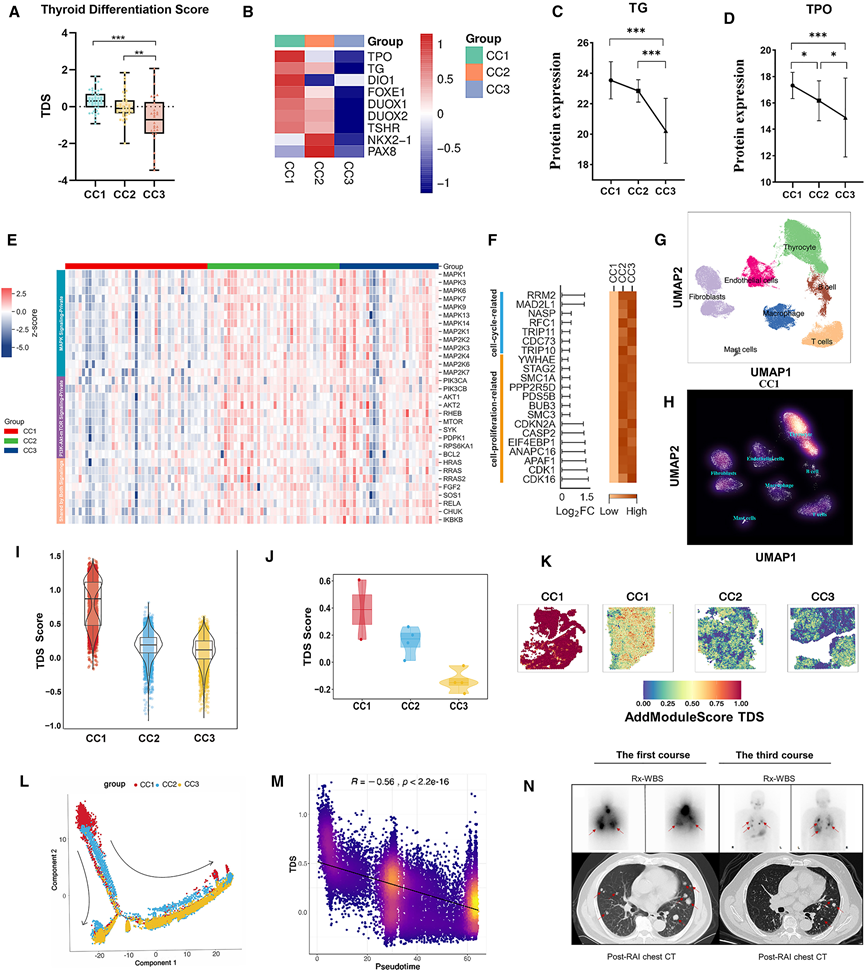
图4. 箱线图比较发现队列中不同 CC 亚型的 TDS。
(A) 热图显示了发现队列( n = 113)中与 TDS 相关的基因的蛋白质组表达水平。(B) 热图显示了发现队列( n = 113)中与 TDS 相关的基因的蛋白质组表达水平。(C-D) 折线图比较了发现队列中三种 CC 亚型甲状腺分化标志物 TG和 TPO的蛋白表达。(E) 热图显示发现队列中 MAPK 通路和/或 PI3K/Akt/mTOR 通路中关键蛋白质的丰度。(F) 热图显示发现队列中三种 CC 亚型中细胞周期相关蛋白和细胞增殖相关蛋白的差异蛋白丰度。(G) 对 scRNA/spRNA-seq 队列(外部队列 1)中 10 个晚期 DTC 样本的 95578 个细胞进行均匀流形近似和投影 (UMAP) 可视化。(H) 密度图可视化展示了外部队列 1中两个 CC1 样本中七种主要细胞类型的丰度。(I) 小提琴图比较外部队列 1中不同 CC 亚型恶性甲状腺细胞的 TDS 评分。(J) 小提琴图比较了来自外部队列 1 中四名患者的 spRNA-seq 数据的 TDS 评分。(K) 利用来自外部队列 1 中四名患者的 spRNA-seq 数据,对 TDS 评分进行空间转录组学映射。(L) 外部队列 1 中 10 个晚期 DTC 样本的恶性甲状腺细胞的伪时间轨迹,按 CC 亚型着色。 (M) 散点图显示,外部队列 1 中所有恶性甲状腺细胞的 TDS 评分与轨迹分析推断出的伪时间值之间存在显著的负相关性。(N) 对外部队列1中CC1型肿瘤的代表性患者(P1)进行放射性碘治疗(RAI)后,分别在第一次和第三次RAI治疗后进行全身扫描(Rx-WBS)和胸部CT扫描。
04
CC2亚型对应于基质丰富的肿瘤
整合素相关通路在CC2亚型中显著富集,提示CC2肿瘤中存在丰富的细胞外基质-肿瘤细胞相互作用。他们进一步研究了三种亚型的蛋白质表达模式,发现多种基质蛋白在CC2亚型中表达上调,包括胶原蛋白、整合素、层粘连蛋白和血小板反应蛋白(图5A)。此外,已知的抗血管生成mTKI靶点——PDGFRB(血小板衍生生长因子受体β)、SRC和FGF(成纤维细胞生长因子)受体2——在CC2亚型中表达上调,在CC3亚型中表达处于中间水平(图5B)。
接下来,他们对scRNA/spRNA-seq队列(外部队列1)中的CC2亚型进行了表征。在单细胞分辨率下,与其他亚型相比,CC2肿瘤显示出更高的基质评分和更丰富的成纤维细胞浸润(图5C-E),其特征性靶基因PDGFRB主要表达于该亚型的成纤维细胞上(图5F)。与这些发现一致,代表性CC2肿瘤的空间转录组图谱显示基质丰度增加(图5G)。此外,表达PDGFRB的区域与这些基质丰富的区域存在显著的空间重叠(图5G)。临床上,该队列中一名CC2肿瘤的代表性男性患者接受了三个疗程的RAI治疗。虽然病灶仍对I131具有亲和力,但他的肺转移灶始终未见缓解。这一发现与在探索队列中观察到的 RAI 对 CC2 肿瘤的次优治疗效果相呼应(图2E-G),促使他们探索抗血管生成靶向疗法(特别是靶向 PDGFR 的疗法),无论是与 RAI 联合使用还是作为二线疗法,以进行该亚型的精准治疗。
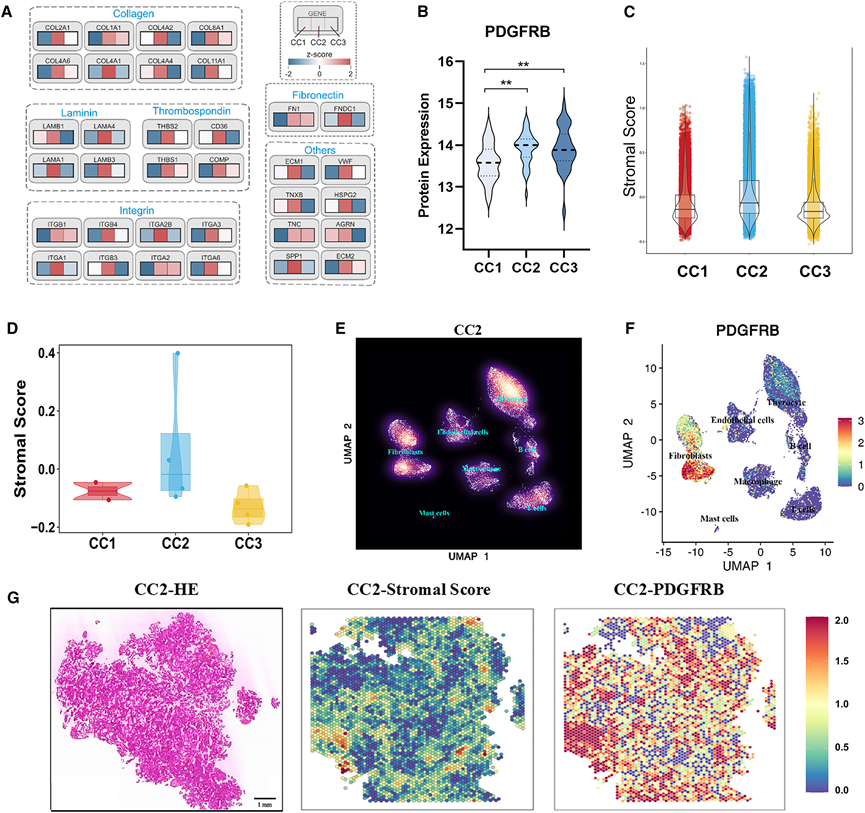
图5. 基质CC2亚型显示肿瘤基质富集和mTKI靶点表达升高。
(A) 发现队列中 CC 亚型中特征蛋白家族(包括胶原蛋白、层粘连蛋白、血小板反应蛋白、整合素、纤连蛋白等)的丰度。(B) 小提琴图比较了发现队列中不同CC亚型中PDGFRB蛋白的表达情况。(C) 小提琴图比较了外部队列 1(n = 10)中 scRNA-seq 数据在单细胞水平上不同 CC 亚型的基质评分。 (D) 小提琴图比较了外部队列 1中单细胞 RNA 测序数据在样本水平(伪体积)上不同 CC 亚型的基质评分。(E) 密度图可视化展示了外部队列 1 中四个 CC2 样本中七种主要细胞类型的丰度。(F) UMAP 可视化图显示了外部队列 1 中四个 CC2 样本的七种主要细胞类型中 PDGFRB 基因的表达。(G) 代表性CC2肿瘤(P3)的H&E染色切片(左图)和基质评分(通过ESTIMATE算法计算,中图)和PDGFRB基因表达(右图)的空间转录组学图谱。
05
CC3亚型以更强的免疫原性表型为特征
CC3 亚型表现出免疫相关通路显著富集。他们对蛋白质组学队列中的全部 113 例患者进行了免疫组织化学 (IHC) 染色。结果显示,与非 CC3 亚型相比,CC3 肿瘤中CD4+和CD8+T细胞浸润显著升高,同时免疫检查点蛋白 PD-L1 的表达也显著升高(图6A-B)。这些观察结果表明,CC3 亚型可能比其他亚型具有更高的免疫原性,提示其可能对免疫治疗更敏感。
他们对scRNA/spRNA-seq队列(外部队列1)中的CC3肿瘤进行了表征。在单细胞分辨率下,CC3肿瘤细胞定位于伪时间轨迹图的末端,并且该亚型中的恶性甲状腺细胞在单细胞水平上表现出最低的TDS评分,这与其在整体数据中分化程度低的结果一致(图4I-L)。CC3肿瘤表现出T细胞和巨噬细胞浸润增强,这与其相对于其他两个亚型的最高免疫评分相符(图6C)。与其他两个亚型不同,CC3肿瘤在肿瘤细胞和巨噬细胞上主要表达PD-L1。T细胞上PD-L1和PD-1之间的相互作用为探索免疫检查点阻断疗法提供了理论依据(图6D)。CC3肿瘤的空间转录组谱分析证实了上述观察结果(图6E-F)。他们回顾了该队列中所有四例CC3患者的临床资料,发现所有患者均患有难治性RAIR疾病。其中一例患者因颈部病灶复发接受了六次颈部手术(图6G)。其余三例患者均表现为广泛的原发肿瘤侵犯,分别累及皮肤、下咽和喉腔(图6H)。他们对后两例患者的原发肿瘤进行IHC和多重免疫荧光染色,结果显示肿瘤细胞PD-L1表达阳性,且肿瘤微环境(TME)中CD8+ T细胞和巨噬细胞(CD68 +)大量浸润(图6I-J)。这些临床发现与上述计算机模拟结果完全吻合。
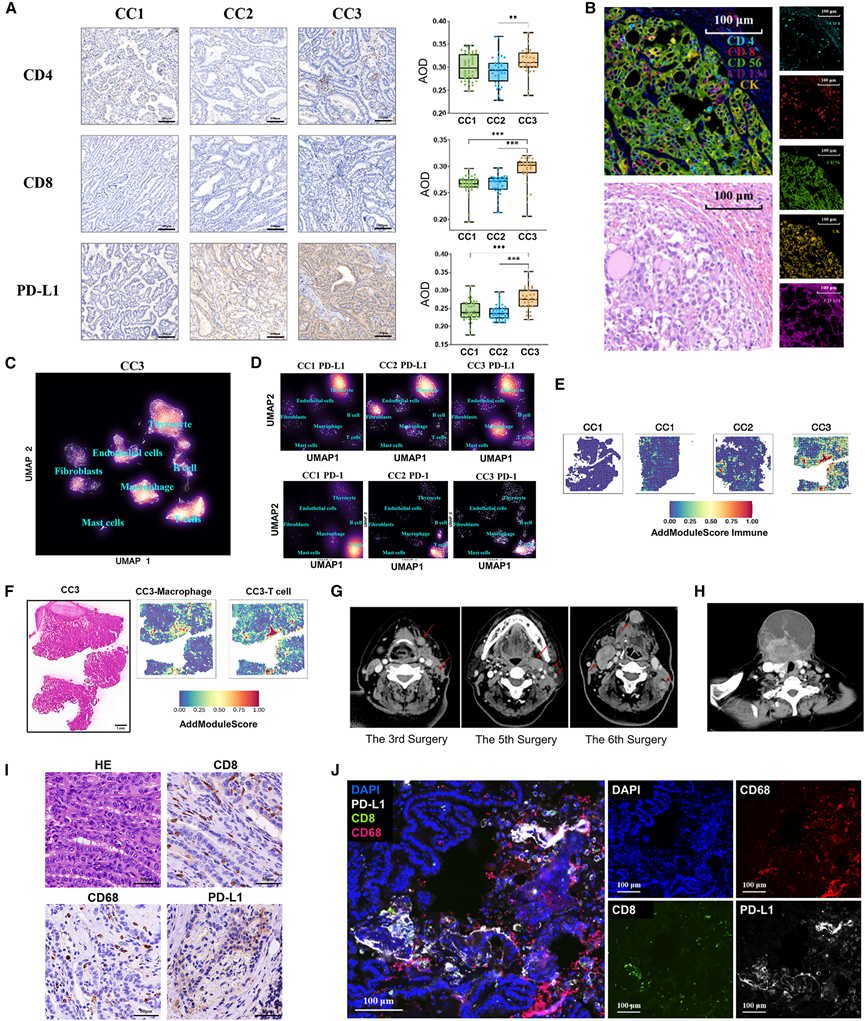
图6. 免疫原性 CC3 肿瘤亚型体现了免疫炎症肿瘤的典型特征,其特点是免疫抑制性肿瘤微环境 (TME) 和高度侵袭性行为。
(A) 各CC亚型CD4、CD8和PD-L1的代表性IHC染色切片(左图)。箱线图比较了发现队列所有病例IHC染色中CD4 +T细胞(右上)、CD8+T细胞(右中)和PD-L1表达(右下)的丰度。(B) 来自探索队列中一名广泛侵袭性滤泡性甲状腺癌(FTC)患者的代表性CC3肿瘤的多重免疫荧光染色。(C) 密度图可视化展示了外部队列 1 中四个 CC3 样本中七种主要细胞类型的丰度。(D) 密度图可视化展示了外部队列 1(n = 10)中 CC 亚型样本中 PD-L1 和 PD-1 的单细胞表达谱。(E) 利用来自外部队列 1 中四名患者的 spRNA-seq 数据,对免疫评分进行空间转录组学映射:两名患有 CC1 肿瘤(P1、P2),一名患有 CC2 肿瘤(P3),一名患有 CC3 肿瘤(P9)。(F) H&E 染色切片(左,比例尺,1mm)和基因表达谱的空间转录组学映射,推断代表性 CC3 肿瘤(P9)中巨噬细胞(中)和 T 细胞(右)的分布。(G)来自外部队列 1 的代表性 CC3 肿瘤患者(P8)的第三次、第五次和第六次颈部手术的术前增强颈部 CT 图像。(H) 来自外部队列 1 的代表性 CC3 患者(P10)的原发肿瘤的 CT 图像。(I) 来自外部队列 1 中代表性 CC3 肿瘤患者(P9)的 H&E 染色和 CD8、CD68 和 PD-L1 IHC 图像。(J) 来自外部队列 1 的代表性 CC3 肿瘤患者(P7)的多重免疫荧光染色显示。
06
基于亚型的精准治疗模式
鉴于三种分子亚型的内在生物学特征,他们提出了一种基于亚型的晚期分化型甲状腺癌(DTC)精准治疗方案。首先,CC1亚型对RAI治疗可获得良好且持久的疗效,因此RAI单药治疗通常足以满足CC1肿瘤患者的治疗需求。其次,CC2亚型对RAI治疗的反应中等,但其抗血管生成mTKI靶点PDGFR的表达水平较高。因此,对于CC2亚型肿瘤患者,可考虑将RAI作为一线治疗,并在RAI耐药后采用抗血管生成靶向治疗(即mTKI)作为二线治疗。第三,CC3亚型对RAI治疗的反应相对较差,且具有最强的免疫原性,抗血管生成mTKI靶点的表达水平也中等。因此,对于RAI治疗失败的CC3亚型患者,联合免疫治疗和靶向治疗可能是一种潜在的治疗方案(图1)。
为了评估他们提出的治疗模式的潜在临床意义,他们建立了一个包含110例接受全身治疗的晚期DTC患者的大型队列,该队列整合了来自四种已获批准疗法和七项临床试验的真实世界数据(外部队列2)(图7A)。对于该队列,他们收集了所有患者在接受全身治疗前的穿刺活检或手术样本,并根据GP框架确定其CC亚型。正如预期的那样,该队列中CC1肿瘤的比例显著低于发现队列,而CC3肿瘤的比例则更高(50.0% vs. 26.5%)(图7B)。这可以解释为,全身治疗(靶向治疗和/或免疫治疗)是晚期DTC在RAI后的二线或后续治疗。与CC3肿瘤不同,对RAI亲和力高的CC1肿瘤很少进展到需要此类治疗的阶段,而CC3肿瘤通常需要二线或探索性治疗。因此,队列组成的这种差异进一步证实了分型系统的生物学有效性。
来自该队列的真实世界治疗数据验证了基于亚型的精准治疗模式。在接受抗血管生成mTKI靶向治疗的患者中,CC2型肿瘤患者的疗效最佳(客观缓解率[ORR]:50%;疾病控制率[DCR]:86.1%),其次是CC3型(ORR:37.5%;DCR:79.2%),而CC1型疗效最差(ORR:25%,DCR:50%)。相反,在接受 mTKI 靶向治疗和抗 PD-1 免疫治疗的患者中,CC3 亚型表现出更优的疗效,ORR 为 56.5%,DCR 为 95.6%,其次是 CC2(ORR:42.1%,DCR:78.9%),而 CC1 的疗效再次最差(ORR:25%,DCR:50%)(图7C-G)。
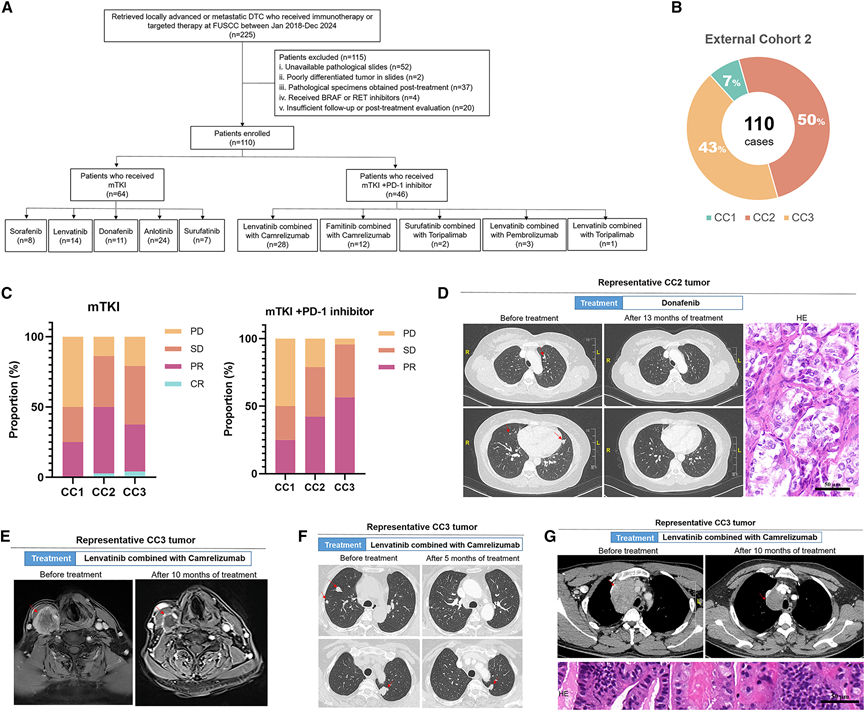
图7. 建立接受系统性治疗的真实世界治疗队列(外部队列 2)并验证提出的基于亚型的精准治疗模式。
(A) 外部队列 2 的选择过程。(B) 饼图显示了外部队列 2中 CC 亚型的分布。(C) 条形图比较了外部队列 2(n = 110)中 CC 亚型患者单独使用 mTKI 或使用 mTKI + PD-1 抑制剂组合的治疗效果,根据 RECIST v.1.1 标准进行评估。(D) 外部队列 2 中代表性 CC2 肿瘤的胸部 CT。(E) 外部队列 2 中代表性 CC3 肿瘤的颈部磁共振成像。(F) 外部队列 2 中代表性 CC3 肿瘤的胸部 CT。(G) 外部队列 2 中代表性 CC3 肿瘤的胸部增强 CT。
+ + + + + + + + + + +
结 论
本研究对 113 例晚期 DTC 进行了蛋白质组学分析,识别出三种分子特征不同的亚型:经典型、基质型和免疫原型。这些亚型在驱动基因突变、组织病理学特征和临床结局方面存在差异。基于其独特的生物学特性,本研究针对每种亚型提出了不同的治疗策略。为了便于临床应用,本研究开发了一种机器学习分类器,该分类器利用常规可用的基因突变和数字病理数据能够准确预测这些亚型。通过单细胞和空间转录组学分析,在一个独立的队列中进一步证实了该分类的生物学意义。此外,对接受各种全身治疗的真实世界患者队列的分析也提供了初步的临床证据,支持该亚型分类框架在指导治疗决策方面的潜在应用价值。总而言之,本研究为未来探索晚期 DTC 的个体化治疗提供了理论依据和实用工具。
+ + + + +



 English
English


