文献解读|Nat Commun(15.7):在单细胞分辨率下鉴定非小细胞肺癌脑转移中免疫微环境的改变及其与免疫检查点抑制剂疗效不佳的关联
✦ +
+
论文ID
原名:Identification of altered immune landscape at single-cell resolution in NSCLC brain metastasis and its association with poor immune checkpoint inhibitor responses
译名:在单细胞分辨率下鉴定非小细胞肺癌脑转移中免疫微环境的改变及其与免疫检查点抑制剂疗效不佳的关联
期刊:Nature Communications
影响因子:15.7
发表时间:2026.03.10
DOI号:10.1038/s41467-026-70715-6
背 景
非小细胞肺癌(NSCLC)是全球癌症相关死亡的主要原因。脑转移(BM)在晚期NSCLC患者中很常见。由于血脑屏障(BBB)的保护作用,全身治疗(如化疗)的疗效有限,因此脑转移患者的治疗选择也较为有限。靶向PD-1/PD-L1轴的免疫检查点抑制剂(ICI)免疫疗法已成为晚期NSCLC的一线标准治疗方案。该疗法在治疗脑转移方面显示出一定的潜力。然而,许多患者对该疗法无反应,且原发肿瘤和脑转移灶的疗效差异也较为常见。这表明原发灶和转移灶之间的肿瘤免疫微环境(TIME)存在显著的异质性。NSCLC会导致预后不良并降低免疫ICI的疗效。然而,导致ICI疗效降低的机制尚不清楚。
实验设计
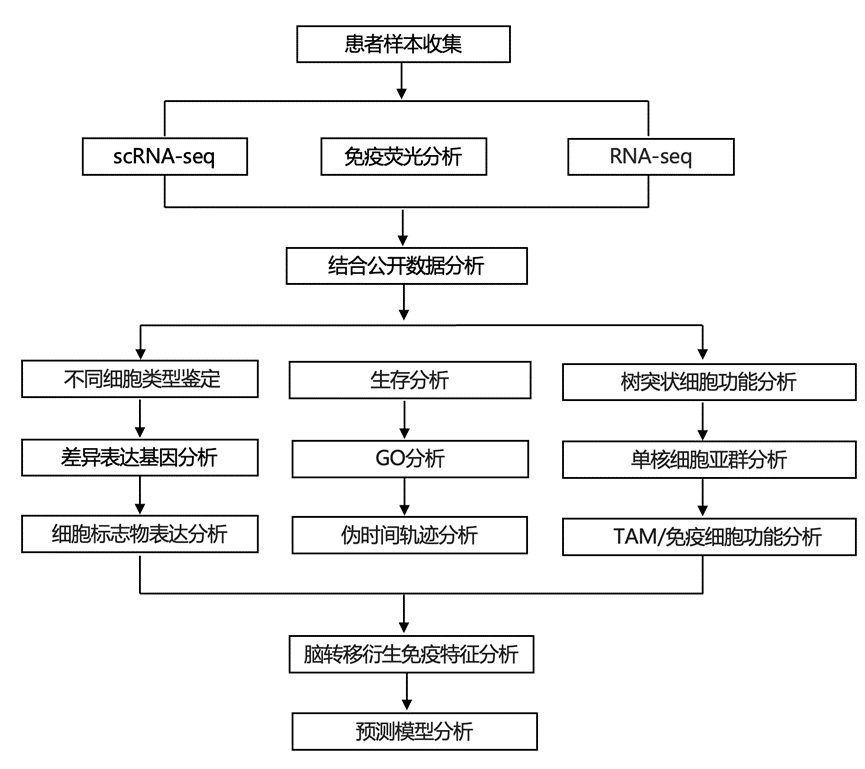
结 果
01
单细胞转录组分析揭示了原发性和脑转移性非小细胞肺癌中不同的免疫图谱
为了研究非小细胞肺癌(NSCLC)中原发灶(PT)和BM免疫微环境的差异,研究团队利用荧光激活细胞分选(FACS)技术从这两个部位分离出活的、免疫相关的(CD45+)细胞,并对其进行单细胞转录组分析(scRNA-seq)(图 1A)。此外,他们还整合了既往研究中的scRNA-seq数据,选取了包含超过2000个细胞的BM样本。这些样本共同构成了本研究的发现队列,共包含19个样本(8个PT样本和11个BM样本)。经过严格的质量控制和双细胞去除后,最终数据集包含117752个细胞,平均每个细胞包含1532个基因和5519个独特的分子标识符(UMI)。
他们利用基于基因表达谱的无监督聚类方法,鉴定出七种主要细胞类型,这些细胞类型具有谱系特异性标记:15019个上皮细胞(EPCAM、CDH1)、774个癌相关成纤维细胞(COL1A2、SPARC)、70895个T细胞和自然杀伤(NK)细胞(CD2、CD3D)、7097个B细胞(CD19、MS4A1)、3484个浆细胞(MZB1、IGHG3)、2798个肥大细胞(KIT、CPA3)以及17685个髓系细胞(LYZ、ITGAX)(图1B-F)。上皮细胞和癌相关成纤维细胞的数据来自之前的研究,因此未纳入后续分析。
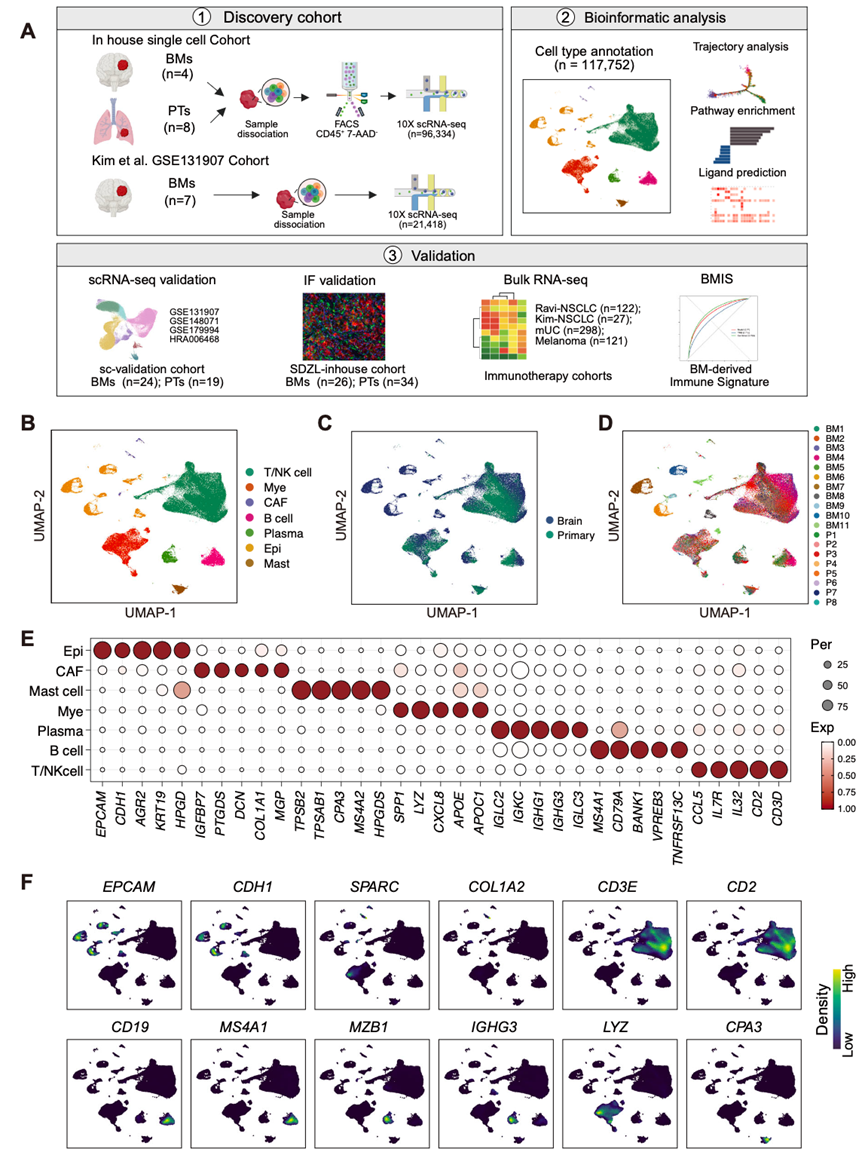
图1. PT 和 BM NSCLC 样本的scRNA-seq 谱。
(A) 研究设计示意图。(B-D) UMAP 图,按细胞类型、样本来源(原发性或脑转移)和单个样本着色。(E) 散点图显示所示细胞类型中标记基因的表达水平。(F) 显示用于细胞类型鉴定的标记基因表达的UMAP图。
02
BM中富集的HSP70高表达T细胞与非小细胞肺癌免疫治疗效果不佳相关
鉴于肿瘤浸润淋巴细胞在TME中发挥的关键作用及其对患者预后的影响,他们首先评估了T细胞群,比较了来自PT和BM的CD4+和CD8+ T细胞的转录谱,以研究BM中T细胞独特的转录状态。热休克蛋白HSPA1A和HSPA1B是BM中CD4⁺和CD8⁺ T细胞中表达上调最显著的基因之一(图 2A)。为了确定这种上调是否延伸到其他HSP70家族成员,他们检测了其他亚型(HSPA5、HSPA8、HSPA9等)的表达。然而,这些亚型在PT和BM之间未显示出显著差异,表明观察到的上调特异性地针对可诱导的HSP70亚型HSPA1A和HSPA1B。基于HSPA1A和HSPA1B表达的HSP70模块评分的样本水平分析证实,与PT相比,BM中CD4+和CD8+T细胞的表达均显著升高 (图 2B)。基于此评分,他们将CD4+和CD8+ T细胞分为HSP70高表达组、HSP70中表达组和HSP70低表达组。scRNA-seq数据显示,BM中HSP70高表达的CD4⁺和CD8⁺ T细胞比例增加。
为了消除疾病分期可能造成的混淆效应,他们整合了公开可用的III-IV期NSCLC患者(包括PT和BM)的T细胞scRNA-seq数据,构建了一个分期匹配的验证数据集。在该分期匹配的验证队列中,T细胞中HSPA1A和HSPA1B的表达上调呈现出一致的趋势,表明HSP70表达升高可能是脑转移微环境的固有特征,而不仅仅是疾病分期差异的结果。在内部的SDZL队列中,包括未经治疗的PT(n = 34)和BM(n = 26)样本(取自手术切除或诊断性活检),多重免疫荧光染色显示BM中多种细胞类型中HSP70表达升高(图 2C)。虽然HSP70上调并非仅限于T细胞,反映了转移微环境中更广泛的应激反应,但鉴于T细胞作为效应细胞和免疫检查点阻断药物的药理学靶点发挥着核心作用,他们重点对T细胞进行了详细的定量分析。该分析显示,与PT相比,BM中HSP70⁺ CD4⁺ T细胞的比例显著更高(图2D),并且HSP70⁺ CD8⁺ T细胞的比例也呈现升高的趋势(图 2E)。当他们将 mIF 分析限制在 IV 期患者(10 例 PT 与 26 例 BM)时,BM 再次显示出 HSP70+CD4+细胞比例较高,并且 HSP70+ CD8+ T 细胞 比例有升高的趋势,而颅外 PT 则没有这种趋势,这表明这种模式在晚期疾病中仍然存在。
CD4⁺和CD8⁺ T细胞中HSPA1A或HSPA1B的高表达与增强的细胞反应状态相关,而这种状态又与免疫治疗耐药性有关。因此,他们分析了精心筛选的T细胞特征,以进一步探索HSP70高表达T细胞的功能特征(图 2F)。与HSP70低表达T细胞相比,CD4⁺和CD8⁺ HSP70高表达T细胞均表现出增强的应激反应特征和减弱的初始T细胞特征。除了这些共同特征外,HSP70高表达CD4⁺ T细胞还表现出增强的耗竭特征,而HSP70高表达CD8⁺ T细胞则表现出增强的细胞毒性特征,并伴有NF-κB信号通路的减弱。基于亚聚类特异性差异表达基因的通路富集分析表明,HSP70高表达 CD4⁺和 CD8⁺ T 细胞均显著富集了与蛋白质折叠、对拓扑错误蛋白质的反应以及分子伴侣介导的蛋白质折叠相关的生物学过程(图 2G-H),这与活跃的细胞应激反应程序一致。
为了评估 HSP70 高表达 T 细胞的临床意义,他们分析了其与两个独立的非小细胞肺癌 (NSCLC) 免疫治疗队列中患者预后的关联。在 Ravi 队列和 Kim 队列中,HSP70高表达 CD8+ T 细胞的特征评分越高,无进展生存期 (PFS) 越短 ,表明其与免疫治疗效果不佳相关(图 2I)。对于 HSP70 高表达 CD4+ T 细胞,在 Ravi 队列中,较高的特征评分同样与较差的预后相关,在 Kim 队列中也观察到了类似的趋势(图 2J)。
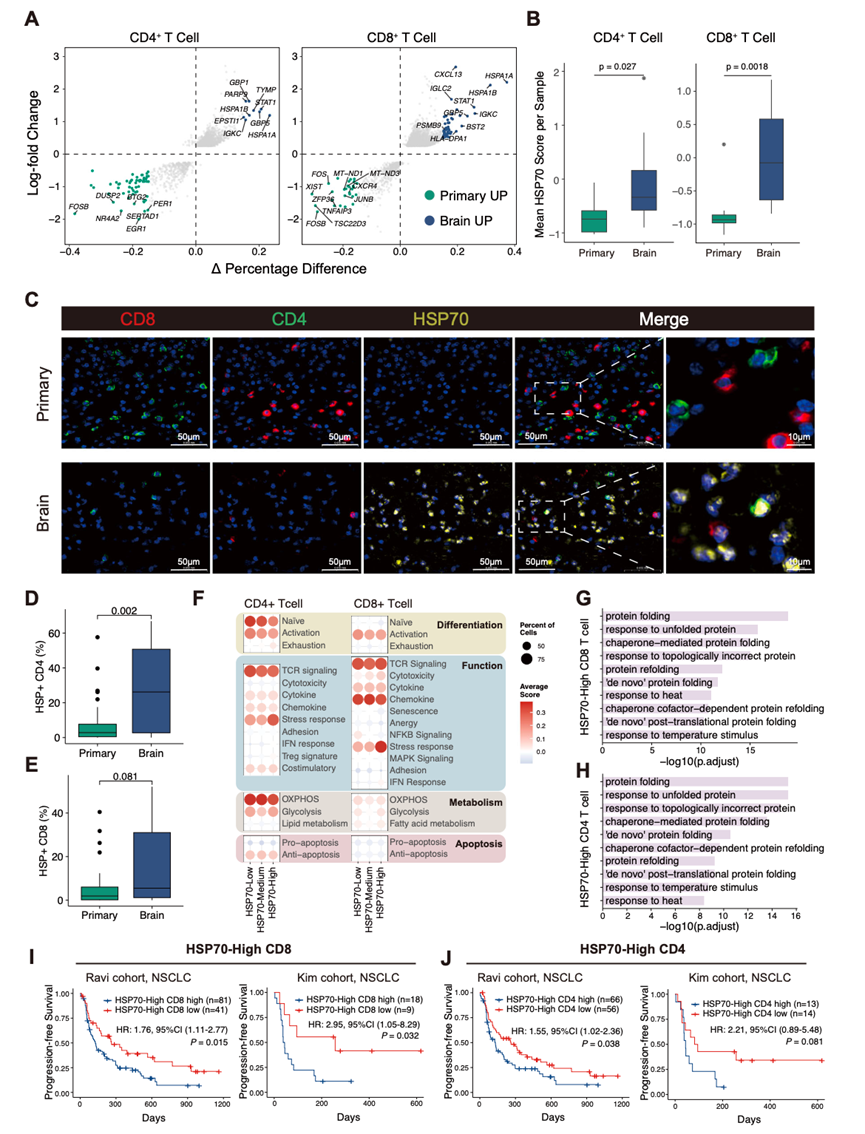
图2. T 细胞中 HSP70 表达升高与接受免疫治疗的患者预后不良相关。
(A)差异表达基因分析。(B) 箱线图比较原发性和脑转移性样本的平均HSP70评分。(C) NSCLC切片的代表性多重免疫荧光图像。(D-E) 箱线图分析了多重免疫荧光图像中的HSP70⁺ CD4⁺ T 细胞和 HSP70+ CD8+T细胞。(F) 点图展示了 HSP70 高表达、HSP70 中表达和 HSP70 低表达的 CD4+(左)和 CD8+(右)T 细胞中基因特征的平均得分。(G-H)GO分析。(I-J) Kaplan-Meier 生存曲线分析。
03
记忆性T细胞的耗竭与非小细胞肺癌的免疫治疗耐药性相关
基于转录谱和精选基因特征对PT和BM中的T/NK细胞进行进一步重新聚类,揭示了15个不同的聚类。其中包括两个NK细胞聚类——NK_FGFBP2和NK_XCL1——其特征是自然杀伤标志物高表达,以及13个T细胞聚类,其特征是CD3D⁺、CD4⁺和CD8⁺表达(图 3A-B)。
在CD4+ T细胞中,他们鉴定了七个功能不同的亚型。中央记忆样T细胞聚类(Tcm样,CD4_IL7R)表现出经典中央记忆标志物(包括CCR7、SELL、IL7R、TCF7和KLF2)的高表达,以及早期激活标志物CD69和CD40LG的高表达(图 3B)。虽然这些细胞存在于肿瘤微环境中,并因抗原刺激而发生克隆扩增(如CD69表达所示),但它们表现出与长期存活和自我更新相关的基因表达模式,类似于中央记忆T细胞。TIMP1+记忆T细胞聚类(TIMP1+ Tn,CD4_TIMP1)表现出IL7R、TIMP1、FTH1和CD40LG的高表达。富含干扰素刺激基因(ISG)的辅助性T细胞聚类(ISG+ Th,CD4_ISG)的特征是干扰素反应基因表达升高,并表现出Th1相关特征,包括CXCR3和TBX21的表达(图 3C)。应激反应T细胞聚类(Tstr,CD4_NR4A1)表现出热休克蛋白(HSPA1A、HSPA1B、HSP90AA1)表达升高,并在CD4⁺ T细胞中显示出较高的应激反应特征评分。滤泡辅助性T细胞聚类(Tfh,CD4_CXCL13)的特征是CXCL13、CTLA4、PDCD1、TOX和TIGIT的高表达,并具有较高的耗竭特征。调节性T细胞聚类(Treg,CD4_FOXP3)表达经典的Treg标志物,包括TNFRSF4、IL2RA、FOXP3和CTLA4。此外,还鉴定出一个CD4+细胞聚类(CD4_XIST)。对经典Th1/Th2/Th17谱系标志物的评估显示,虽然CD4_ISG表现出Th1相关特征,但没有细胞聚类显示出强烈的Th2(CCR4+GATA3+)或Th17(CCR6+RORC+IL17A+)极化。
在CD8+T细胞中,他们鉴定了六个功能不同的亚型。效应记忆T细胞聚类(Tem,CD8_GZMK)高表达效应分子GZMK、GZMA、KLRG1和CD44,且活化特征评分升高。组织驻留记忆T细胞聚类(Trm,CD8_ZNF683)具有特征性的驻留标志物,包括CD69、ITGAE和ZNF683,同时组织迁移标志物CCR7、SELL和S1PR1表达下调。干扰素反应T细胞聚类(Tisg,CD8_ISG)高表达干扰素刺激基因,且干扰素反应特征评分较高。增殖性T细胞聚类(CD8_Cycling)的特征是高表达增殖标志物MKI67、TOP2A和STMN1,以及代谢特征升高。耗竭T细胞聚类(Tex,CD8_HAVCR2)高表达耗竭标志物HAVCR2、LAG3、TIGIT、PDCD1和CTLA4。与既往研究结果一致,该细胞聚类也表达细胞毒性相关基因,包括CXCL13、ENTPD1和TNFRSF9,表明这些细胞是经历过抗原刺激的细胞。前体耗竭T细胞聚类(Tpex,CD8_SPRY1)处于效应T细胞和耗竭T细胞之间的中间状态,其TOX和免疫检查点抑制剂的表达相对较低,而TCF7、IL7R和CD28的表达则较高(图 3A-C)。
对 PT 和 BM 之间的这些亚群进行比较分析,结果显示存在显著差异(图 3D)。与 PT 相比,BM 中 CD4+ Tcm 样细胞 (CD4_IL7R) 和CD8⁺ Trm 细胞 (CD8_ZNF683)的比例较低。相反,BM 显示出增殖性 CD8+ T 细胞 (CD8_Cycling) 富集的趋势。鉴于队列中 PT 和 BM 之间 EGFR 突变分布不平衡,他们进行了逻辑回归分析,并对 EGFR 状态进行了校正。BM中 CD4_IL7R 和 CD8_ZNF683 的耗竭在校正后仍具有统计学意义,表明记忆性 T 细胞的耗竭在很大程度上与 EGFR 突变状态无关,CD8_ZNF683 显示出潜在的 EGFR 相关变异。在分期匹配的验证队列中,他们鉴定了 12 个主要的 T/NK 细胞聚类。与发现队列一致,他们将 CD4_IL7R 鉴定为具有高表达 IL7R 和 CD40LG 的中央记忆样 T 细胞。此外,他们发现验证队列中BM中的 CD4_IL7R 与 PT 相比显著减少。
对亚聚类特异性差异表达基因进行通路富集分析发现,CD4_IL7R 细胞富集于对细胞外刺激(包括氧水平、激素信号和机械刺激)的细胞反应通路以及淋巴细胞分化通路(图 3E)。CD8_ZNF683 细胞则表现出与淋巴细胞介导的免疫和细胞毒性相关的基因表达升高,包括 T 细胞受体信号通路、抗原受体介导的信号通路和细胞杀伤通路(图 3F)。这些结果表明,CD4_IL7R 和 CD8_ZNF683 细胞均参与主动免疫监视和抗肿瘤反应。
为了评估这些T细胞群的临床意义,他们分析了接受免疫治疗的NSCLC患者的批量RNA测序数据。在Ravi队列中,CD4_IL7R细胞丰度升高与无进展生存期(PFS)改善显著相关,在Kim队列中也呈现出类似的趋势(图 3G)。同样,在Kim队列中,CD8_ZNF683水平升高与更好的预后相关,虽然这种关联在Ravi队列中未达到统计学意义(图 3H)。相反,增殖性CD8+ T细胞(CD8_Cycling)丰度增加与两个队列的不良预后均相关。此外,他们还研究了前体耗竭T细胞聚类CD8_SPRY1(Tpex)的临床意义,该细胞聚类是PD-1抑制剂的关键靶细胞群。CD8_SPRY1细胞丰度越高,接受免疫治疗的患者预后越好,这与其作为抗肿瘤免疫反应可再生储备库的作用相符。
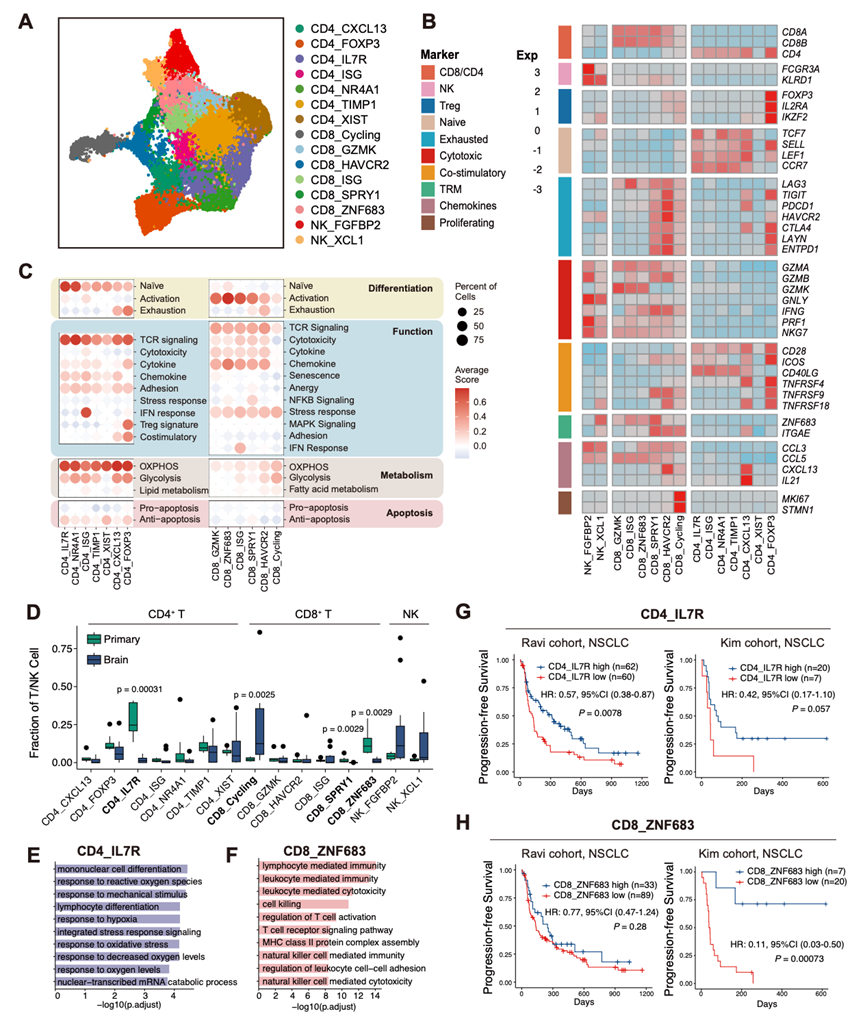
图3. PT 和 BM 样本中 T/NK 细胞的特征分析。
(A) 所有T细胞和NK细胞的UMAP图,按已鉴定的细胞聚类着色。(B) 热图展示了各细胞聚类中典型T细胞和NK细胞标志基因的标准化表达。(C) 点图显示了T细胞聚类中精选基因特征的平均得分。(D) T细胞和NK细胞亚聚类的比例。(E-F) GO分析。(G-H) Kaplan-Meier生存曲线。
04
抗炎性 cDC2 样树突状细胞分析
由于髓系细胞在肿瘤微环境(TIME)中发挥着关键的调控作用,尤其是在BM中,他们分析了该细胞谱系。无监督聚类分析揭示了12个髓系细胞亚群,包括4个肿瘤相关巨噬细胞聚类(TAM_MARCO、TAM_PLTP、TAM_SPP1和TAM_MKI67)、2个单核细胞聚类(Mono_FCN1和Mono_TIMP1)、4个树突状细胞(DC)聚类(DC_CLEC10A、DC_CLEC9A、DC_CD207和DC_LAMP3)以及1个中性粒细胞聚类(图 4A)。这些细胞聚类表现出不同的基因表达模式和转录因子谱(图 4B-C)。
对DC聚类的分析揭示了来自PT和BM的DC之间存在不同的转录谱。差异表达分析表明,PT中的DC上调了与抗原呈递和免疫激活相关的基因,而BM中的DC则上调了与代谢重编程和应激反应相关的基因。通路富集分析进一步证实了这些差异:PT中的DC富集了与抗原加工和呈递、肽抗原与MHC II类分子的组装以及适应性免疫反应相关的通路,而BM中的DC则富集了ATP代谢过程和氧化磷酸化。在四个DC聚类中,DC_CLEC9A高表达cDC1标志物(XCR1、CLEC9A、CADM1);DC_CD207和DC_CLEC10A与cDC2标志物(CD1C、FCER1A、CLEC10A)相关;DC_LAMP3 归类为活化的 DC,其特征是活化基因和共刺激基因(LAMP3、CD80、CD86)的高表达(图 4D)。
使用 Wilcoxon 秩和检验和 scCODA 对 PT 和 BM 中 DC 亚聚类比例进行比较分析,结果显示两个 cDC2 亚聚类 DC_CLEC10A 和 DC_CD207 在 PT 中显著富集(图 4E)。对亚聚类特异性差异表达基因进行通路富集分析发现,DC_CLEC10A 富集于外源性抗原的抗原呈递、MHC II 类分子介导的抗原呈递、肽抗原与 MHC II 类分子的组装以及 MHC 蛋白复合物的组装(图 4F)。类似地,DC_CD207 也富集于抗原加工和呈递、肽抗原与 MHC II 类分子的组装以及淋巴细胞介导的免疫(图 4G)。这些结果表明,两种cDC2亚群均参与原发肿瘤中的抗原呈递和T细胞活化。使用Monocle 2进行的伪时间轨迹分析揭示了DC亚群之间的发育关系(图 4H-I)。DC_CD207和DC_CLEC10A均处于发育轨迹的早期至中期位置,这与其作为能够启动T细胞的抗原呈递细胞的功能相符。
为了评估这些DC聚类的临床意义,他们分析了它们与接受免疫治疗的NSCLC患者预后的关系。DC_CLEC10A 的丰度与总生存期的改善显著相关(图 4J),而 DC_CD207 则显示出与生存期恶化相关的趋势,但未达到统计学意义。这些发现提示,NSCLC 患者PT和BM中 DC 亚群的分布模式存在差异,其中 DC_CLEC10A 代表预后良好的群体,与免疫治疗疗效增强相关。
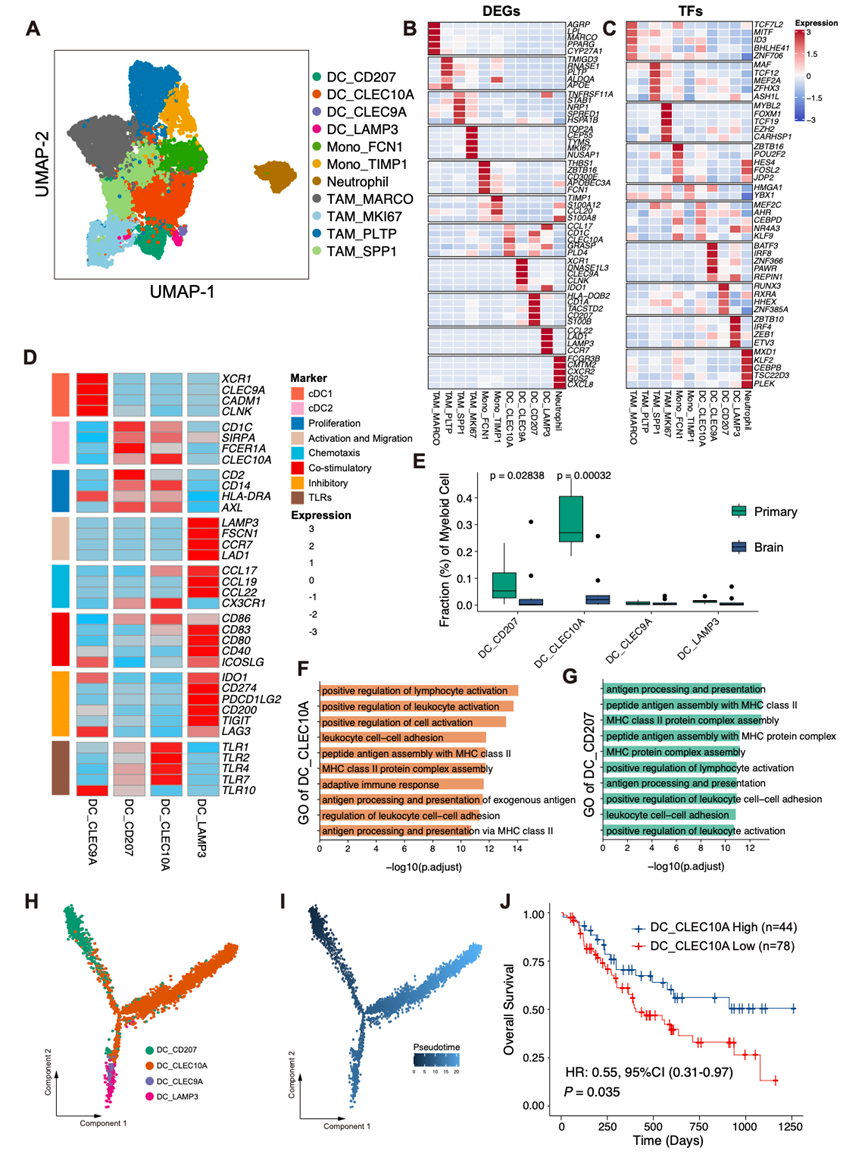
图4. 原发性非小细胞肺癌中抗炎 cDC2 样树突状细胞增多与免疫疗法疗效相关。
(A) 所有髓系细胞的UMAP图,按细胞聚类着色。(B-D) 热图显示各聚类中差异表达基因、转录因子和经典树突状细胞标记基因的标准化表达。(E) 箱线图分析DC亚聚类的比例。(F-G)GO分析。(H-I) Monocle 2推断的树突状细胞轨迹分析。(J) Kaplan-Meier 生存曲线。
05
非小细胞肺癌中不同的单核细胞亚群与免疫治疗反应存在差异性关联
他们鉴定出两个单核细胞亚群,其特征是单核细胞标志物(如FCN1、VCAN、S100A8和S100A9)表达升高(图 5A)。对PT和BM中单核细胞比例的比较分析显示,Wilcoxon秩和检验结果显示存在显著差异。scCODA成分分析考虑了细胞类型比例的相互依赖性,证实BM中Mono_FCN1的缺失是主要的成分变化(图 5B)。多重免疫荧光验证了这种分布模式,结果显示原发肿瘤中CD14⁺FCN1⁺细胞水平显著升高,脑转移瘤中CD14+TIMP1+细胞水平有升高的趋势,但未达到统计学意义(图5C-D)。在仅限于IV期疾病的亚组分析中,原发肿瘤中CD14+FCN1+细胞比例再次升高,而脑转移瘤中CD14⁺TIMP1⁺细胞比例也呈现类似的升高趋势,表明这种模式在晚期疾病中仍然存在,并且更符合组织特异性差异,而非单纯由分期驱动的差异。
利用伪批量分析进行的转录组分析揭示了这些单核细胞亚群之间存在不同的功能程序。Mono_FCN1的特征是早期转录调节因子(FOS、FOSB和NR4A2)以及免疫激活标志物(NLRP3和CD83)的表达升高,表明该亚群代表了正在经历与分化和免疫激活相关的转录重编程的活化单核细胞群。相比之下,Mono_TIMP1表现出参与免疫代谢重编程的基因(包括MIF、LDHA、ENO1、TPI1和GSTO1)的高表达,表明其处于代谢改变的状态,可能支持免疫抑制功能(图 5E)。
通路富集分析进一步证实了这些功能差异(图 5F)。Mono_FCN1富集于与皮质类固醇反应、白细胞介导的细胞毒性正向调控、慢性炎症反应以及B细胞活化调控相关的通路,这与活化的促炎表型相符。相反,Mono_TIMP1富集于核糖核苷代谢过程、ATP代谢过程和嘌呤核苷三磷酸代谢过程,突显了其代谢重编程状态。使用Monocle 2和scTour进行的轨迹分析证实,Mono_TIMP1代表幼稚型单核细胞,而Mono_FCN1代表单核细胞和巨噬细胞之间的中间状态(图 5G)。
他们分析了NSCLC患者的转录组分析(RNA-seq)数据,以评估这些单核细胞亚群的潜在临床意义。结果显示,Mono_FCN1的丰度与PFS无显著相关性(图5H),而Mono_TIMP1的高丰度与较差的预后相关(图 5I)。这些结果表明,Mono_FCN1与原发肿瘤中的激活促炎状态相关,而Mono_TIMP1在脑转移瘤中表现出代谢重编程,这可能导致免疫抑制微环境的形成,并降低免疫治疗的疗效。
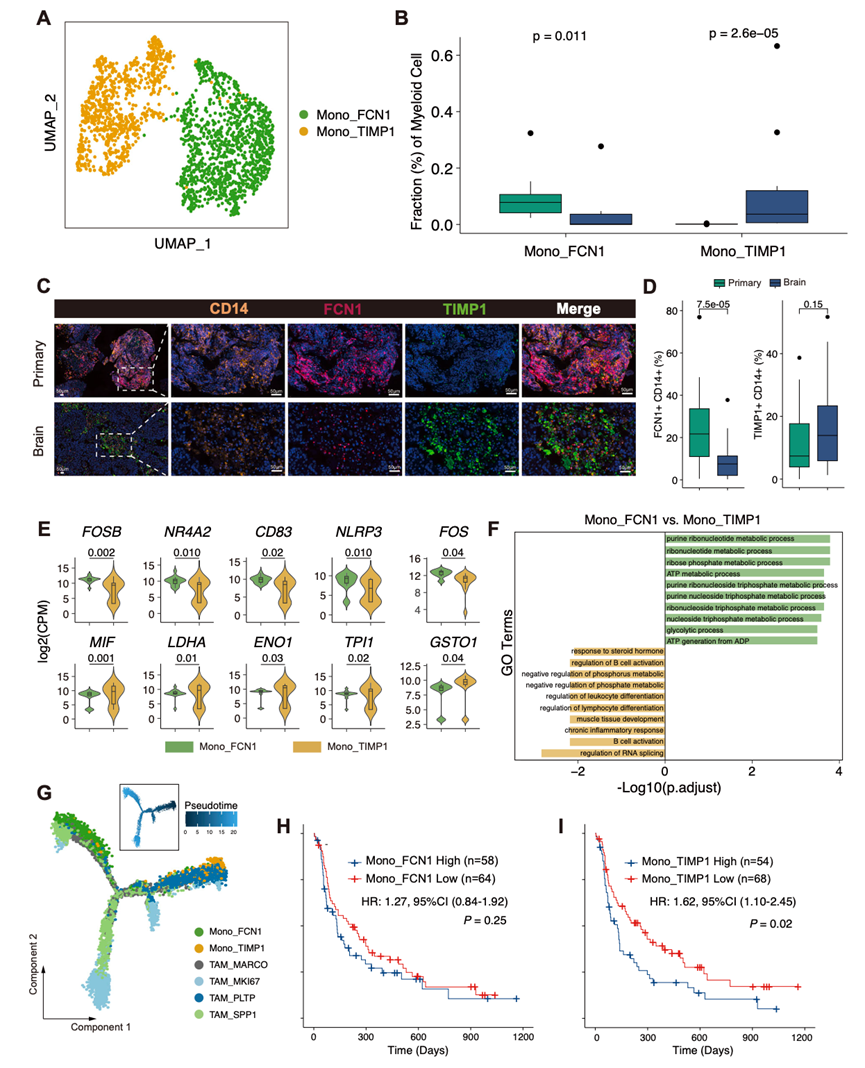
图5. BM和 PT 样本中的单核细胞表现出不同的功能,并可预测免疫治疗结果。
(A) UMAP图显示了两个单核细胞亚群。(B) 单核细胞亚群的比例。(C) 代表性的NSCLC切片多重免疫荧光图像。(D) 箱线图分析了免疫荧光图像中FCN1+CD14+和TIMP1+CD14+细胞的数量。(E) 小提琴图显示了 Mono_FCN1(绿色)和 Mono_TIMP1(橙色)中代表性基因的表达。(F) GO分析。(G) 通过Monocle 2推断的单核细胞和肿瘤相关巨噬细胞的轨迹分析。(H-I) Kaplan-Meier 生存曲线。
06
TAM亚群调节免疫抑制微环境,并与免疫治疗疗效相关
肿瘤相关巨噬细胞(TAM)介导PT和BM中的抗肿瘤免疫。本研究鉴定了四个不同的TAM亚群(图 6A)。其中,TAM_MARCO和TAM_PLTP亚群表现出免疫抑制基因(如C1QA、C1QB、GPNMB和APOE)的高表达。同样,M2样特征基因(如CD163、CCL18和MSR1)以及MHC II类基因的表达也升高。这种表达谱提示其参与抗原呈递和免疫微环境的调控。此外,基于VEGFA、CD163和TGFB1的高表达水平,TAM_SPP1亚群与肿瘤血管生成和免疫逃逸相关。与之相反,TAM_MKI67 的特征是增殖标志物MKI67和TOP2A的高表达,表明其在 TAM 增殖中的作用。
使用 Wilcoxon 秩和检验和 scCODA 对 PT 和 BM 中 TAM 亚群比例进行比较分析,结果显示存在显著差异(图 6B)。TAM_MARCO 在 PT 中显著富集,而 TAM_PLTP 主要存在于 BM 中,表明巨噬细胞群存在部位特异性的功能特化。多重免疫荧光染色验证了这种差异分布,结果显示 BM 中 CD68+PLTP+细胞的水平显著高于 PT(图 6C-D)。仅限于 IV 期疾病(10 例 PT 与 26 例 BM)的子集分析同样证实了 BM 中 CD68+PLTP+细胞的富集,表明这种模式在晚期疾病中仍然存在,并且更符合组织特异性差异,而不是纯粹由阶段驱动的差异。
为了表征TAM_MARCO和TAM_PLTP之间的功能差异,他们评估了巨噬细胞极化特征并进行了伪批量差异表达分析。TAM_MARCO表现出M0和M1特征评分升高,以及干扰素刺激基因(MX1、IFIT3、ISG15)和免疫激活标志物(CD44、TRIM22)的高表达。相反,TAM_PLTP表现出M2特征评分升高,以及与免疫调节功能相关的基因(包括PLTP、FOLR2和CD300A)和补体成分C1QA和C1QB的高表达(图 6E-F)。
对两个亚群间差异表达基因的通路富集分析表明,TAM_MARCO 和 TAM_PLTP 参与不同的免疫激活程序(图 6G)。TAM_MARCO 富集干扰素介导的信号通路和抗病毒防御通路,这是抗肿瘤巨噬细胞的特征。TAM_PLTP 富集补体激活(经典途径、免疫球蛋白介导的体液免疫反应、B 细胞介导的免疫)和适应性免疫反应。虽然这两个亚群均表现出免疫激活特征,但肿瘤微环境中的补体介导免疫与通过血管生成和免疫抑制性髓系细胞募集促进肿瘤生长有关,这与这些 TAM 亚型相关的不同临床结局相一致。
为了评估这些TAM细胞群的临床意义,他们分析了它们与接受免疫治疗的NSCLC患者预后的关系。TAM_MARCO细胞丰度升高与PFS改善呈正相关趋势(图 6H),而TAM_PLTP细胞水平升高则与预后不良显著相关(图 6I)。这些结果表明,TAM_PLTP可能参与了脑转移性NSCLC特有的免疫抑制微环境的形成。
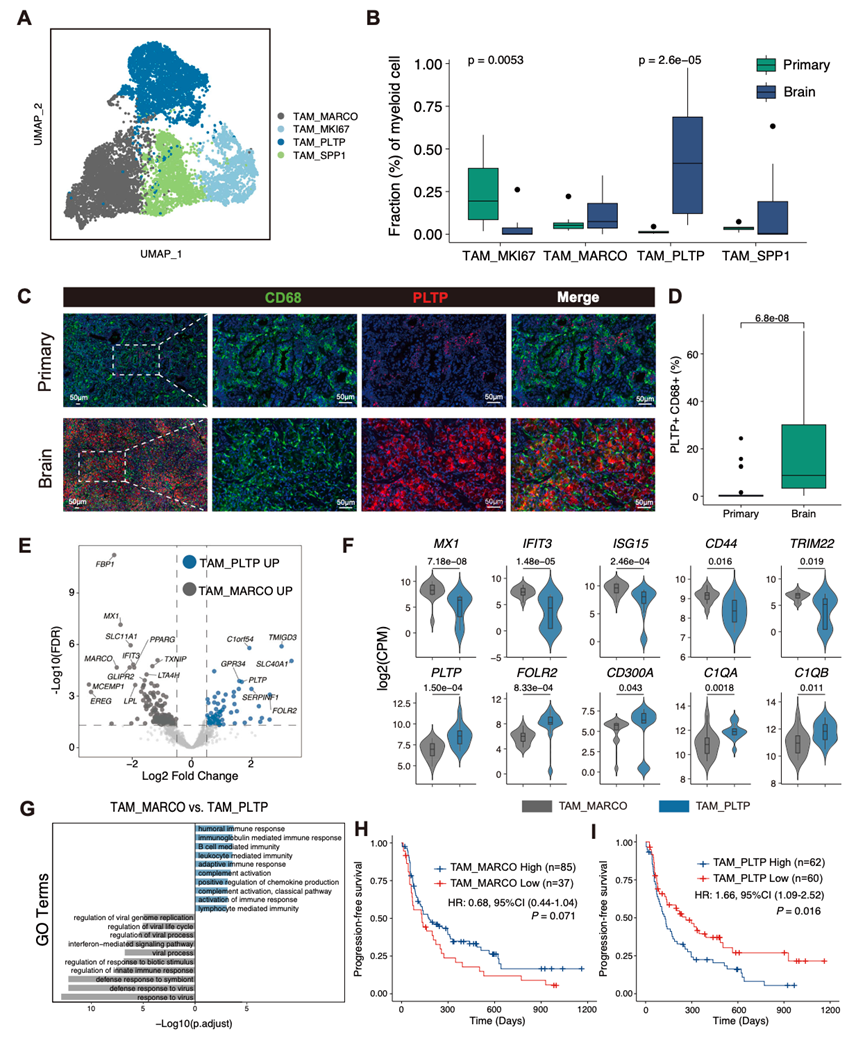
图6. PT 和 BM 中不同的肿瘤相关巨噬细胞 (TAM) 与不同的功能特征和预后意义相关。
(A) UMAP图显示了四个TAM亚聚类。(B) TAM亚聚类的比例。(C) 代表性的NSCLC切片多重免疫荧光图像。(D) 箱线图分析了免疫荧光图像中PLTP+ CD68+细胞的数量。(E) TAM_MARCO和TAM_PLTP之间差异基因表达的火山图。(F) 小提琴图展示了 TAM_MARCO(深灰色)和 TAM_PLTP(蓝色)中代表性基因的表达量。(G)GO分析。(H-I) Kaplan-Meier生存曲线分析。
07
PT和BM中B细胞和浆细胞亚群的特征
B细胞和浆细胞积极参与抗肿瘤免疫,并与免疫疗法的疗效相关。他们将这些细胞重新聚类为14个不同的亚群,以评估它们在NSCLC PT和BM中的分布情况。这些亚群包括5个记忆B细胞群(Bm_MS4A1、Bm_CD83、Bm_CD74、Bm_ALDOA和Bm_FCRL4)、2个幼稚B细胞群(Bn_IGHD和Bn_SPP1)、1个生发中心B细胞群(Bgc_LMO2)和6个浆细胞群(PC_IGHG1、PC_FKBP2、PC_XBP1、PC_JSRP1、PC_MKI67和PC_IGHM)(图 7A)。
他们比较了PT和BM中这些细胞聚类的相对丰度,以表征它们的功能。在Wilcoxon检验和scCODA分析中,他们观察到BM中幼稚B细胞聚类Bn_IGHD的比例降低(图 7B)。该细胞聚类的特征是IGHD、FCER2、IL4R和YBX3表达升高(图 7C)。表达IL4R和FCER2的B细胞与B细胞活化和IgE产生增加相关。使用NicheNet进行配体预测进一步鉴定出白细胞介素-4是Bn_IGHD的特异性配体(图 7D)。通路富集分析显示,该细胞聚类富集于B细胞活化、白细胞间黏附和抗原呈递通路,包括肽抗原与MHC II类分子的组装以及MHC II类蛋白复合物的组装(图 7E)。这些研究结果表明,Bn_IGHD 细胞有助于原发肿瘤中 B 细胞介导的免疫反应和抗原呈递。
他们通过评估 Bn_IGHD 与患者预后的关联性,探讨了其临床意义。这种幼稚 B 细胞聚类的富集显示出改善PFS的趋势(图 7F)。这些发现表明,Bn_IGHD 可能有助于抗肿瘤免疫,并可作为治疗反应的潜在生物标志物。
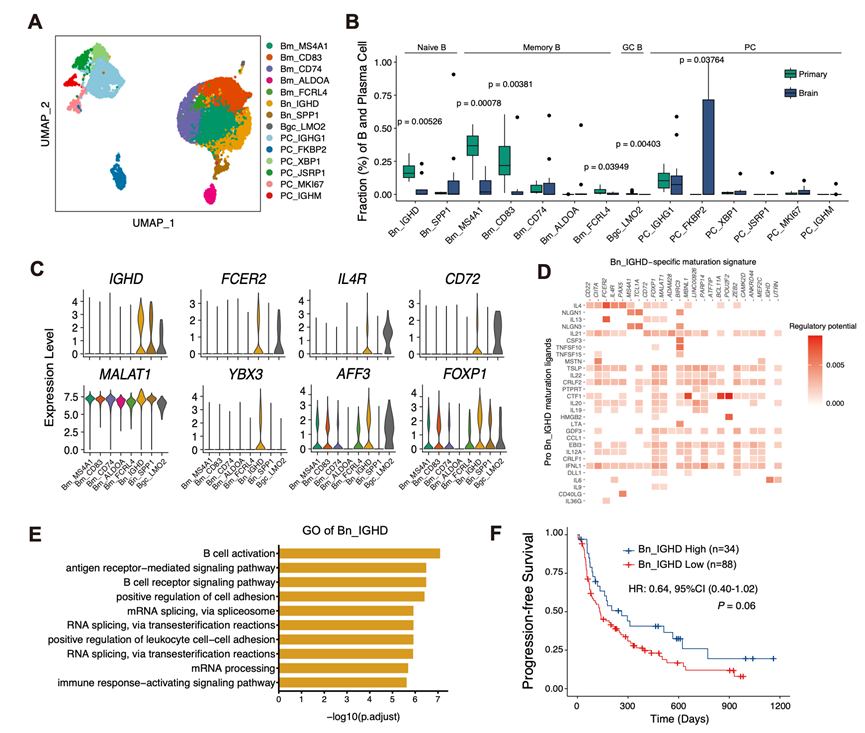
图7. PT 和 BM 中 B 细胞和浆细胞的特征分析显示 PT 中幼稚 B 细胞富集。
(A) UMAP图显示B细胞和浆细胞亚群。(B) 箱线图比较PT和BM NSCLC样本中B细胞和浆细胞亚群的比例。(C) 小提琴图显示Bn_IGHD细胞在不同亚群中的标记基因表达。(D) 热图显示驱动Bn_IGHD细胞表型的潜在配体。(E) GO分析。(F) Kaplan-Meier生存曲线分析。
08
BM来源免疫特征(BMIS)与多种癌症的免疫疗法疗效相关
为了验证通过scRNA-seq鉴定的细胞亚群的临床相关性,首先基于原发肿瘤和脑转移灶之间差异表达的六种关键细胞群(CD4_IL7R、DC_CLEC10A、TAM_MARCO、HSP70-High CD8、HSP70-High CD4、TAM_PLTP)的特征评分,对Ravi队列进行了无监督聚类分析。该分析识别出四个不同的患者群,这些患者群具有不同的免疫浸润特征(图 8A)。其中,以脑转移灶富集细胞群(HSP70-High T细胞和TAM_PLTP)浸润增强为特征的聚类2,在Ravi队列中显示出总生存期较差的趋势,但未达到统计学意义(图 8B)。在 mUC 队列中也观察到了类似的模式(图 8C)。
鉴于BM富集细胞群与免疫治疗耐药性之间的关联,通过提取与不良预后相关的细胞群(HSP70-High CD4、HSP70-High CD8、TAM_PLTP)中的差异表达基因,构建了一个定量预后模型。利用基于随机森林的变量选择(VSURF)进行特征选择(图 8D),他们鉴定出一个稳健的7基因特征(PLK3、VAMP8、CKS2、TSPYL4、CDKN1A、LAMTOR1、IFNG)。随后,他们训练了一个逻辑回归模型来预测治疗反应(CR/PR vs PD/SD),并将模型预测的概率作为连续的BMIS评分。
他们首先在发现队列中评估了BMIS的性能。使用预先设定的临界值,BMIS评分高的患者的PFS和OS均显著缩短(图 8E)。经年龄、性别和初始肿瘤分期校正的多因素Cox回归分析证实,BMIS是PFS和OS的独立预后因素。此外,与有疗效的患者(PR/CR)相比,无疗效的患者(PD/SD)的BMIS评分显著升高(图 8F)。相应地,高 BMIS 组的客观缓解率(PR/CR)仅为 27.2%,远低于低 BMIS 组的 65.9%(图 8G)。
为了评估BMIS的普适性,他们在三个独立的队列中进行了验证。在Kim队列中,高BMIS组的PFS呈现持续缩短的趋势,但由于样本量有限,该结果未达到统计学意义(图 8H)。在更大的转移性尿路上皮癌(mUC)队列中,BMIS展现出强大的预后价值,高BMIS评分与较差的OS和显著降低的客观缓解率显著相关(图 8I)。然而,在黑色素瘤队列中,他们未观察到BMIS与PFS或OS之间存在显著相关性。这表明,源自非小细胞肺癌脑转移的特征可能无法直接应用于黑色素瘤,这可能反映了不同癌症类型在肿瘤生物学和免疫微环境方面的根本差异。
最后,他们将BMIS的预测性能与现有生物标志物进行了比较,包括肿瘤突变负荷(TMB),后者是一种广泛用于免疫治疗反应的生物标志物。在Ravi队列中进行的受试者工作特征(ROC)分析显示,BMIS(AUC = 0.773)的预测能力与TMB(AUC = 0.715)相当。重要的是,整合BMIS和TMB的联合模型取得了更优的性能(AUC = 0.805)(图 8J)。这种互补的预测价值在mUC队列中得到了证实,其中BMIS + TMB联合模型(AUC = 0.764)的性能优于单独使用BMIS或TMB(图 8K)。这些发现表明,BMIS可能捕捉到不同于肿瘤突变图谱的免疫微环境特征,并且二者的整合可以增强对免疫治疗结果的预测。
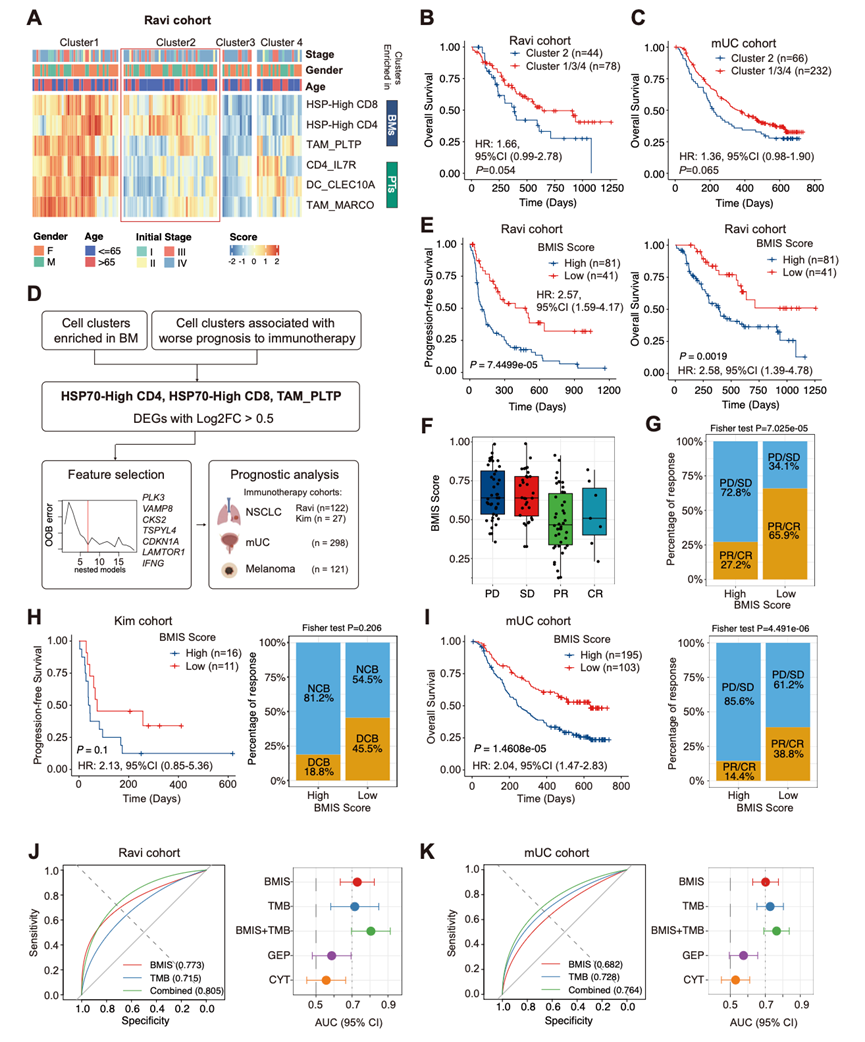
图8. 脑转移衍生免疫特征 (BMIS) 与各种癌症类型免疫治疗结果相关的开发和验证。
(A)无监督聚类分析。(B-C) Kaplan-Meier 生存曲线分析。(D) BMIS 开发流程。(E) 生存分析。(F) Ravi队列中BMIS评分在免疫治疗反应类别中的分布。(G) Ravi队列中按BMIS分组的达到客观缓解(PR/CR)或疾病进展/稳定(PD/SD)的患者比例。(H) 无进展生存曲线(左)和缓解率(右)。(I) 按BMIS分层的总生存曲线(左)和缓解率(右)。(J-K) 比较了BMIS与已建立的免疫治疗生物标志物(包括肿瘤突变负荷(TMB)、基因表达谱评分(GEP)和细胞溶解活性评分(CYT)的性能。
+ + + + + + + + + + +
结 论
本研究对来自原发肿瘤和脑转移灶的117752个肿瘤浸润免疫细胞进行了scRNA-seq,以阐明其独特的免疫微环境。BM表现出显著的免疫抑制性重编程,其特征是高HSP70应激反应性T细胞和PLTP+肿瘤相关巨噬细胞的富集,以及记忆性T细胞和cDC2样树突状细胞的减少,这些细胞与ICI疗效呈相反的相关性。整合这些发现,他们构建了一个包含七个基因的BMIS,该特征与NSCLC和转移性尿路上皮癌的ICI疗效和生存率相关,并提供了与肿瘤突变负荷互补的信息。这些结果突出了脑转移性非小细胞肺癌特有的免疫特征,并为改善这一高危人群的免疫疗法提供了候选生物标志物和治疗途径。
+ + + + +



 English
English


