文献解读 |Nat Commun ( 15.7 ):多模态皮肤图谱揭示了与特应性皮炎中角质化紊乱和特定 T 细胞扩增相关的多细胞免疫基质群落
✦ +
+
论文ID
原名:Multi-modal skin atlas identifies a multicellular immune-stromal community associated with disrupted cornification and specific T cell expansion in atopic dermatitis
译名:多模态皮肤图谱揭示了与特应性皮炎中角质化紊乱和特定T细胞扩增相关的多细胞免疫基质群落
期刊:Nature Communications
影响因子:15.7
发表时间:2026.02.25
DOI号:10.1038/s41467-026-69587-7
背 景
皮肤屏障和免疫功能的失调会导致慢性炎症组织生态系统的形成。特应性皮炎 (AD) 是一种常见的皮肤炎症性疾病,其特征是真皮上层存在免疫细胞浸润、表皮屏障功能受损,以及以 2 型极化免疫反应为核心,并可伴有 22 型、17 型和 1 型免疫反应特征。局部治疗和针对 2 型免疫反应的疗法,例如拮抗性 IL-4RA 抗体,仅对约 60% 的 AD 患者有效,且需要持续用药,这凸显了识别该疾病不同亚型和寻找合适干预措施的迫切需求。
实验设计
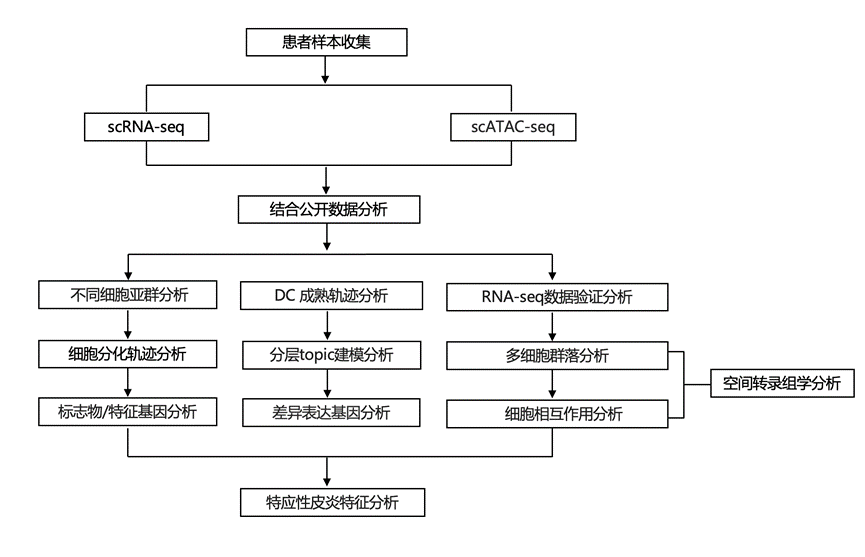
结 果
01
健康和AD皮肤的整合式多模态人类单细胞图谱
为了构建健康成人皮肤、AD非病变皮肤和AD病变皮肤的多模态细胞图谱,研究团队分析了来自17名成年人的27个样本,其中包括11名AD患者的21个样本(11个来自病变皮肤,10个来自非病变皮肤)以及6名性别匹配的健康对照者(涵盖白种人、黑人、亚裔和西班牙裔)的各1个样本(图 1a)。为了与AD进行比较,他们还收集了2名硬皮病患者的4个样本(图 1a)。他们采用基于单细胞转录组测序(scRNA-seq)技术和单细胞T细胞受体测序(scTCR-seq)技术分析了细胞(图 1a)。从39个通道(7个健康通道和32个AD通道)中保留了280518个高质量的细胞数据,从硬皮病样本中保留了29689个高质量的细胞数据,并获得了7256个T细胞,并为本研究队列中的8名AD患者分配了TCR序列(克隆)(图 1a)。
迭代聚类和事后注释解析出16个大的细胞类别(图 1b)和86个颗粒细胞亚群(图 1c-d),其中包括一些反映先前未识别状态和稀有细胞的亚群。例如,这些亚群包括MMP12+树突状细胞(DC)、CPE+成纤维细胞、CD90/THY1阴性的NGFR+和CDH19 +雪旺样成纤维细胞、多种稀有的皮肤附属器细胞亚群(包含毛囊、汗腺和皮脂腺亚群)以及循环固有淋巴细胞(ILC)。正如预期的那样,在病变(发炎)样本中,角质形成细胞(KC)表达的关键表皮炎症标志物S100A8和KRT16比非病变或健康样本高得多(图 1e-f)。
对健康、非病变和病变 AD 皮肤的总体细胞组成进行比较,结果显示,与健康皮肤相比,非病变和病变AD 皮肤中 DC 的比例均增加,病变皮肤中 T 细胞和自然杀伤 (NK) 细胞、巨噬细胞和中性粒细胞的比例也增加(图1g-h),这与免疫细胞浸润到病变中一致。相反,非病变和病变AD 皮肤中周细胞/平滑肌细胞(SMC)的比例降低,病变皮肤中血管内皮细胞、黑素细胞和汗腺细胞的比例降低(图1g-i)。
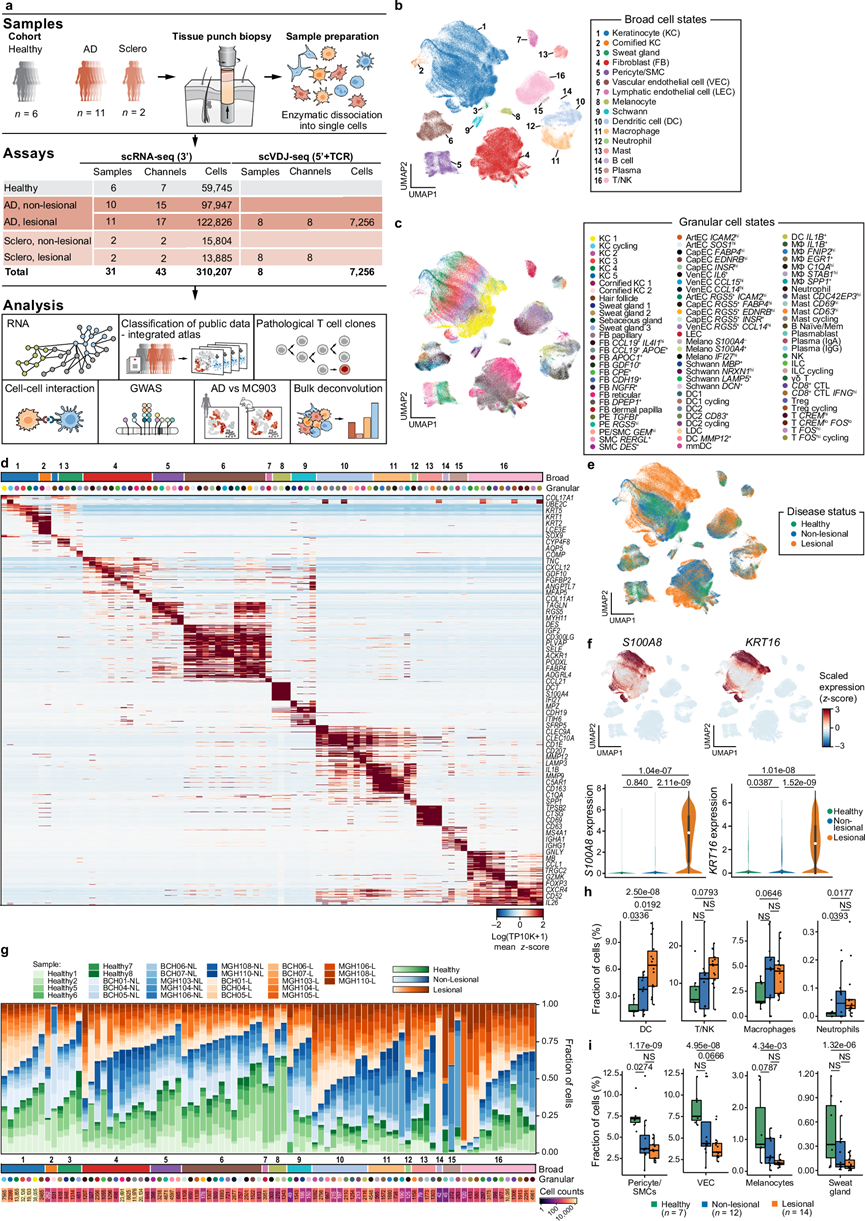
图1. AD患者健康皮肤、非病变皮肤和病变皮肤的多模态单细胞图谱。
(a)实验方案。(b-f) 皮肤细胞图谱。(g-i) 病变皮肤中免疫细胞比例增加。
02
角质形成细胞分化的全面重建
皮肤屏障的形成是通过角质形成细胞经基底层、棘层、颗粒层和角质层进行终末分化实现的。基于图的聚类和基于分区的近似图分析(PAGA)对KC揭示了8种相互连接的KC状态,这些状态重现了已知的KC分化特征(图 2a):从表达基底标记的KC1(KRT15、COL17A1)到循环KC(UBE2C、TOP2A)和KC2(MT1X、MT1G),棘状标记阳性的KC3(KRT1、KRT10),表达颗粒状标记的KC4(KRT2、DSC1)和KC5(CNFN、KLK7),最后是角质化的KC1(SPRR2A、SPRR2B)和角质化的KC2(IL37、PSORS1C2、LCE1B)(图 2a-c),不同角质形成细胞亚群中富集的基因集与已知的生物学机制一致。多项证据支持从 KC5 到角质化KC1和KC2的排序,包括晚期角质化包膜 (LCE) 与基底和棘状角质形成细胞标记基因的差异表达、角质化角质形成细胞中自噬和线粒体自噬基因的高表达。
接下来,他们将健康人KC的分化过程重建为一个连续过程[通过计算所有健康样本中KC的扩散伪时间(DPT),观察到一致的顺序,并捕捉到分化过程中动态的基因表达变化](图2d),这与人类蛋白质图谱中相应标记蛋白的空间定位相一致(图 2e)。这突显了关键已知分化转录因子(TF)(TP63、GATA3、GRHL3、GRHL1、PRDM1)和先前未与分化相关的TF(例如NFE2、NPAS1、ETV7)以及单基因皮肤病基因的时间模式。例如,引起大疱性表皮松解症的基因在基底层角质形成细胞的早期 DPT 点表达达到峰值,而引起鱼鳞病的基因在上层颗粒层和角质层的晚期 DPT 点表达达到峰值,这与KC附着于基底膜和脂质角质包膜形成的作用相一致。
AD 中的皮肤炎症改变了KC的轨迹和状态,导致角质化KC层重塑,并从角质化 KC2 向角质化 KC1 转变。首先,AD 病变皮肤中循环KC的比例和颗粒状 KC4 的比例增加,而基底KC1的比例减少(图 2f-g);此外 ,健康 样本中以角质化 KC2 为主,而 AD 病变皮肤中几乎完全以角质化 KC1 为主(图 2h-i)。基于DPT分析(图 2j),病变部位的KC分化轨迹与健康或非病变皮肤相比发生了改变。病变部位的KC5的DPT显著延迟,且存在一个特别延迟的模式;而病变部位的角质化KC(cKC)主要为cKC1,其DPT模式较早(图 2h-j)。这提示病变部位的AD的特征是基底KC1向循环KC的转变,随后KC5向cKC的分化减少,最终导致角质化缺陷。这种转变伴随着病变 AD 角质形成细胞中晚期角质化包膜基因(例如LCE5A、LOR)的细胞内在表达降低,以及富含脯氨酸的小蛋白(SPRR基因)表达增加(图 2k)。在非病变 AD 皮肤和两名硬皮病患者的病变样本中,未观察到cKC形成细胞层的重塑以及角质化 KC2 的减少和角质化 KC1 的相应增加,这强调了病变 AD 驱动的角化改变的独特性。未来的研究需要最终确定观察到的角质形成细胞分化改变是由于分化停滞,还是由于 AD 皮肤不同层细胞状态和存活率的变化所致。
病变角质形成细胞中表皮炎症标志物、干扰素通路基因、抗菌反应基因、脂质和限速胆固醇代谢基因的细胞内在表达也增加(图 2k),以及与 AD 中表皮增生和屏障功能障碍有关的 IL-20 相关细胞因子基因IL19和IL24。在所有KC中,cKC优先表达IL-1家族细胞因子和调节因子(IL1A、IL1B、IL18、IL36G、IL37、IL1F10/IL38、IL36RN)以及炎症小体通路相关基因(GSDMA、NLRP10、PYDC1)(图 2l),这与先前的体外观察结果一致。虽然在病变cKC中促炎细胞因子IL36G表达上调,但抗炎细胞因子IL37和IL1F10/IL38表达下调。
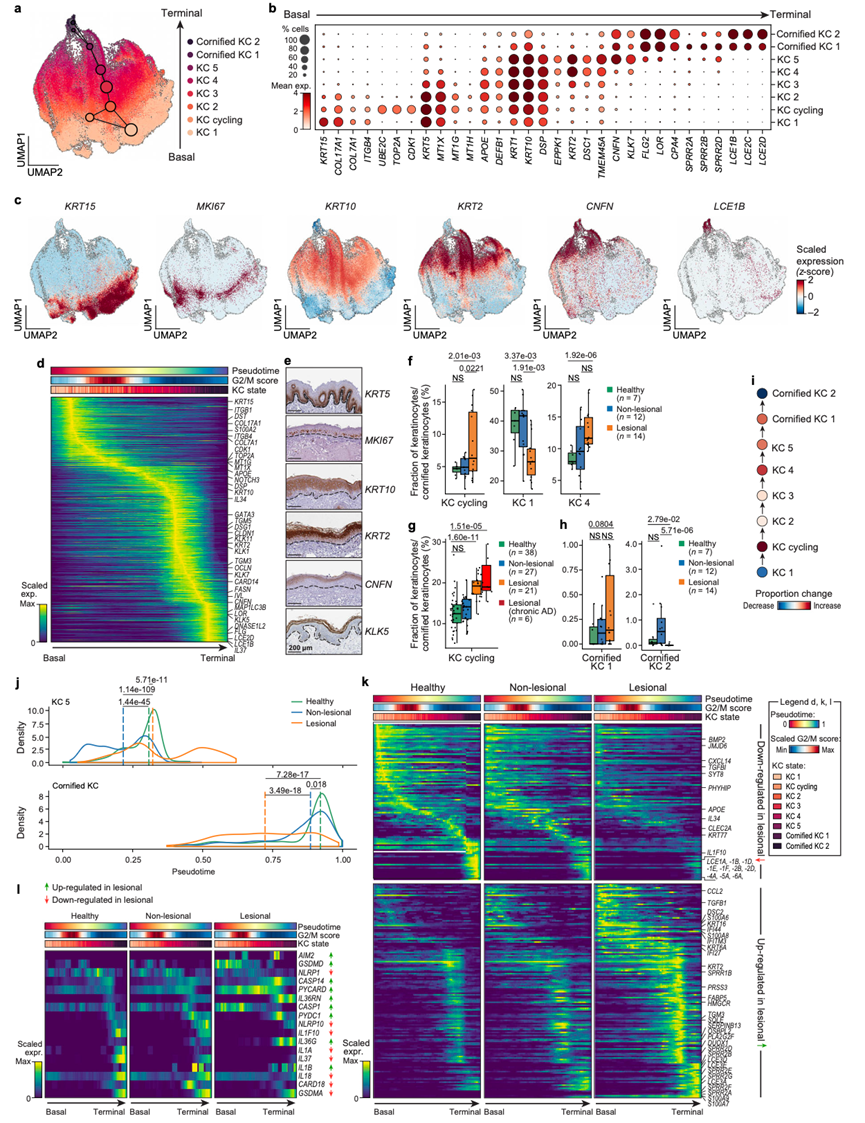
图2. 特应性皮炎中角质形成细胞分化的转变。
(a) 角质形成细胞亚群。(b) 角质形成细胞亚群(行)标记基因(列)的平均表达量和表达细胞比例。(c) 角质形成细胞亚群标记基因的z分数表达。(d) 健康对照组细胞(列)中标记基因的缩放表达值,按角质形成细胞从基底层到终末角质层的分化扩散伪时间(DPT)排序。(e) 免疫组织化学(IHC)染色。(f-h) 角质形成细胞亚群的比例。(i) 角质形成细胞比例随分化而变化。(j) AD皮肤中异常的 KC分化轨迹。(k-l) 差异表达基因分析。
03
健康、无病变和病变皮肤中树突状细胞(DC)成熟轨迹的两种情况
来自健康和AD皮肤的髓系细胞涵盖了一系列细胞状态,他们将其大致分为多个C1QA高表达的巨噬细胞(MΦ)亚群(C1QA、MS4A7、MAF、CCL18、CCL13)、炎症性IL1B+ MΦ(IL1B、MMP9)、脂质相关SPP1+ MΦ(SPP1、LPL)、组织驻留朗格汉斯树突状细胞(LDC)(CD207/Langerin、FCGBP)、DC1(CLEC9A、XCR1)和DC2(CD1C、FCER1A)、CD83+ DC2、炎症性IL1B + DC(先前称为DC3;IL1B、IL23A、CXCL8)以及最近发现的MMP12+ DC(MMP12,CD1B、RAB7B)、成熟迁移树突状细胞(mmDC)[LAMP3、CCR7;也称为富含免疫调节分子的成熟树突状细胞(mregDC)]、循环DC1和DC2(UBE2C、MKI67)以及中性粒细胞(CXCL8、FCGR3B、S100P)(图3a-b)。
在DC中,他们推断出两条不同的成熟轨迹,这两条轨迹均起源于DC2,并分别经由MMP12 + DC分化为mmDC(轨迹1),或经由CD83 + DC2分化为炎症性IL1B + DC(轨迹2)(图 3c-e)。
在轨迹1中,MMP12 + DC构成了一个CD40hiCD83 hiCD86lo LAMP3 lo CCR7lo的过渡状态,表明在 mmDC之前存在一种活化但未完全成熟的DC状态(图 3d)。与 DC 活化一致, MMP12+ DC高表达抗原呈递基因(HLA-DRB1、HLA-DQB1、CD1B、CD1A)、成熟调控转录因子(REL、NFKB1、SPI1、IRF4)和共刺激膜蛋白(CD226、CD40、CD83、TNFRSF4/OX40)(图 3d)。除了表达关键的 AD 疾病标志基因MMP12外,这些MMP12+ DC还表达编码特定蛋白酶抑制因子(CST6、CST7)和LDC标志物(CLDN1、CD207/Langerin)的基因(图 3d),表明MMP12+ DC中存在活化的LDC 。沿着轨迹1,MMP12+DC向 mmDC分化,后者表达已报道的mregDC特征,包括关键转录因子IRF4、肌动蛋白细胞骨架和迁移基因、DC成熟标志物、免疫调节程序(CD274/PD-L1、PDCD1LG2/PD-L2、CD200、IDO1)、CCL22和CCL17、参与募集CCR4+ 2 型炎症性 T 细胞的AD 疾病标志物、TSLP警报素素受体(CRLF2、IL7R)以及细胞因子IL15和 IL27 亚基EBI3(图 3d)。
在轨迹 2 中,DC2 细胞经由CLEC10AhiFCER1A hiCD83+过渡态(CD83+DC2 细胞)向IL1B+DC 细胞转变,后者以特定转录因子(CEBPB、HIF1A、STAT3)、特定趋化因子(CXCL2、CXCL3、CXCL8)、DC 成熟标志物(CCR7、LAMP3)的高表达以及IL1B和银屑病相关IL23A的大量表达为特征(图 3e),这种表达特征与已报道的皮肤 DC3 细胞一致。
在所有DC中,MMP12+ DC和mmDC在病变皮肤中均显著增加,与健康对照组相比, MMP12+ DC 在非病变通道中也富集(图 3f),而IL1B+ DC和CD83+ DC2的比例保持不变(图3f)。在另外两个经分类器注释的AD患者队列的scRNA-seq中,非病变皮肤和病变皮肤中MMP12+ DC和mmDC的比例也增加,并且在对AD患者的bulk RNA-seq进行反卷积时也观察到了类似的结果(图 3g)。病变皮肤中的MMP12+ D和mmDC的预测STAT6 TF活性增加,这可能会影响mmDC的活化或分化。
由于在多种炎症性疾病中均有报道存在mmDC/mregDC,他们将AD中mmDC的特征与人类mmDC/mregDC图谱进行了比较,构建了一个包含2551个mmDC的人类mmDC图谱,这些mmDC表达了核心mmDC特征,这些mmDC来自24个不同组织和疾病的scRNA-seq数据集,其中包括本研究中的1025个AD mmDC(图 3h-i)。与其他mmDC相比,AD病变部位的mmDC呈现出CCL22 hi、CCL17 hi、CCL19 lo、 IDO1 lo的状态(图3j-k),这与它们在诱导2型免疫反应中的功能相符。
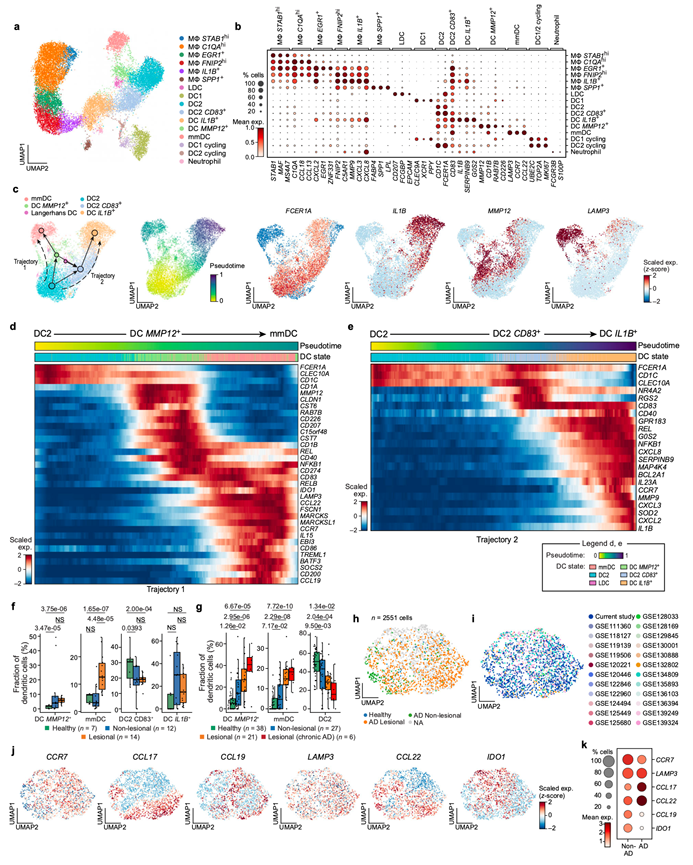
图3. AD 中MMP12+ DC和 mmDC通过激活轨迹增加。
(a)细胞亚群分析。(b) 髓系细胞标记物(列)在不同细胞亚群(行)中的平均表达量(点颜色)和表达细胞比例。(c) 选定的DC scRNA-seq谱的二维嵌入图和来自所有样本的定向PAGA连接图(节点和边)。(d-e) 所有样本中细胞的标记基因表达。(f-g) 病变皮肤中MMP12+ DC 和 mmDC 细胞比例增加。(h-k)富集状态分析。
04
细胞炎症程序在皮肤的CD4和CD8 T细胞中均处于活跃状态
16种淋巴细胞亚群包括CD3D阴性NK细胞(KLRD1、KLRF1、GNLY hi)和ILC(KIT、MB、SPINK2),γδT细胞(TRGC2、FXYD2、ZNF683/HOBIT),CD8A+细胞毒性T细胞(CD8A、CCL5、GZMK),CD4+调节性T细胞(Treg)(CTLA4、TIGIT、FOXP3、CCR8),在CD4+和CD8+T细胞中均存在多种CD40LG+T细胞,其中TCREM hi (CREM、CXCR4)和TFOS hi(FOS、IL32)状态均存在,幼稚/记忆B细胞(MS4A1/CD20、CD79A、SELL/CD62L),以及浆母细胞(FKBP4、IRF8)和表达IgA或IgG的浆细胞 (JCHAIN、MZB1、TNFRSF17)(图4a-b)。
由于许多皮肤淋巴细胞的变异是连续的(而非离散的亚群),并且可能共有相同细胞过程,他们采用随机块模型(SBM)(一种分层topic建模方法)对健康、非病变和病变皮肤样本中的淋巴细胞基因程序进行了表征。虽然一些程序反映了不同的细胞类型,例如调节性T细胞(topic #148)和细胞毒性T细胞(topic #227),但其他程序反映了细胞生物学过程(细胞周期,topic #97)或关键免疫过程(topic #196)。
一个显著的炎症免疫程序(topic #190)在多个 T 细胞亚群中表达(图4c-d),包括关键的2型或 17 型基因,例如细胞因子IL13、IL5、致痒因子IL31、IL22和IL26、IL25警报素受体IL17RB以及花生四烯酸、前列腺素和类花生酸通路基因(TBXAS1、HPGDS、CRTH2、SLC27A2、ALOX5AP、PLA2G16)(图 4e),包括PPARG,它与Th2 细胞分化和活化有关。基于对2518个非人灵长类动物背根神经节(DRG)神经元的scRNA-seq结果,IL31的表达可能允许其与表达IL31受体亚基(IL31RA、OSMR)的DRG NP3神经元相互作用。CD4+和CD8+ T细胞均表达该程序,其中CREM和FOS hi T细胞最为显著,而Treg细胞和CD8+GZMK+细胞毒性淋巴细胞则大多不表达,这与炎症效应程序的预期一致。
与健康皮肤中主要由CD8+细胞毒性 T 细胞组成的细胞群相比,病变 AD 中CD4+ T 细胞的比例较高,如先前报道(图 4f)。病变 AD 中非增殖和增殖性 Treg 细胞、增殖性FOS hi T 细胞、增殖性 ILC 细胞和IgG +浆细胞的比例也增加(图4g)。病变皮肤中的循环ILC表达细胞毒性基因(GZMB、KLRC1、PRF1)、CCL1以及关键炎症介质CSF2/GM-CSF、OX40配体TNFSF4和细胞毒性及组织驻留转录因子ZNF683/HOBIT(图 4h)。病变皮肤中的Treg表达较高水平的TNFRSF9(4-1BB)、TNFRSF4(OX40)、TNFRSF18(GITR)和T细胞活化标志物(CD69、HLA-DPA1)。
为了寻找AD特异性程序,他们计算了病变皮肤样本和健康皮肤样本之间的差异主题表达,并将表达炎症免疫程序的T细胞topic #190确定为差异表达最显著的topic(图4j-k)。这与AD特异性的T细胞状态从细胞毒性向促炎状态的转变相一致。他们还发现Treg(#148)、细胞周期(#111、#97、#94、#23)和T细胞活化/分化程序(#53、#113、#196)发生了显著变化(图4j-k),以及细胞毒性程序(#227、#78)的减少(图 4j-k)。在非病变和病变 AD 皮肤中,表达IL13、IL22和IL26的细胞比例均持续增加,而病变 AD 中表达IFNG 的细胞比例低于健康通道(图4k)。在病变皮肤中,出现了表达IL13、IL22和IL26中两种或三种的 T 细胞,尤其是在循环FOShi T 细胞中,以至于大多数(>66%)IL13+细胞也共表达IL22和IL26中的至少一种(图 4l-m)。
对来自 8 名患者的病变活检组织进行 scTCR-seq 和scRNA-seq 联合分析(图 4n),检测到2294个扩增的和3753个非扩增的CD4 + T 细胞(图 4o),扩增的CD4 + T 细胞中 IL13/IL22/IL26双阳性和三阳性 T 细胞以及topic #190 表达显著富集(图4p-s)。这表明存在一种与疾病相关的、克隆扩增的促炎性 T 细胞群,具有2型和 17 型 T 细胞的重叠特征。
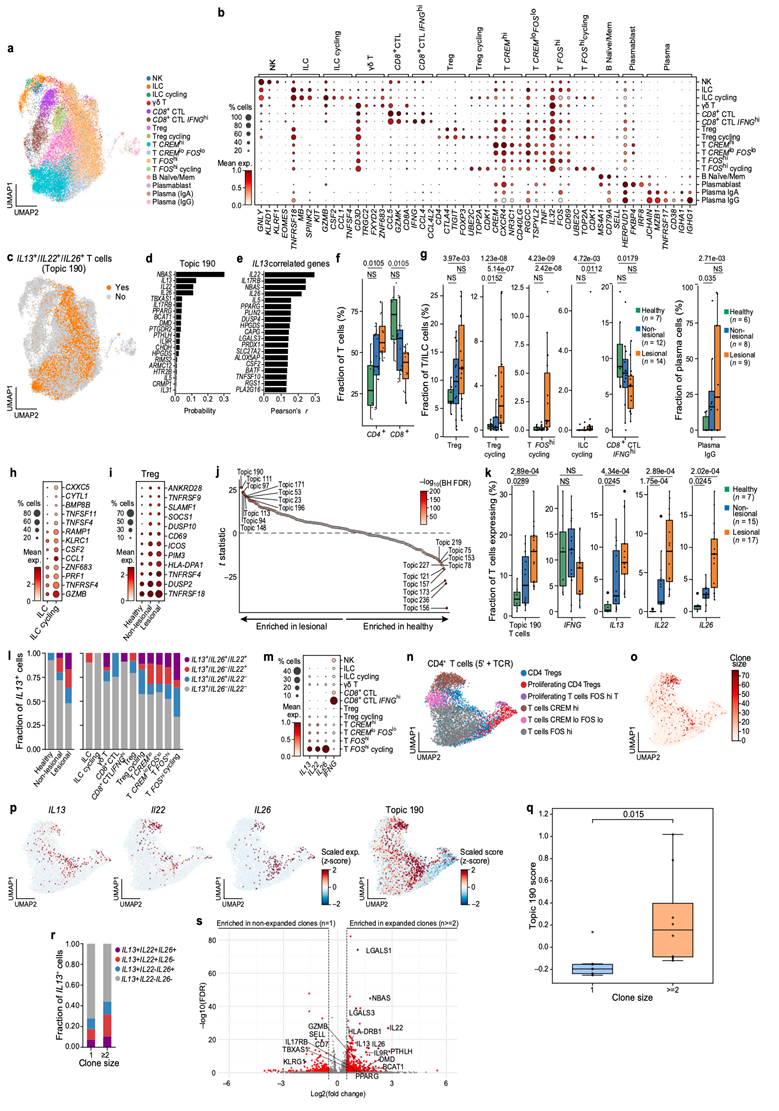
图4. AD 中扩增的 T 细胞克隆中的IL13/IL22/IL26程序。
(a) 所有样本的皮肤淋巴细胞scRNA-seq谱的二维嵌入图。(b) 按细胞亚群划分的标记基因的平均表达量和表达淋巴细胞的百分比。(c) scRNA-seq谱的二维嵌入图(与a相同),按IL13/IL22/IL26的表达着色。(d) 得分最高的基因的概率。(e) 与单个淋巴细胞谱中IL13表达相关性最高的基因。(f-g) 血浆 IgG 细胞类型。(h-i) ILC 亚群或 Treg 细胞中特定病变富集基因的平均表达量和表达细胞百分比。(j)差异分析。(k) 淋巴细胞比例。(l) 不同条件下或淋巴细胞亚群中单阳性、双阳性或三阳性IL13/IL22/IL26共表达细胞的比例。(m) 平均表达量和表达IFNG、IL13、IL22、IL26的细胞百分比。(n-p) 细胞类型分析。(q) Topic #190 评分。(r) 表达IL13的非扩增和扩增T细胞克隆中单阳性、双阳性或三阳性共表达细胞的比例。(s) 扩增与非扩增CD4+ T细胞中差异表达分析。
05
AD基质重塑伴免疫调节成纤维细胞增多
皮肤基质细胞包括 11 个成纤维细胞亚群、8 个血管和淋巴管内皮细胞亚群(图 5a-c)、5 个周细胞亚群、平滑肌细胞以及髓鞘形成细胞和非髓鞘形成细胞。11个成纤维细胞亚群(图 5d-e)包括两个富含免疫调节功能的CCL19+成纤维细胞亚群: CCL19+ IL4I1 +成纤维细胞(IL32、TNC、VCAM1),表达高水平的MHC-I和MHC-II 呈递基因(图 5f);以及CCL19+ APOE +成纤维细胞(RBP5、TNFRSF13B、CXCL1),两者均表达先前在其他人类病理(包括溃疡性结肠炎)中报道的CCL19+和ADAMDEC+成纤维细胞的标记物。成纤维细胞还包括两个表达近期报道的神经相关成纤维细胞标志物的亚群:CDH19 +细胞(SCN7A、ANGPTL7、EBF2)和NGFR+细胞(ITGA6、TNNC1、WNT6)(图5d-e)。除了近期报道的THY1+皮肤基质细胞外,还揭示了多种THY1-基质细胞群,包括CDH19+和NGFR+细胞以及RERGL+和DES+平滑肌细胞。
与健康皮肤相比,AD 病变中的基质亚群组成发生了显著变化,CCL19+ IL4I1 +成纤维细胞、GDF10+成纤维细胞、INSR+ CapEC和ICAM2 hi ArtEC的比例显著升高,而乳头状成纤维细胞和EDNRB hi CapEC的比例则降低(图 5g)。与之前的报道一致,CCL19+IL4I1+成纤维细胞在AD病变中增多最为显著,他们在重新注释的已发表AD单细胞数据和转录组分析(RNA-seq)数据中进一步证实了这一点(图5g)。与健康皮肤中的相应细胞相比,病变皮肤中的CCL19+IL4I1+成纤维细胞中VI型胶原基因、PDPN、IL13RA2、T细胞和中性粒细胞募集趋化因子(CCL19、CXCL1)以及免疫细胞黏附和组织修复调节因子(VCAM1、POSTN)的表达均增加(图 5h)。这些特征与炎症性肠病中结肠CCL19+成纤维细胞和唾液腺三级淋巴结构中CCL19 +成纤维细胞的特征相似。
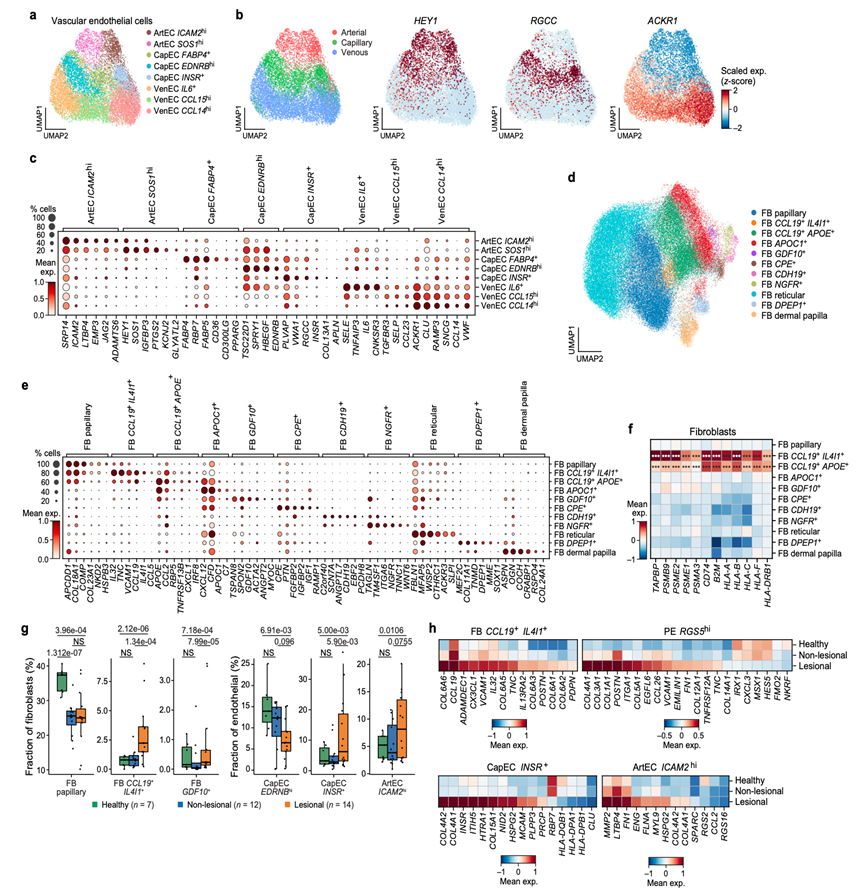
图5. AD 皮肤基质中免疫调节成纤维细胞增加。
(a-b) 皮肤血管内皮细胞分析。(c) 血管内皮细胞亚群(行)中标记基因(列)的平均表达量(点颜色)和表达细胞百分比(点大小)。 (d) 所有样本的成纤维细胞scRNA-seq谱的二维嵌入图,按细粒度注释着色。(f) 各亚群(行)中标记基因(列)的平均表达量(点颜色)和表达细胞百分比(点大小)。(g) 不同条件下基质细胞亚群(x轴)的比例(y轴)(柱状图颜色)。(h) 基质细胞亚群(上)在疾病条件(行)之间差异表达的基因(列)的 Z 分数平均表达。
06
AD 中的多细胞群落可能影响 KC 分化
通过主成分分析 (PCA),健康、非病变和病变通道根据其细胞组成进行区分(图 6a)。第二主成分 (PC2) 捕捉了病变通道与非病变/健康通道之间的差异,反映了病变中IL13+/IL22 +/IL26+T 细胞、mmDC、MMP12+ DC、中性粒细胞和CCL19+ IL4I1+ 成纤维细胞的共同增加,以及角质化KC2的显著减少(图 6b)。
在不同样本中,病变富集的免疫细胞和基质细胞亚群的细胞比例高度相关,从而在病变皮肤中识别出多个多细胞群落(图 6c)。其中一个群落由IL13+/IL22+/ IL26+T细胞、增殖的FOS hi T细胞、mmDC、MMP12+ DC和CCL19+ IL4I1+成纤维细胞组成(群落1)(图 6c),另一个群落(部分重叠)由中性粒细胞、IL1B+DC和CREM hi T细胞亚群组成(群落2)。他们使用公开的AD空间数据集进一步验证了这些群落的存在和结构。首先,RNA原位杂交表明,T细胞是AD病变皮肤中IL13的主要来源。其次,AD病变皮肤的空间转录组学鉴定出邻近细胞具有IL13、IL13RA1、IL13RA2、CCL17、CCL19、CCL22和MMP12的独特转录特征,与AD图谱中的群落1成员相匹配,包括IL13+/IL22+/ IL26+T细胞、循环FOShi表达T细胞、CCL19+IL41+成纤维细胞、mmDC和MMP12+ DC(图 6d-e)。类似地,他们观察到另一组空间相邻的细胞表达IL17A、CXCL1、CXCL8、CCL20、IL22和IL26,与群落2成员相匹配,包括IL1B +DC和IL13+/IL22+/ IL26+ T 细胞。
在群落1发现了多个受体-配体 (RL) 相互作用,这些相互作用在病变 AD 中显著富集(图6d-f),具有多个自我增强的正反馈回路,可能有助于群落的稳定性,尤其是在FOShi T 细胞、mmDC、ILC 和CCL19+IL41+成纤维细胞之间(图 6f)。例如,mmDC 表达CCL19、CCL17和IL15,分别募集和扩增T细胞和ILC/NK 细胞,相反,循环的FOShi T 细胞表达TNFSF4、FLT3LG、CSF2和TNFSF11/RANKL,它们是 DC 活化、扩增、存活和成熟的介质(图6d-f)。与该模型一致,mmDC 中CCL19和CCL17细胞固有表达水平与增殖的FOShi T细胞比例之间存在正相关性(图 6f),增殖的FOShi T细胞中TNFSF4表达与mmDC比例之间也存在正相关性(图 6f)。
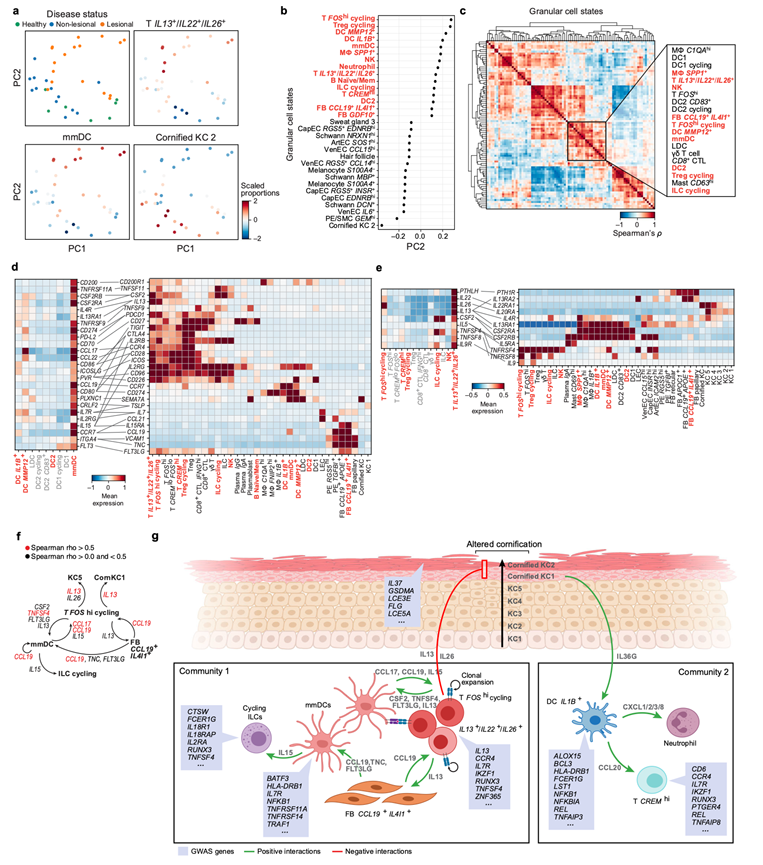
图6. 与疾病相关的两种多细胞群落。
(a) 基于细胞组成主成分分析(PCA)得到的前两个主成分(PC)对健康、非病变和病变通道进行二维嵌入,并根据疾病状态或所示细胞亚群的缩放比例进行着色。(b) PC2载荷最高的(红色)和最低的(黑色)15个细胞亚群。(c) 细胞状态分析。(d-e) 细胞间相互作用。(f) 多个正反馈回路可能启动或稳定多细胞群落。(g) 多细胞病理过程的示意图。
+ + + + + + + + + + +
结 论
本研究对来自 17 名成年人(包括 11 名 AD 患者)的完整皮肤组织样本中的 280518 个细胞进行了多模态分析,并将其与来自先前四项研究的 430186 个细胞谱整合,构建了一个全面的人类皮肤细胞图谱。KC分化的重建揭示了AD中角质化受损与免疫和基质多细胞群落的信号相关——该群落由MMP12+和迁移性DC、ILC、NK、炎症性CCL19 + IL4I1 +成纤维细胞以及克隆扩增的IL13+ IL22+ IL26 + T 细胞组成,这些细胞通过细胞间反馈回路相互连接,预计会影响群落的稳定性,该细胞群的亚群以及受损的角质形成细胞形成的该通讯网络的功能障碍可能引发AD。
+ + + + +



 English
English


