文献解读|Signal Transduct Target Ther(52.7):小细胞肺癌的外在和内在特征以及治疗脆弱性的表征
✦ +
+
论文ID
原名:Characterization of the extrinsic and intrinsic signatures and therapeutic vulnerability of small cell lung cancers
译名:小细胞肺癌的外在和内在特征以及治疗脆弱性的表征
期刊:Signal Transduction and Targeted Therapy
影响因子:52.7
发表时间:2025.09.10
DOI号:10.1038/s41392-025-02378-6.
背 景
小细胞肺癌(SCLC)是一种高度侵袭性的恶性肿瘤,占所有肺癌病例的15%,每年在全球造成27万患者死亡。由于手术治疗较少,导致缺乏用于深入研究疾病发病机制的标本。在SCLC中,已检测到抑癌基因(包括TP53和RB1)的功能缺失突变,但癌基因的高频功能获得性突变却鲜有报道。根据转录因子 Achaete-scute 同源物 1 (ASCL1, A)、神经源性分化因子 1 (NEUROD1, N)、POU 2 类同源框 3 (POU2F3, P) 和 Yes 相关蛋白 1 (YAP1, Y) 的表达以及炎症基因特征,SCLC在分子水平上可分为 SCLC-A、N、P、Y 和 I 型。在这些亚型中均检测到肿瘤内异质性 (ITH) 增加和免疫抑制性肿瘤微环境 (TME)。虽然免疫疗法已广泛应用于临床,但所有分期 SCLC 患者的 5 年生存率仍低于 7%。因此,仍需开展多组学研究,以识别癌基因和分子亚型中高频的功能获得性改变,从而优化治疗方案。
实验设计
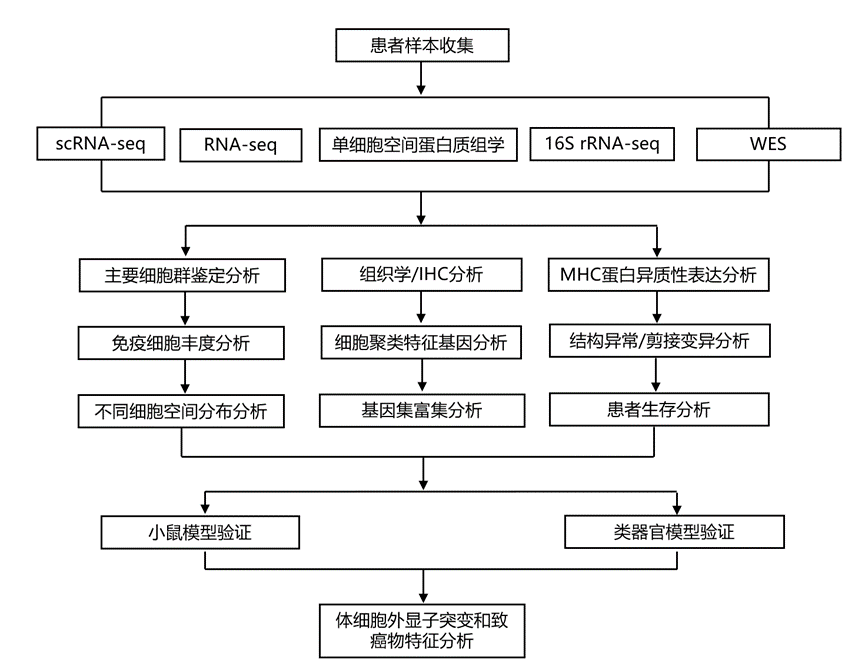
结 果
01
小细胞肺癌队列分析
为了深入研究小细胞肺癌(SCLC)的肿瘤发生机制和治疗靶点,研究团队收集了来自中国8个城市10家医院的314例患者的配对肿瘤组织和正常组织标本。其中,300例(95.5%)诊断为SCLC,14例(4.5%)为混合型SCLC。从人口统计学特征来看,237例(75.5%)为男性,77例(24.5%)为女性。共有150例(47.8%)年龄小于60岁,164例(52.2%)年龄在60岁及以上。在这些患者中,208例(66.2%)为吸烟者,88例(28.0%)为非吸烟者。就疾病分期而言,125 例(39.8%)患者归类为 IA-IIB 期,154 例(49.0%)患者归类为 IIIA-IV 期。
为了全面研究 SCLC 的内在和外在改变,他们对 39 例患者的 65 个样本(39 个肿瘤、14 个邻近正常肺组织、7 个外周血单核细胞和 5 个淋巴结)进行了 scRNA-seq(图1a),对 45 对肿瘤-正常组织进行了转录组分析(RNA-seq),对 53 对肿瘤-正常组织进行了 16S rRNA-seq 以评估微生物群落,对 111 对肿瘤-正常组织进行了全外显子组测序(WES),对 12 个福尔马林固定石蜡包埋 (FFPE) 样本进行了单细胞空间蛋白质组学分析,对 62 例 SCLC 患者和 56 例健康供体的血清进行了细胞因子/趋化因子谱分析,并对一组独立的 136 例 SCLC 肿瘤进行了等位基因特异性剪接(ASE)分析。
为了确定小细胞肺癌(SCLC)中的主要细胞群,本研究对患者的样本进行了单细胞转录组分析(scRNA-seq)。从27例未经治疗的患者和12例接受治疗的患者中获得了432959个单细胞。通过选择各细胞谱系中的标记基因,鉴定出7种主要细胞类型和58种亚型(图1b-c)。主要细胞类型包括内皮细胞、成纤维细胞/成纤维细胞样细胞、I/II型肺泡细胞(AT1/2)/基底细胞/纤毛细胞/棒状细胞、神经内分泌细胞(NE)/癌细胞、巨噬细胞(Mφ)/单核细胞、B细胞和T/NK细胞(图1c)。如前所述,9个NE细胞聚类是SCLC癌细胞的代表。在27例治疗前肿瘤中,19例(70.4%)肺癌肿瘤的免疫细胞数量较少(<10%),7例(25.9%)肺癌肿瘤的免疫细胞数量中等(10-50%),1例(3.7%)肺癌肿瘤的免疫细胞数量较多(>50%)(图1d),提示不同患者的免疫微环境存在异质性。在血液样本中也检测到了癌细胞,这与之前的报道一致。与正常肺组织相比,肿瘤样本中AT2细胞和巨噬细胞数量较少,而癌细胞数量则有所增加。在治疗前和治疗后的肿瘤样本中,III期和IV期小细胞肺癌(SCLC)样本中的B细胞数量均显著低于I期和II期SCLC样本。在接受化疗或化疗联合免疫疗法(依托泊苷/顺铂联合抗PD-L1抗体)治疗的12例患者中,分别有4例、4例、3例和1例患者达到完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。他们比较了缓解组和无缓解组的细胞组成,观察到缓解组中巨噬细胞、基底细胞和纤毛细胞的比例显著高于无缓解组,而癌细胞的比例显著低于无缓解组。
为了检验SCLC和非小细胞肺癌(NSCLC)免疫浸润的潜在差异,他们比较了该队列中SCLC肿瘤样本与中国人群NSCLC样本中免疫细胞的比例。与NSCLC样本相比,治疗前SCLC样本中T/NK细胞、B细胞和Mφ细胞的比例略低,但差异无统计学意义;而治疗后SCLC样本中B细胞的比例略高于NSCLC样本(图1e)。对不同数据集的RNA-seq数据进行反卷积分析显示,SCLC和NSCLC患者的T细胞、B细胞或Mφ细胞水平无显著差异(图1f)。
为了进一步阐明小细胞肺癌(SCLC)肿瘤样本中SCLC细胞和免疫细胞的空间分布,他们进行了单细胞分辨率的空间蛋白质组学分析。他们发现,肿瘤组织中浸润的免疫细胞数量少于正常肺组织,且早期SCLC患者的肿瘤中颗粒酶B+/CD8+ T细胞数量多于晚期SCLC患者。治疗后,CR和PR患者的这些免疫细胞数量高于SD患者。此外,他们在肿瘤中检测到了三级淋巴结构(TLS),发现早期患者的TLS数量多于晚期患者和治疗无应答患者(图1g-h)。这些 TLS 对 CD45、CD8、CD3、CD4 和 CD20 呈阳性,但对CD14呈弱阳性(图1g)。
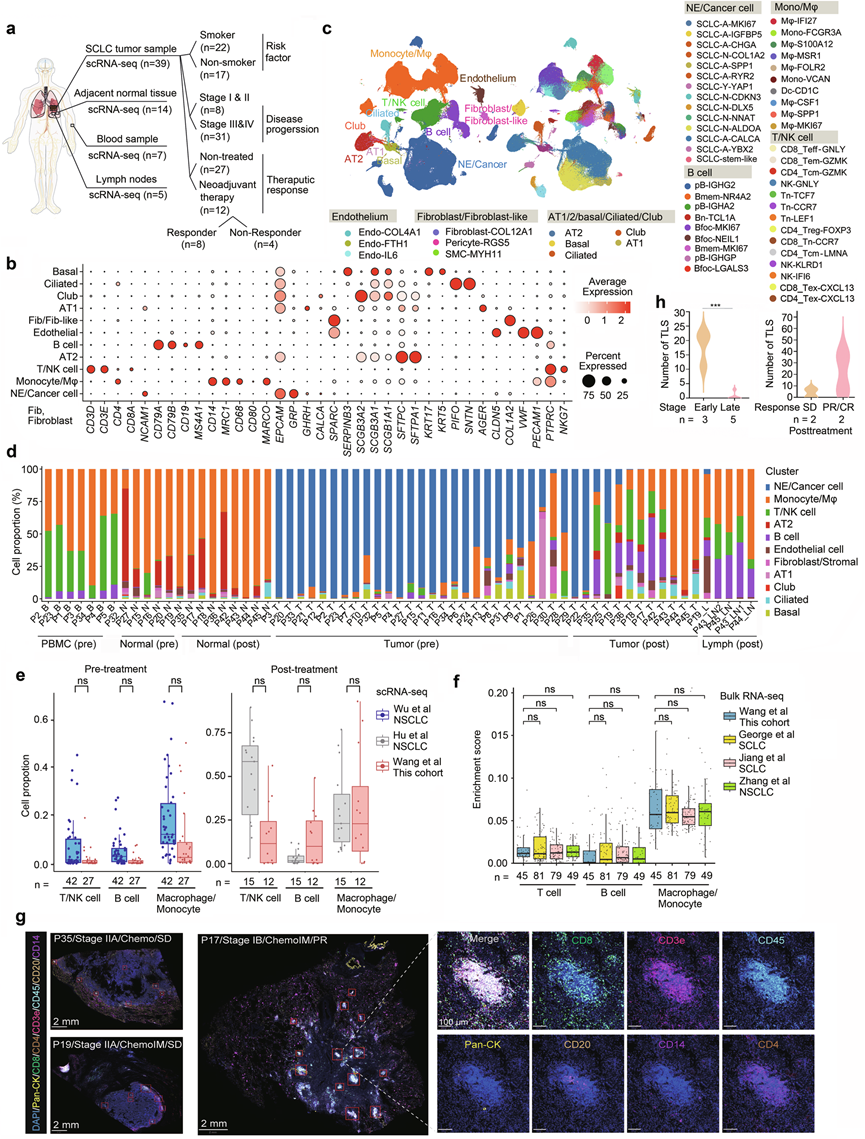
图1. 小细胞肺癌 (SCLC) 的微环境图。
(a) 转录组学研究设计示意图。(b) 各细胞谱系中选定的标记基因的点图。(c) UMAP可视化肿瘤微环境中癌症和免疫细胞的表达谱聚类。(d) 条形图显示了每个样本中 7 种主要细胞类型的分布。(e)分析T/NK 细胞、Mφ/单核细胞和 B 细胞的比例。(f) T细胞、巨噬细胞/单核细胞和B细胞相对富集的比较。(g-h) 接受新辅助治疗患者的TLS和定量。
02
小细胞肺癌微环境中免疫细胞的改变
他们研究了SCLC患者复杂微环境中存在的免疫细胞亚型,鉴定了7种不同的Mφ亚型、2种单核细胞亚型和1种树突状细胞(DC)聚类(图2a-b)。Mφ亚型因样本类型、肿瘤分期和新辅助治疗方案而异。具体而言,Mφ- IFI27(干扰素α诱导蛋白27)和Mφ- MSR1(巨噬细胞清道夫受体1)主要在正常邻近组织样本中发现,而大多数单核细胞则在外周血单核细胞(PBMC)样本中检测到(图2a)。新辅助治疗后,Mφ- S100A12(S100钙结合蛋白A12)、Mono- VCAN(Versican)和Mφ- SPP1水平降低,而Mφ- MSR1水平升高(图2c)。在未接受治疗的人群中,吸烟者的Mφ- MKI67(增殖标志物Ki-67)水平显著高于非吸烟者(图2d)。此外,达到部分缓解/完全缓解(PR/CR)的患者中Mφ- IFI27和Mφ- CSF1(克隆刺激因子1)水平升高,而Mφ- SPP1水平低于疾病稳定/进展(SD/PD)患者(图2e)。Mφ- SPP1与血管生成和肿瘤进展相关,他们通过分析其转录组特征对其进行了进一步表征。在 Mφ- SPP1中,参与受体介导的内吞作用和趋化因子反应的基因,如APOE、甘露糖受体 C 型1 (MRC1) 和CXC 基序趋化因子配体 8 (CXCL8),均显著上调。
他们鉴定出14种不同的T/NK细胞亚群,包括幼稚T细胞(Tn细胞),其表达TCF7(转录因子7)、CCR7(CC基序趋化因子受体7)和LEF1(淋巴增强因子结合因子1);中央记忆T细胞(Tcm细胞),其表达GZMK(颗粒酶K)和LMNA(层粘蛋白A/C);效应T细胞(Teff细胞),其表达GNLY(颗粒溶素);效应记忆T细胞(Tem细胞),其表达GZMK;耗竭CD4 +和CD8 + Tex细胞,其表达CXCL13(CXC基序趋化因子配体13);调节性T细胞(Treg细胞),其表达FOXP3(叉头框蛋白P3);NK细胞,其表达GNLY、KLRD1(杀伤细胞凝集素样受体D1)和IFI6(干扰素α诱导蛋白6)(图2f)。在该队列的肿瘤样本中,他们鉴定出 84 个NK细胞,占总 T/NK 细胞的 0.52%,占所有肿瘤细胞的 0.03%。此外,对3例未经治疗的SCLC患者的 FFPE 样本进行免疫组织化学(IHC) 分析显示,在 973346 个肿瘤细胞中,有3548个(0.36%)细胞 CD94(一种 NK 细胞标志物)呈阳性。新辅助治疗后,CD8_Tem -GZMK和 NK- KLRD1水平升高,而 CD4_Treg- FOXP3水平降低(图2g)。
他们鉴定了 9 个不同的 B 细胞亚群,包括幼稚 B (Bn) 细胞 Bn- TCL1A(TCL1 家族 AKT 共激活因子 A)、记忆 B (Bmem) 细胞类型 Bmem- NR4A2(核受体亚家族 4 A 组成员 2)和 Bmem- MKI67、滤泡 B (Bfoc) 亚型 Bfoc- NEIL1(Nei 样 DNA 糖基化酶 1)、Bfoc- LGALS3(半乳糖凝集素 3)和 Bfoc- MKI67,以及浆细胞亚型 pB- IGHA2(免疫球蛋白重链恒定区 α 2)、pB- IGHG2(免疫球蛋白重链恒定区 γ 2)和 pB- IGHGP(免疫球蛋白重链恒定区 γ P)(图2h)。新辅助治疗后,pB- IGHA2、Bmem- MKI67和 Bfoc- LGALS3的水平升高,其中达到PR或CR的患者pB- IGHA2水平更高(图2i)。这些结果提示 B 细胞可能在SCLC中发挥抗肿瘤作用,这与其在肺腺癌中的作用一致。
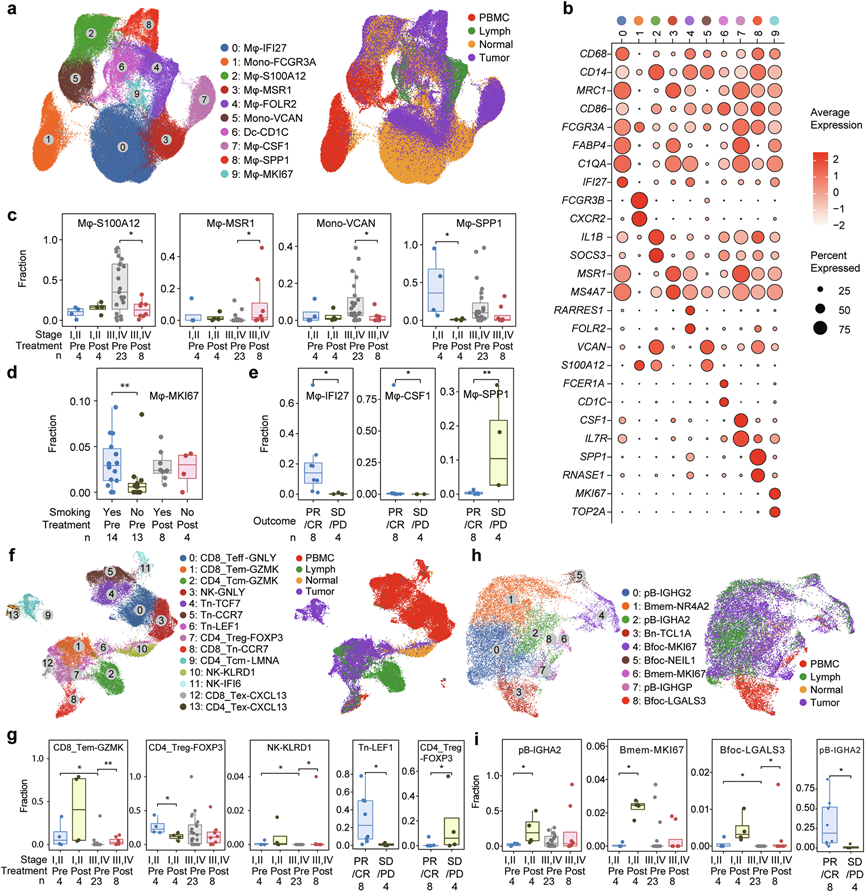
图2. SCLC 微环境中的免疫细胞。
(a) 巨噬细胞 (Mφ)/单核细胞分析。(b) 每种细胞谱系中选定基因表达的点图。(c-e) 箱线图表示每种 Mφ/单核细胞群体的相对比例。(f) T /NK 细胞分析。(g) 箱线图表示每种 T/NK 细胞亚型的相对比例。(h) B细胞分析。共鉴定出 9 种 B 细胞亚型(左图)。右图显示了不同样本类型中的细胞分布。(i) 箱线图表示每种 B 细胞亚型的相对比例。
03
小细胞肺癌细胞的异质性
为了阐明癌细胞的复杂特征,他们分析了肿瘤样本中的非造血细胞,并鉴定了 19 个细胞聚类,其中包括 5 个非癌性细胞聚类:AT1、AT2、基底细胞、纤毛细胞和棒状细胞(图3a-b)。共获得 190313个癌细胞,并将其分为 14 个亚聚类:C0:SCLC-A-MKI67,C1:SCLC-A- CRIP2(富含半胱氨酸蛋白 2),C3:SCLC-A-CHGA(嗜铬粒蛋白 A),C4:SCLC-N- COL1A2(I 型胶原蛋白 α2 链),C6:SCLC-A- SPP1,C8:SCLC-A- RYR2(兰尼碱受体 2),C9:SCLC-Y- YAP1,C10:SCLC-N- CDKN3(细胞周期蛋白依赖性激酶抑制剂 3),C12:SCLC-A- DLX5(远端缺失同源框 5),C13:SCLC-N- NNAT(神经蛋白),C14:SCLC-N- ALDOA(醛缩酶,果糖二磷酸 A),C16:SCLC-A- CALCA(降钙素相关多肽 α),C17:SCLC-A- YBX2(Y-Box 结合蛋白 2),以及 C18:SCLC-干细胞样细胞(SLC)(图3b-c)。
C1 和 C0 细胞聚类的数量分别达到 100754 个(占所有癌细胞的 52.94%)和 40807 个(占 21.44%),代表了两种最主要的癌细胞群。患者中 C1 和 C0 细胞聚类的中位比例分别为 65.52%(0–100%)和 18.59%(0–53.78%)(图3d)。44 号患者在接受化疗免疫治疗后达到完全缓解,治疗后未检测到癌细胞。此外,大多数肿瘤样本包含多个癌细胞聚类,在 39 个样本中的 28 个(71.79%)中检测到了 SCLC-A 和 SCLC-N 细胞群(图3e)。肝细胞核因子4α (HNF4A)是神经内分泌癌,尤其是胃肠道神经内分泌癌的一个新兴标志物。然而,HNF4A在癌细胞中的表达相对较低。此外,与正常上皮细胞相比,癌细胞聚类表现出更高的拷贝数变异(CNV)负荷,这与恶性表型相符。
C18聚类表达与干细胞和癌症起始细胞特征相关的基因,包括活化白细胞黏附分子(ALCAM)/CD166、Musashi 2 (MSI2)、SRY-box 转录因子2 (SOX2)、SOX1、胰岛素样生长因子结合蛋白 5 (IGFBP5)、L-Myc (MYCL)、prominin-1 (PROM1)/CD133、转录因子3(TCF3)以及神经内分泌标志物嗜铬粒蛋白A(CHGA)(图3c)。基因集富集分析 (GSEA) 显示,与其他类型的癌细胞相比,SLC显著富集 MYC 靶基因和 WNT-β-catenin 通路基因(图3f)。这些结果为进一步的功能研究提供了证据,以验证所鉴定通路的生物学意义。与其他细胞聚类相比,SLC的多能性评分最高(图3g)。SLC 包含 1771 个细胞,占每位患者所有癌细胞的 0% 至 25.78%。在一例确诊三天后死亡的 IV 期患者(#P26)中,SLC 占 2207 个癌细胞中的 569 个(25.78%)。在两例接受新辅助治疗的患者中,SLC 占治疗后肿瘤样本的 10% 以上。在39例患者中,27例(69.2%)检测到SLC,其中SCLC-A亚型23例,SCLC-N亚型3例,SCLC-Y亚型1例。28例男性患者中有16例(57.1%)SLC阳性,11例女性患者中有11例(100%)SLC阳性;22例吸烟者中有12例(54.5%)SLC阳性,17例非吸烟者中有15例(88.2%)SLC阳性。
他们采用“加权最近邻”方法对上皮细胞的身份基因标记进行了富集分析,发现除SCLC- YAP1细胞外,几乎所有癌细胞均表现出神经内分泌富集评分(图3h)。此外,SCLC-A和SCLC-Y细胞的聚类1、13、17、8和4呈现出中等至强的棒状细胞和弱的基底细胞评分(图3h),提示SCLC可能具有不同的起源。然而,研究表明,在肺发育过程中,Notch信号通路通过阻断前体细胞分化为神经内分泌细胞,并通过RE1沉默转录因子(REST)和YAP1促进神经内分泌细胞向棒状细胞转化,从而诱导神经内分泌向非神经内分泌的转换。因此,这些结果提示SCLC可能仍然起源于共同的祖细胞。
他们分析了不同疾病阶段的SCLC细胞聚类,发现SCLC-A- MKI67和SCLC-A -CRIP2细胞聚类在I-II期和III-IV期均较高,且在新辅助治疗后显著降低,同时AT2细胞显著增加。在治疗前样本中,SCLC-A- MKI67细胞聚类占每位患者所有癌细胞的20.93%;在治疗后样本中,该细胞聚类消失(图3i),证实了初始治疗的临床疗效。SCLC-A- CRIP2细胞聚类在治疗前样本中占所有癌细胞的69.08%(范围:0%–96.82%),在治疗后样本中占所有癌细胞的33.33%(范围:0%–100%)(图3i),提示其可能在耐药性和复发中发挥作用。在新辅助治疗后,达到 PR/CR 的患者中 SCLC-A-MKI67细胞的比例低于达到 SD/PD 的患者,并且 PR/CR 组中非癌细胞的比例高于 SD/PD 组(图3j)。
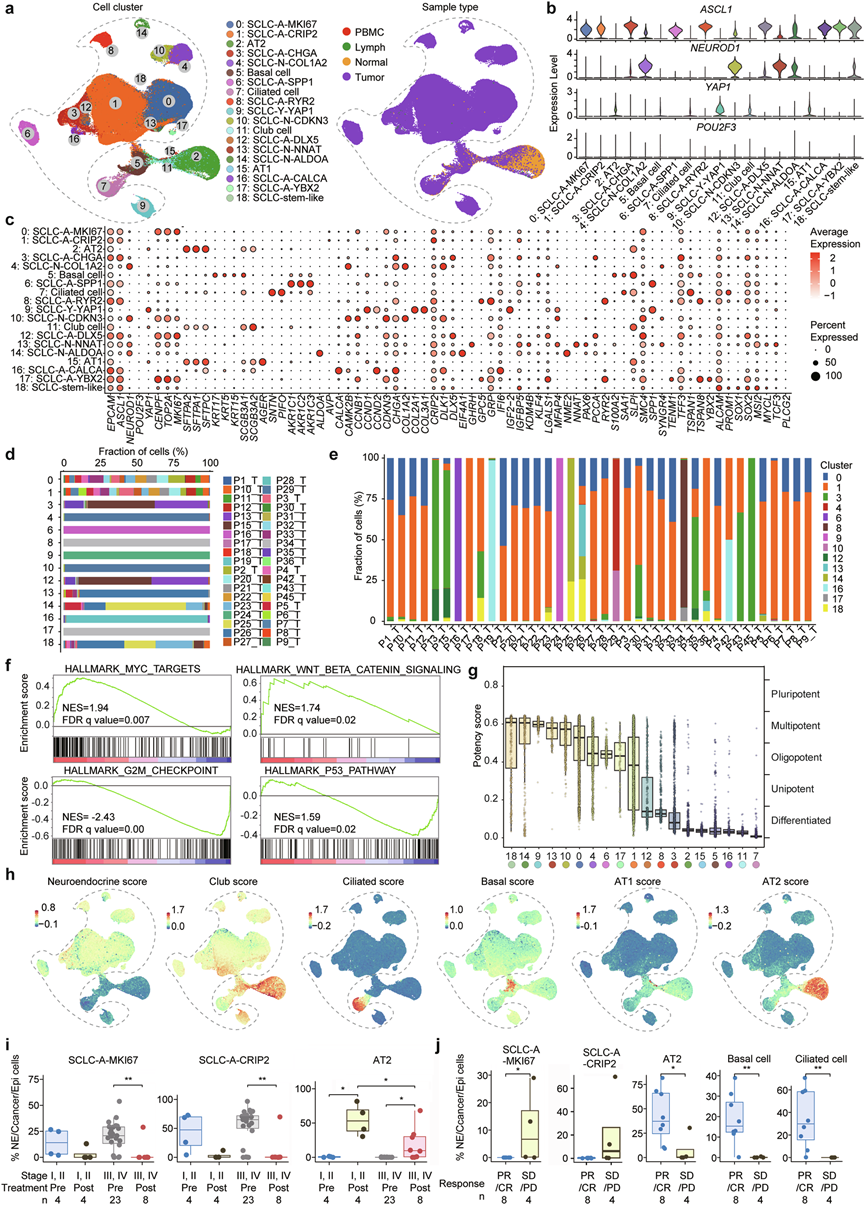
图3. SCLC中的癌细胞和癌症干细胞样细胞。
(a) 通过分析癌细胞和非免疫正常细胞,确定了 19 个细胞聚类(左图)。右图显示了不同样本类型中的细胞分布。(b-c) 细胞聚类中特征基因的表达。(d) 14 个癌细胞聚类中肿瘤样本的相对比例。(e) 39 个肿瘤样本中不同肿瘤细胞聚类的分布。(f) 干细胞样细胞聚类和其他癌细胞聚类中所示基因集的基因集富集分析 (GSEA) 图。(g) 通过CytoTrace算法评估 19 个细胞聚类的潜能和分化状态。(h) 肺组织中 SCLC 潜在细胞来源的富集分数。(i-j) 所示细胞聚类在不同阶段和新辅助治疗结果的比较。
04
主要组织相容性复合体成分的异质性表达
他们分析了SCLC中的抗原加工和呈递(APP)通路,发现大多数癌细胞中通过主要组织相容性复合体I类(MHC-I)和MHC-II的APP表达显著受到抑制(图4a),这与之前的报道一致。他们分析了每个细胞聚类中的MHC-I评分,结果显示,HLA-A、HLA-B和HLA-C在癌细胞聚类13、0、9、1、6和18中的表达较低;在聚类14、4和10中的表达中等;在聚类8、17、3、12和16中的表达较高(图4b),表明SCLC细胞群体中MHC-I的表达存在异质性。MHC-I高表达聚类的总数为19191个,占所有SCLC癌细胞的10.08%。为了验证上述发现,他们分析了空间蛋白质组学数据,发现一部分EPCAM+癌细胞也表达HLA-A(图4c),中位比例为5.79%(图4d)。一部分EPCAM+癌细胞表达HLA-DRA(图4e),中位比例为10.28%(图4d)。然而,EPCAM+KI67+细胞HLA-A和HLA-DRA均为阴性(图4f)。他们通过SCLC蛋白质组学数据分析了MHC组分与MHC-I低表达或高表达细胞聚类的标志基因之间的潜在关联,发现MKI67的表达水平与MHC-I和MHC-II分子的表达水平呈负相关(图4g)。因此,SCLC细胞聚类中MHC表达的异质性以及MKI67在MHC-I和MHC-II调控中的作用值得进一步研究。
几乎所有癌细胞聚类中MHC-II分子的表达均较低(图4b)。MHC-II分子,特别是HLA-DQB1,在几乎所有T/NK细胞聚类中表达均较低,而HLA-DRA和HLA-DRB1在T/NK细胞聚类1和8中表达较低。HLA-DRA、DRB1和DQB1在巨噬细胞/单核细胞聚类1中也表达较低(图4b)。通过CellChat方法进行的细胞间相互作用分析显示,在39例患者中,癌细胞与T/NK细胞/巨噬细胞之间通过MHC-I和MHC-II的相互作用概率较低。单细胞空间蛋白质组学分析显示,早期SCLC患者肿瘤组织中HLA-A和HLA-DR的表达水平均高于晚期SCLC患者(图4h-i)。治疗前癌细胞中HLA-A/HLA-DR表达水平较高的患者对新辅助治疗的反应更好,且治疗有效者的HLA-A/HLA-DR表达水平高于治疗无效者(图4h-j)。位于肿瘤中心的癌细胞HLA-A染色较弱,而位于肿瘤边缘的癌细胞染色较强,且周围环绕着免疫细胞(图4k)。
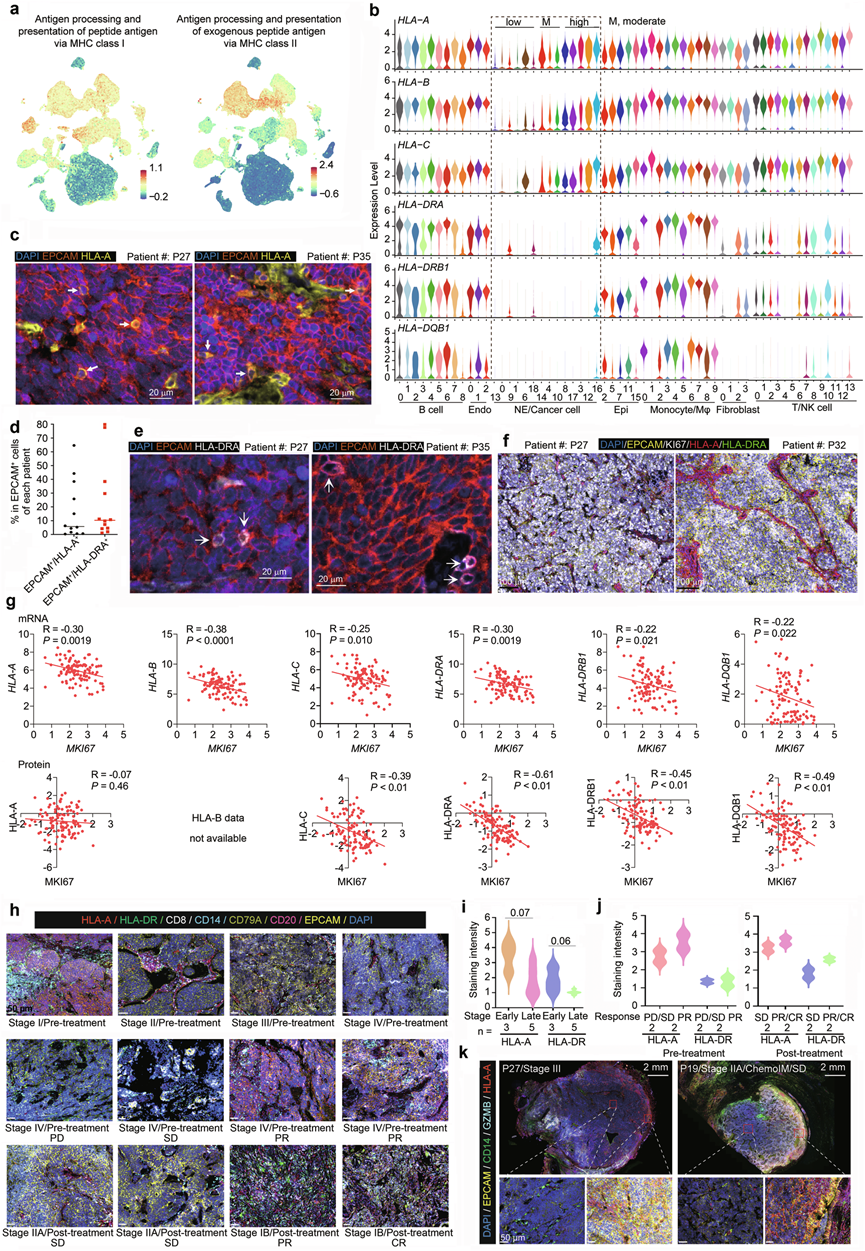
图4. SCLC 中的抗原加工和呈递 (APP) 机制。
(a) UMAP显示通过 MHC-I 和 MHC-II 富集与 APP 相关的基因。(b) 所示细胞聚类中 MHC 分子的表达。(c-e) EPCAM+癌细胞上 HLA-A 和 HLA-DRA 的表达。(f) EPCAM+ KI67 +癌细胞中HLA-A和HLA-DRA的表达。(g) SCLC中KI67与MHC成分表达水平的相关性。(h-j) 癌细胞和免疫细胞中HLA-A/HLA-DR的表达。(k) 位于肿瘤中心和边缘的癌细胞和免疫细胞中的HLA-A表达。
05
结构异常和高频剪接变异
他们使用STAR-Fusion 52和FusionInspector工具检测融合基因,排除正常样本中发现的融合基因,最终获得32个候选融合基因。其中9个(ARID1B-ZDHHC14、CSNK1D-CCDC57、CTNNBIP1-CLSTN1、DNER-PID1、EIF4G3-ECE1、MED20-USP49、PSMB7-NR6A1、TIRAP-DCPS和TPD52L2-DNAJC5)已在之前的研究中报道过。其余23个融合基因包含完整的启动子和终止子,可用于蛋白质翻译。利用 RT-PCR 和可用的肿瘤样本,他们验证了ARID1B-ZDHHC14和CSNK1D-CCDC57,表明它们具有潜在的生物学相关性,值得进一步研究。
为了进一步阐明SCLC的内在改变,他们利用RNA-seq数据分析了ASE,鉴定出存在于肿瘤组织而非正常肺组织中的剪接变异。在45个SCLC样本中,18268个基因表现出ASE,其中3092个具有显著性。这些事件包括跳跃外显子(SE)、5'端可变剪接位点(A5SS)、3'端可变剪接位点(A3SS)、互斥外显子(MEE)和内含子保留(RI)。最常见的ASE是SE,在18268个受影响的基因中,有18029个(98.7%)基因存在SE。在45例患者中,分别有1971、1024、267、219和409个显著基因与SE、MEE、A3SS、A5SS和RI相关。
包括CD47、CLSTN1、DLG1、EEF1D和FAK/PTK2在内的16个基因(图5a)在所有 45 例患者中均表现出ASE(图 5a)。选择FAK剪接变体进行进一步研究,是因为这些变体在非小细胞肺癌 (NSCLC) 中出现频率相对较低,但在小细胞肺癌 (SCLC) 中未见报道。此外,FAK 抑制剂对 SCLC 细胞具有抑制作用,并且在 I 期临床试验中,接受 PF562271 治疗的 1 例患者均实现了病情稳定。在 SCLC 中,编码自磷酸化位点 Y397 的密码子两侧分别插入了两个额外的剪接盒,长度分别为 18 bp(盒 6)和 21 bp(盒 7),分别命名为FAK 6、FAK7和FAK6,7(图5b)。在 FAK 6中,插入了六个氨基酸,原有的 Y397 残基变为 Y403;在 FAK 7和 FAK 6,7中,分别在 Y397 之后插入了一个额外的酪氨酸残基 Y414 或 Y420(图5b)。肿瘤组织中含有 Box 6 和 Box 7 的FAK转录本的剪接百分比 (PSI) 值远高于正常肺组织中的值(图5c)。在本队列中,合并 SCLC 患者的样本量较小,且合并 SCLC 患者的 FAK 6/7水平似乎与 SCLC 患者相当。然而,当纳入其他队列的RNA-seq 数据后,他们发现纯 SCLC 患者中检测到的 FAK 剪接变体数量多于合并 SCLC 患者。
为了评估这些ASE对FAK功能的潜在影响,他们使用AlphaFold2预测了FAK的结构。野生型(WT)FAK结构。与相应的晶体结构相比,FERM结构域和激酶结构域的Cα均方根偏差(RMSD)值分别为1.046 Å和0.983 Å。预测的FAK结构呈现自抑制构象(图5d),这与之前的报道一致。在该构象中,位于连接区并夹在FERM结构域和激酶结构域之间的Y397远离激酶结构域的激活环(A环)(图5d)。在FAK6中,Box 6的插入发生在Y403的N端,远离激酶结构域,提示其对自身磷酸化的影响可能很小(图5e)。在FAK7和FAK6,7中,Box 7的插入增加了Y397 C端环的长度,使其具有更大的构象自由度,并可能促进FAK7中Y397和FAK6,7中Y403的自身磷酸化(图5f-g)。此外,FAK7和FAK6,7中额外的酪氨酸残基可能作为额外的磷酸化位点(图5f-g),从而增强激酶活性,并可能在SCLC的发生发展中发挥重要作用。
他们在另外 109 例SCLC样本中验证了FAK变体,利用 RT-PCR 和后续的 Sanger 测序,他们对 37 例肿瘤-正常配对患者组织样本进行了分析),发现正常肺组织中仅检测到野生型FAK(图5h)。在 37 例肿瘤样本中,6 例 (16.2%) 仅显示FAK条带,4 例 (10.8% )显示两条条带(FAK和FAK6或FAK7),27 例 (73%) 显示三条条带(FAK、FAK6 / FAK7和FAK6,7)(图5h)。
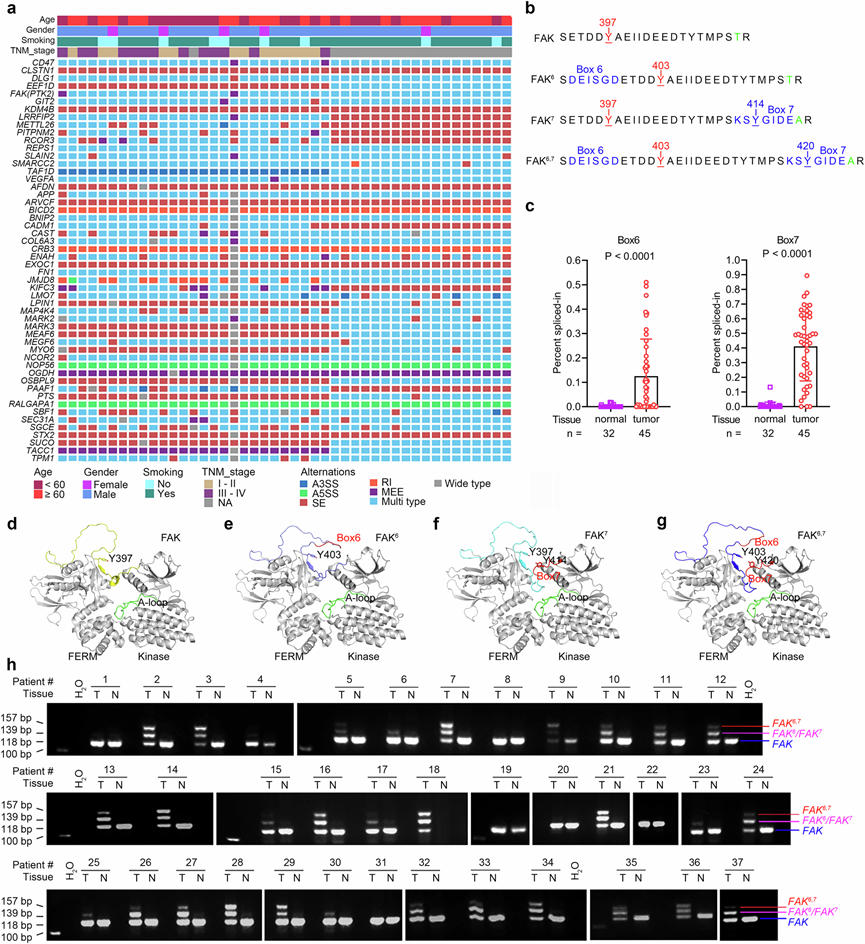
图5. SCLC 中的高频可变剪接基因。
(a) 45 个 SCLC 中最常受影响基因中的可变剪接事件(ASE)。(b) FAK、FAK 6、FAK 7和 FAK 6,7的排列。(c) 肿瘤和对应正常肺组织中含有 Box 6 和 Box 7 的 FAK 转录本的剪接百分比 (PSI) 值。(d-g) FERM和激酶结构域。(h) 通过 RT-PCR 在 37 名患者的配对肿瘤-正常样本中检测到FAK变体。
06
小细胞肺癌中的FAK剪接变异
在正常对照组织中,未检测到FAK的替代剪接(图5h),这促使他们通过RT-PCR分析进一步研究福尔马林固定石蜡包埋(FFPE)样本中的FAK剪接变体。他们发现,27例(27.3%)、10例(10.1%)和62例(63.6%)患者分别携带FAK+、FAK6 /FAK 7和FAK 6,7(图6a)。
为了可视化FAK剪接变体的单个 RNA 分子,他们对 56 个 FFPE 样本进行了 BaseScope 双重检测,这些样本已使用针对 Box 6 和 Box 7 的探针通过 RT-PCR 进行了检测。在 13 个 RT-PCR 检测FAK呈阳性的样本中,未检测到 Box 6 或 Box 7 信号;在 5 个FAK6 / FAK 7样本中,检测到了 Box 6(蓝色)和 Box 7(红色)信号;在 35 个FAK6,7样本中,检测到了 Box 6(蓝色)和 Box 7(红色)信号,以及FAK6,7(重叠信号)(图6b)。
为了确定 FAK ASE 是否在特定的 SCLC 亚型中富集,他们分析了FAK剪接变异体与四种潜在 SCLC 亚型之间的潜在关联。在 68 例ASCL1+ SCLC 中,65 例(95.6%) 存在FAK变异体;在 50 例NEUROD1+SCLC 中,45 例 (90%) 存在 FAK 变异体;在 12 例POU2F3+SCLC 中,6 例 (50%) 存在 FAK 变异体;在 24 例YAP + SCLC中,3 例 (12.5%) 存在FAK 变异体(图6c),表明 FAK 剪接变异体主要与ASCL1+和NEUROD1+SCLC 亚型相关。
他们使用针对磷酸化Y397(存在于FAK和FAK7中)或Y403(存在于FAK6和FAK6,7中)的抗体,通过IHC检测了FFPE样本中磷酸化FAK(p-FAK)的表达。结果显示,FAK6 /FAK7患者的p-FAK水平高于FAK单突变患者,而FAK6,7患者的p-FAK染色水平最高(图6d)。与此一致的是,FAK6,7患者的免疫反应评分(IRS)最高(中位数为12),其次是FAK6 /FAK7患者(中位数为9),最后是FAK单突变患者(图6e)。在这些患者中,p-FAK主要定位于细胞质,但也观察到核内p-FAK,尤其是在FAK6,7和FAK6/FAK7双阳性患者中(图6d)。Western blot分析证实,FAK6,7双阳性患者的p-FAK表达水平高于FAK单阳性患者(图6f)。
为了验证携带 FAK 剪接变体的患者中核内 p-FAK 表达增加,他们对SCLC细胞系进行了亚细胞分级分离分析。结果发现,与表达 FAK 的 H1339 和 DMS114 细胞相比,表达 FAK6,7 的 H524 和 H82 细胞系中核内 p-FAK 表达增加(图6g)。此外,与转染 FAK 的细胞相比,瞬时转染FAK7和FAK6,7 的DMS114 细胞中也检测到了核内 p-FAK 表达增加(图6h)。鉴于核内FAK能够调节趋化因子CCL5、CCL10、CCL1、CCL7和CXCL13、白细胞介素6 (IL6)、IL33、凋亡调节因子BCL2以及原癌基因MYC和MDM2的表达,他们检测了FAK变体对这些基因在野生型FAK阳性的DMS114和H1339细胞中的潜在影响,这些细胞已转染了FAK或FAK转录本。通过qPCR,他们发现FAK和FAK6,7均能上调这些基因的表达;在这些细胞中,FAK6,7对CCL7、CXCL13和BCL2的影响显著大于FAK(图6i)。
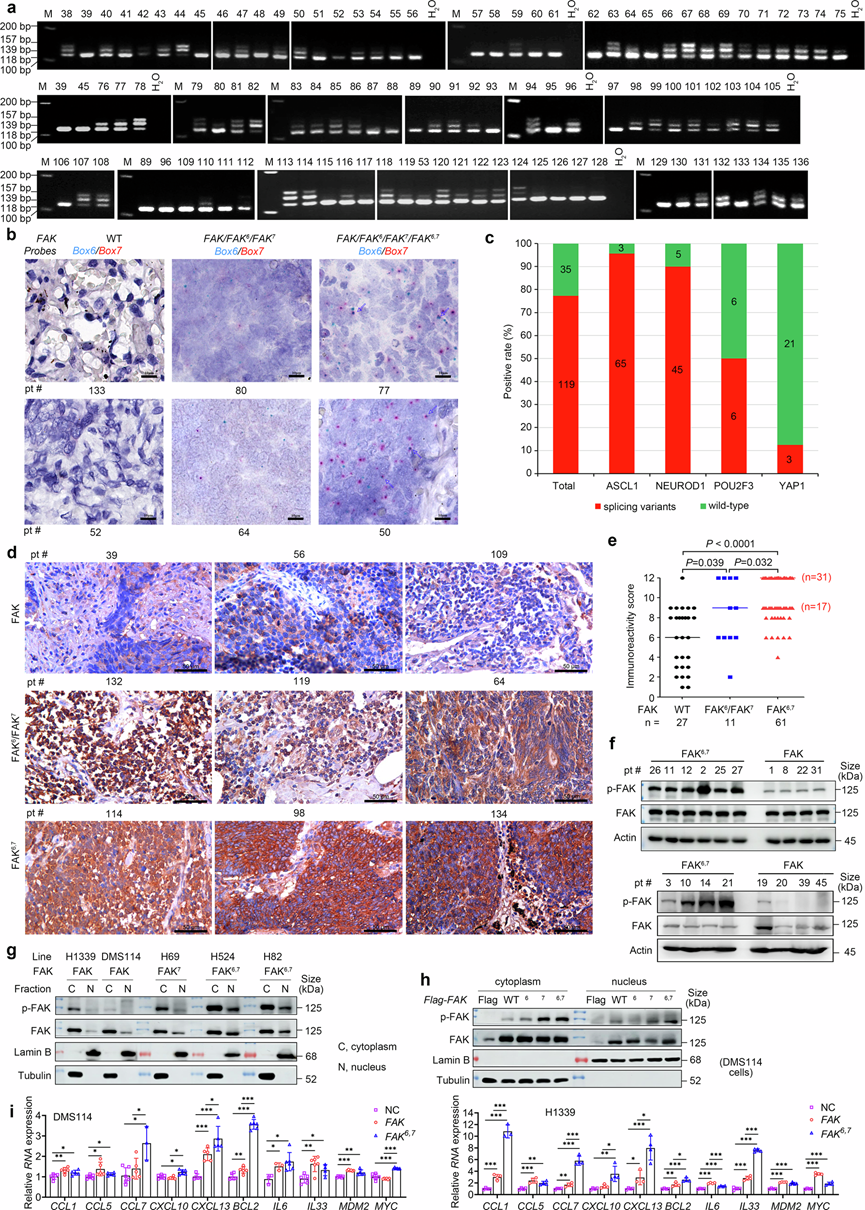
图6. 另外 99 例 SCLC 患者中的 FAK 剪接变异体。
(a) 通过RT-PCR 检测到的患者肿瘤组织中的 FAK 变异体。(b) 通过 原位杂交 BaseScope Duplex 检测检测到的肿瘤组织中 FAK 变异体的代表性结果。(c) 不同亚型SCLC中FAK剪接变异体的阳性率。(d) 通过 IHC 检测检测到肿瘤组织中FAK变异体患者的 p-FAK 代表性结果。(e) FAK剪接变异体患者的免疫组织化学检测免疫反应评分。(f-h)免疫印迹分析。(i) 分离 RNA 样本进行定量 RT-PCR。
07
FAK剪接变体与小细胞肺癌预后不良相关
他们分析了FAK变异与可获得生存信息的患者预后之间的潜在关联,其中包括24例FAK-/-患者、10例FAK6/FAK7患者和60例FAK6,7患者。与携带FAK剪接变异的患者相比,携带FAK剪接变异的SCLC患者的预后显著更差(图7a),提示FAK可变剪接变异可能在SCLC的发病机制中发挥关键作用。
由于这些细胞系已建立数十年且存在明显的局限性,他们检测了PF562271对患者来源类器官(PDO)和患者来源异种移植(PDX)模型的影响。利用随机获得的样本建立了三个SCLC PDO,其中两个携带FAK6,7突变(图7c)。PF562271对FAK6,7突变PDO的生长有轻微抑制作用,但对FAK6,7突变PDO的生长有显著抑制作用(图7c)。他们测试了PF562271对携带FAK6,7突变PDX模型的影响(图7d)。在PDX模型1中,该模型来源于一名携带FAK 6,7突变以及TP53和Rb1基因突变的男性患者,相对低剂量(50 mg/kg)的PF562271可显著抑制肿瘤生长达73.5%(图7d-e),并使肿瘤重量减轻75%(图7f)。IHC分析显示,PF562271显著下调了p-FAK和Ki67的表达(图7g-h)。通过对肿瘤样本裂解液进行Western blot分析,证实了PF562271治疗小鼠中p-FAK的下调(图7i)。在源自FAK6,7突变、TP53和Rb1突变女性患者的PDX模型2中,PF562271显著抑制了肿瘤生长(图7j-k),降低了肿瘤重量(图7l),并抑制了p-FAK和Ki67的表达(图7m-o)。此外,在H82异种移植小鼠模型中,50 mg/kg/天剂量的PF562271抑制了肿瘤生长,而150 mg/kg/天的剂量则有效抑制了肿瘤生长,并显著降低了p-FAK和Ki67的水平(图7p-u)。
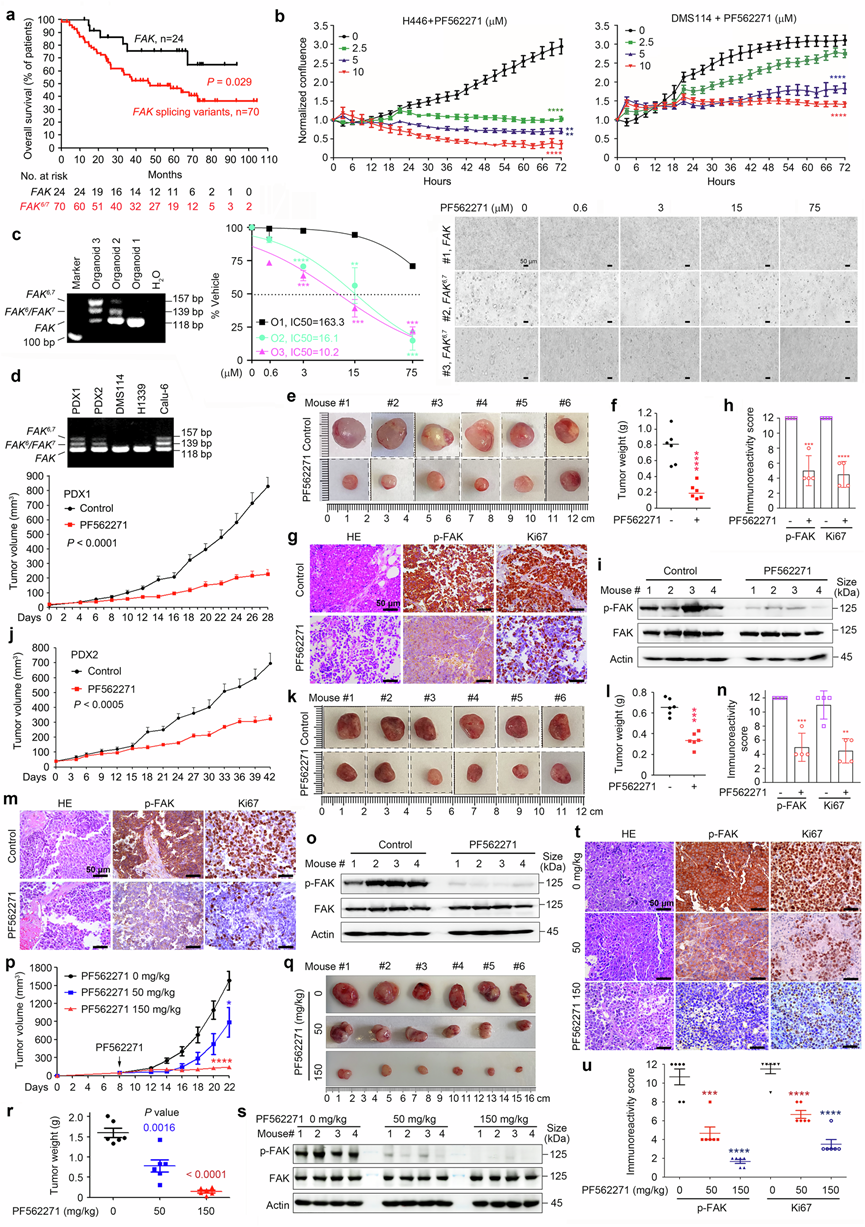
图7. FAK剪接变体在SCLC中的临床意义。
(a) 野生型FAK和剪接变体SCLC患者的OS。(b) 用2.5至10 μM PF562271处理H446和DMS114细胞,并用IncuCyte活细胞分析系统监测。(c) CCK-8测定法量化类器官细胞活力。(d) 通过 RT-PCR 检测两种患者来源的异种移植 (PDX) 模型中的FAK ,以及分析肿瘤体积。(e) 从小鼠中分离的异种移植肿瘤图像。(f) 从小鼠中分离的异种移植肿瘤重量。(g-h) 苏木精-伊红 (HE) 染色和 IHC 检测的代表性图像,以及免疫反应评分。(i) 免疫印迹分析。(j) 肿瘤体积分析。(k) 从小鼠身上分离的异种移植肿瘤图像。(l) 从小鼠身上分离的异种移植肿瘤重量。(m) HE 染色和 IHC 检测的代表性图像。(n) 计算 p-FAK 和 Ki67 的免疫反应性评分。(o) 免疫印迹分析。(p) 肿瘤体积分析。(q) 从小鼠中分离出的异种移植肿瘤图像。(r) 从小鼠中分离出的异种移植肿瘤的重量。(s) 免疫印迹分析。(u) 通过IHC分析结果计算p-FAK和Ki67的免疫反应性评分。
08
除RB1和TP53外,还鉴定出11种高频突变
为了研究肠道菌群在SCLC中的潜在作用,他们对53例患者的肿瘤邻近正常肺组织配对样本进行了16S rRNA基因测序。结果显示,肿瘤组织和正常肺组织中细菌DNA的比例、肠道菌群α多样性指数以及整体肠道菌群组成均无显著差异。在肿瘤组织和正常组织中,变形菌门、厚壁菌门和拟杆菌门均为优势菌门,而乳杆菌属、不动杆菌属和甲基杆菌属则是优势菌属。此外,肿瘤组织微生物群的差异与肿瘤分期或吸烟状况。
在111例患者中,TP53和RB1分别在78例(70.3%)和53例(47.7%)中发生突变(图8a)。WES和RNA-seq数据显示,在Rb1野生型肿瘤(n = 18)中,Cyclin D1、Cyclin D2和Cyclin D3的表达略高于Rb1突变型肿瘤。在TP53野生型肿瘤(n = 10)和TP53突变型肿瘤中,Cyclin D1、Cyclin D2和Cyclin D3的表达无显著差异。这些结果表明,SCLCp53 和 Rb1 通路可能存在其他改变,值得进一步研究。
核苷酸变化分析显示,C:G→A:T颠换和C:G→T:A转换是最常见的核苷酸替换,吸烟者的替换率高于非吸烟者(图8b)。在吸烟者中,C:G→T:A转换的平均数量(每Mb 6.71个)高于C:G→A:T颠换的平均数量(每Mb 5.95个)。此外,这些患者的平均C:G→G:C颠换(烟草致癌物1,3-丁二烯的特征突变)和平均T:A→A:T颠换(空气污染物氯乙烯的特征突变)也较高(图8b-c)。T:A→C:G 转换通常由烟草致癌物 N-亚硝基二乙胺和一种广泛使用的合成工业化学品 1,4-二恶烷诱导,导致吸烟者中每兆碱基发生 3.11 个突变,非吸烟者中每兆碱基发生 1.83 个突变。他们分析了每位患者中每个突变碱基的 5' 和/或 3' 序列环境中的核苷酸替换,发现特征 4(多环芳烃暴露的特征)在吸烟者和非吸烟者中均是最常见的特征。特征 5、24、39 和 87 在这些患者中也相对较高。
利用非负矩阵分解算法和突变模式数据,他们获得了四种新的突变特征A、B、C和D(图8d),这些特征与各种内在或外在因素相关的特征相似。特征A主要由C>T突变和极少的C>A颠换组成。特征B的特征是突变分布于所有96种碱基替换亚型中,其中C>T、C>G和T>A突变的水平相对较高。特征C表现出较高比例的C>T和T>C突变,而特征D的特征是除其他5种突变类型外,还存在C>A替换(图8d)。根据这些新发现的特征,将111 名患者分为四组:第 1 组(12 名患者,10.8%)的特征是特征 A,第 2 组(10 名患者,9%)的特征是特征 B,第 3 组(38 名患者,32.2%)的特征是特征 C,第 4 组(51 名患者,45.9%)的特征是特征 D(图8c)。他们根据选定环境因素的突变特征以及暴露于烟草相关化合物(如苯并[a]芘-7,8-二氢二醇-9,10-环氧化物 (BPDE)/BaP、二苯并[a,j]吖啶 (DBAC)、甲基丁香酚、二苯并[a,h]蒽 (DBA) 和甲醛)的证据,分析了这些患者基因组中的核苷酸替换情况。对突变谱及其基因组体细胞突变比例的分析显示,吸烟者和非吸烟者之间的环境特征相似,提示非吸烟者可能暴露于二手烟和空气污染物。
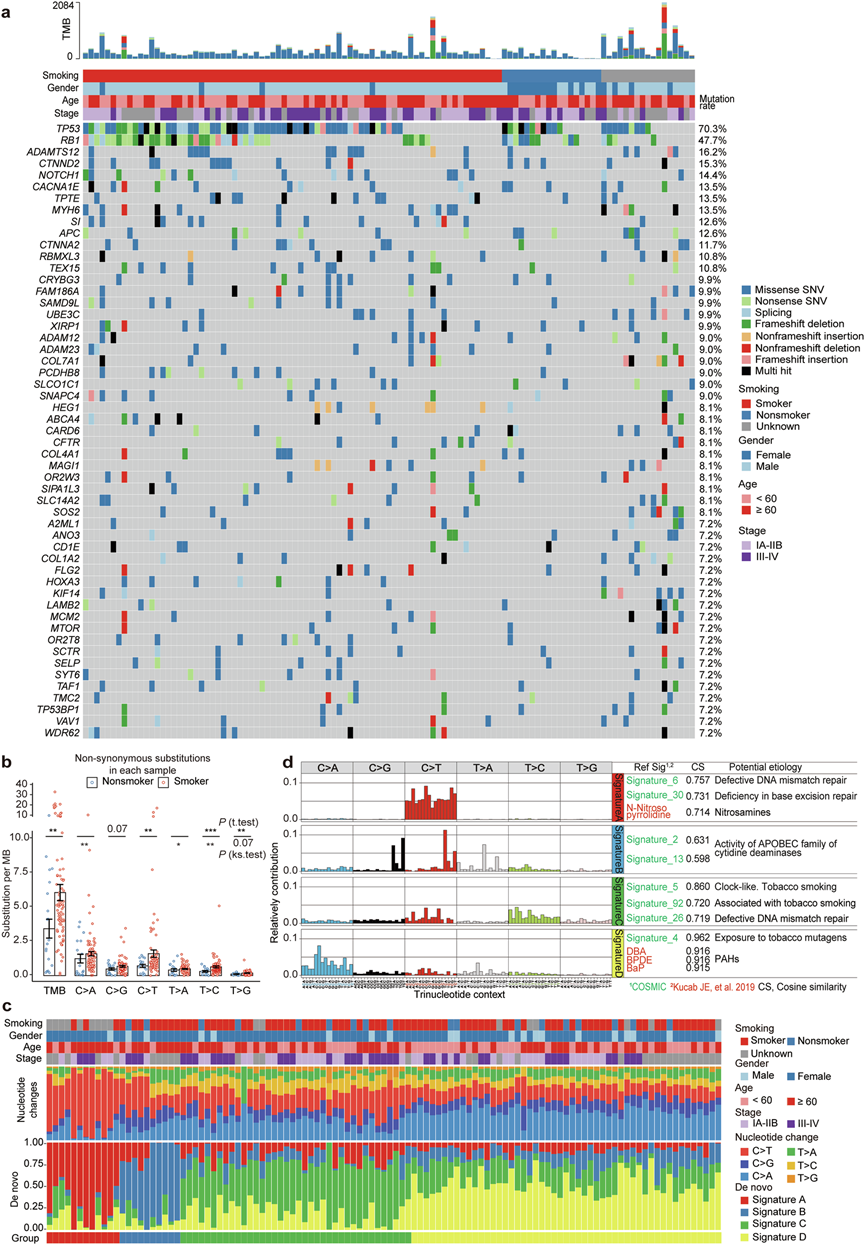
图8. 小细胞肺癌(SCLC)中的体细胞外显子突变和致癌物特征。
(a) SCLC中的体细胞外显子突变。(b) 吸烟者和非吸烟者的核苷酸替换。(c-d) 每位患者的核苷酸变化。
+ + + + + + + + + + +
结 论
本研究通过对314例SCLC样本进行多组学分析,发现ASCL1+ / MKI67+和ASCL1+/ CRIP2+细胞聚类占39例患者共190313个SCLC癌细胞的74.38%,而ASCL1+SOX1+干细胞样细胞聚类则存在于所有SCLC亚型中。MHCI类分子在6个癌细胞聚类中低表达,在5个癌细胞聚类中高表达,且MHC I类分子的表达水平与KI67的表达水平呈负相关。mRNA异常剪接是SCLC的特征之一,在154例患者中,119例(77.3%)检测到FAK剪接变异。FAK变异表现出激酶活性升高,预后最差,并且在患者来源的类器官和异种移植模型中对FAK抑制剂敏感。除TP53和RB1外,还发现了11种高频突变,吸烟状况和肿瘤分期不影响SCLC患者的肠道菌群变异。综上所述,本研究的数据进一步揭示了复杂的肿瘤内异质性,并发现FAK剪接变异代表了SCLC癌基因的高频功能获得性改变,是这种难治性癌症的潜在治疗靶点。
+ + + + +



 English
English


