文献解读|Nat Commun(15.7):一项纵向队列研究揭示了类风湿性关节炎临床发病和治疗反应之前的血浆蛋白生物标志物
✦ +
+
论文ID
原名:A longitudinal cohort study uncovers plasma protein biomarkers predating clinical onset and treatment response of rheumatoid arthritis
译名:一项纵向队列研究揭示了类风湿性关节炎临床发病和治疗反应之前的血浆蛋白生物标志物
期刊:Nature Communications
影响因子:15.7
发表时间:2025. 07.21
DOI号:10.1038/s41467-025-62032-1.
背 景
类风湿关节炎 (RA) 是一种持续性、进行性全身炎症性疾病,主要影响关节。了解其病因、亚型异质性、诊断性生物标志物和最佳治疗靶点面临巨大挑战,因为不同疾病阶段具有不同的致病特征。RA发病的关键前奏是“高危”期,其特征是自身抗体水平升高。研究这一高危期对于揭示疾病发展的细微差别以及确定预防或减轻其影响的干预措施至关重要。
实验设计
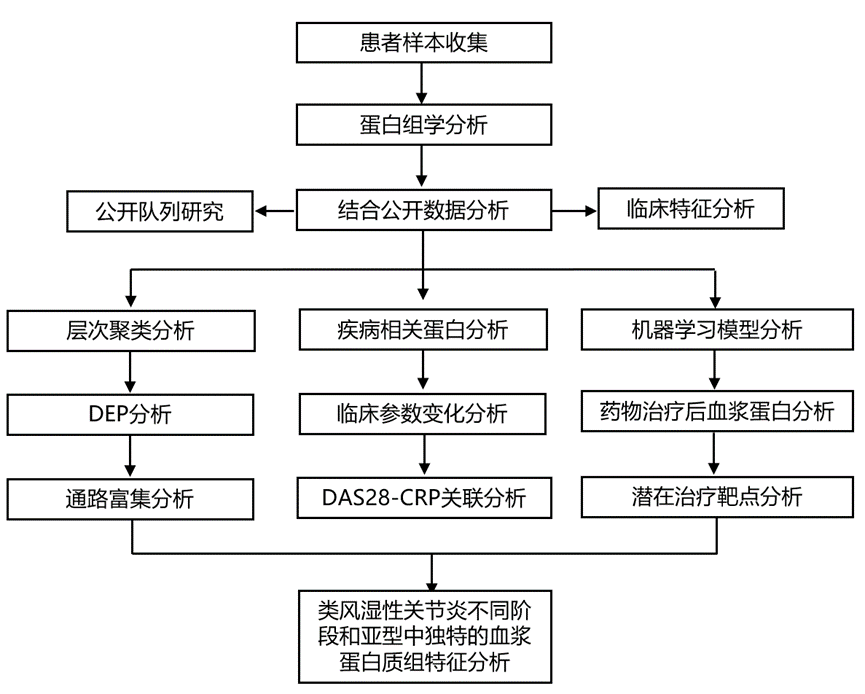
结 果
01
高风险、抗瓜氨酸化肽自身抗体(ACPA) 阳性和 ACPA 阴性 RA 个体的蛋白质组学特征
研究团队从中国西部地区招募了 278 名 RA 患者,其中女性 231 名(83%)(图 1a-b)。RA 患者平均年龄为 51 岁,范围为 16 岁至 77 岁。28 个关节的疾病活性评分与 C 反应蛋白(DAS28-CRP)从 1.24 到 8.39 不等,平均值为 3.53。ACPA 阴性个体年龄稍大,平均年龄为 52 岁(ACPA 阳性 RA 患者为51 岁),DAS28-CRP 评分较低,为 3.07(ACPA 阳性 RA 患者为 3.71)。纳入研究的患者在采集血浆样本前至少 6 个月未接受过 传统的合成抗风湿药物 (csDMARD)治疗。在有随访数据的 206 例 RA 患者中,140 例在接受甲氨蝶呤(MTX)单药治疗或 csDMARD 联合治疗后,于 3-6 个月时进行了一次随访,59 例在 6-9 个月时进行了两次随访。此外,他们招募了 60 名风险个体,其中 38 例随访了 5-7 年,以及 99 名健康对照者进行比较分析。健康对照者平均年龄为 51 岁,范围为 38-76 岁(79 名女性和 20 名男性)。60 名风险个体的平均年龄为 48 岁(32 名女性和 28 名男性),范围为 29 至 74 岁。
接下来,他们对这些血浆样本进行了蛋白质组学分析(图 1a),观察到的标准化蛋白质丰度分布的稳定性也表明批次效应最小(图 1c)。分别从 RA 患者、高危个体和健康个体中鉴定出 2504、2022 和 1924 种蛋白质(图 1d)。每组个体中超过 50% 的样本中定量的蛋白质,总计 996 种血浆蛋白,用于后续数据分析。
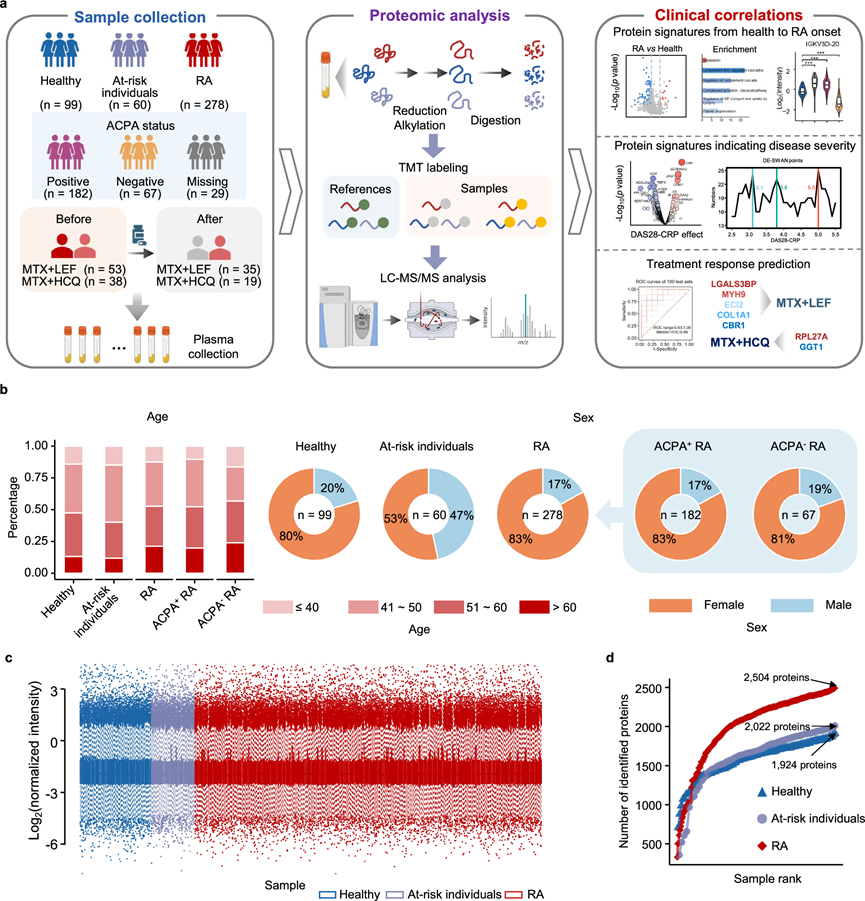
图1. 蛋白质组学分析工作流程和质量控制。
(a) 研究示意图。(b) 条形图(左)和饼图(右)描绘了不同临床亚组中年龄和性别组的分布。(c)蛋白质强度分析。(d) 已鉴定蛋白质数量。
02
从健康到类风湿性关节炎发病期间血浆蛋白质组的波动
他们最初对 182 名 ACPA 阳性 RA 患者、67 名 ACPA 阴性 RA 患者、60 名高危个体和 99 名健康对照者的血浆蛋白质组数据进行了层次聚类(图 2a),揭示了这些组之间的明显区别(图 2b)。比较分析确定了 ACPA 阳性 RA 患者、ACPA 阳性 RA 患者、高危个体和健康对照者之间的许多差异表达蛋白质 (DEP) 和通路(图 2c)。然后,他们结合了健康组和其他组之间不同的蛋白质,并进行了通路富集分析(图 2c)。该分析表明,在 ACPA 阳性 RA 患者和高危人群中,与中性粒细胞脱颗粒、细胞应激反应和可溶性外源抗原交叉呈递相关的蛋白质均上调。然而,ACPA 阳性 RA 患者表现出更强烈的免疫和急性期反应(图 2c)。相反,下调的蛋白质主要参与代谢失调、氧化还原过程(如过氧化氢分解代谢)和蛋白质加工,表明内质网应激增加。值得注意的是,高危人群中特异性升高的蛋白质与 RNA 代谢有关,而 RNA 代谢与炎症有关。此外,他们观察到ROBO受体信号的上调,这会抑制成骨分化和轴突导向通路,已知这两者在RA中均上调(图 2c)。
虽然ACPA阳性和ACPA阴性类风湿性关节炎患者在临床特征、病情进展和治疗反应方面存在差异,但其蛋白质组谱的差异仍不清楚。他们观察到ACPA阳性类风湿性关节炎患者的炎症反应更强烈,即使在校正了DAS28-CRP水平后,这种炎症反应在两组患者之间仍然显著。这些发现表明,炎症反应增强是ACPA阳性表型的内在效应,与疾病活性无关。自身免疫性疾病可能具有共同的致病机制。因此,他们研究了RA患者中富集最多的蛋白质是否也在其他自身免疫性疾病患者(包括原发性干燥综合征、系统性硬化症、特发性炎症性肌病和系统性红斑狼疮)中与健康对照组相比出现异常表达。结果证实了这些 DEP 的类风湿性关节炎特异性,因为大多数 DEP在其他自身免疫性疾病患者和健康对照组之间没有显著差异。与其他组相比,ACPA 阳性 RA 组的大多数 DEP 与性别无关,均表现出中性粒细胞脱颗粒、补体级联调节和急性期反应增加的共同趋势。与 RA 患者相比,高危人群表现出更高水平的 ROBO 受体信号传导和 RNA 代谢,且男性的 RNA 代谢更高。相反,男性 RA 患者的轴突引导更为明显,表明骨重塑压力增加。ACPA阴性 RA 患者的脂质代谢明显增加,尤其是男性的脂肪酸 β-氧化升高。类风湿性关节炎的临床前期是确定致病机制和潜在预防目标的关键时期。他们随访了 38 名高危人群,其中 8 名发展为类风湿性关节炎(转化者)。这些转化者的补体成分水平显著降低,表明在向类风湿性关节炎转变的过程中,免疫复合物的形成导致补体耗竭。此外,代谢相关蛋白(如 PSMB7)上调,表明免疫蛋白酶体活化(图 2d-e)。他们采集了其中 3 名转化者的血浆样本,比较其发病前后的蛋白质组学差异(图 2f)。转化者和非转化者之间以及 RA 发病前后常见的蛋白质包括 APOE、HIST2H3A 和 TF。这些发现强调了脂质代谢失调、中性粒细胞胞外诱捕网形成和铁稳态在 RA 发展中的作用。
IgG 在类风湿性关节炎 (RA) 的发病机制中发挥双重作用。他们鉴定出特定 IgG 片段,这些片段在疾病组与健康对照组相比水平存在差异。具体而言,IGKV3D-20、IGKV4-1 和 IGHV4-61 在 ACPA 阳性 RA 或高危人群中升高,而 IGHV3-15、IGKV3D-15 和 IGKC 降低。此外,所有差异 IgG 片段在 ACPA 阴性 RA 患者中均最低(图 2g)。
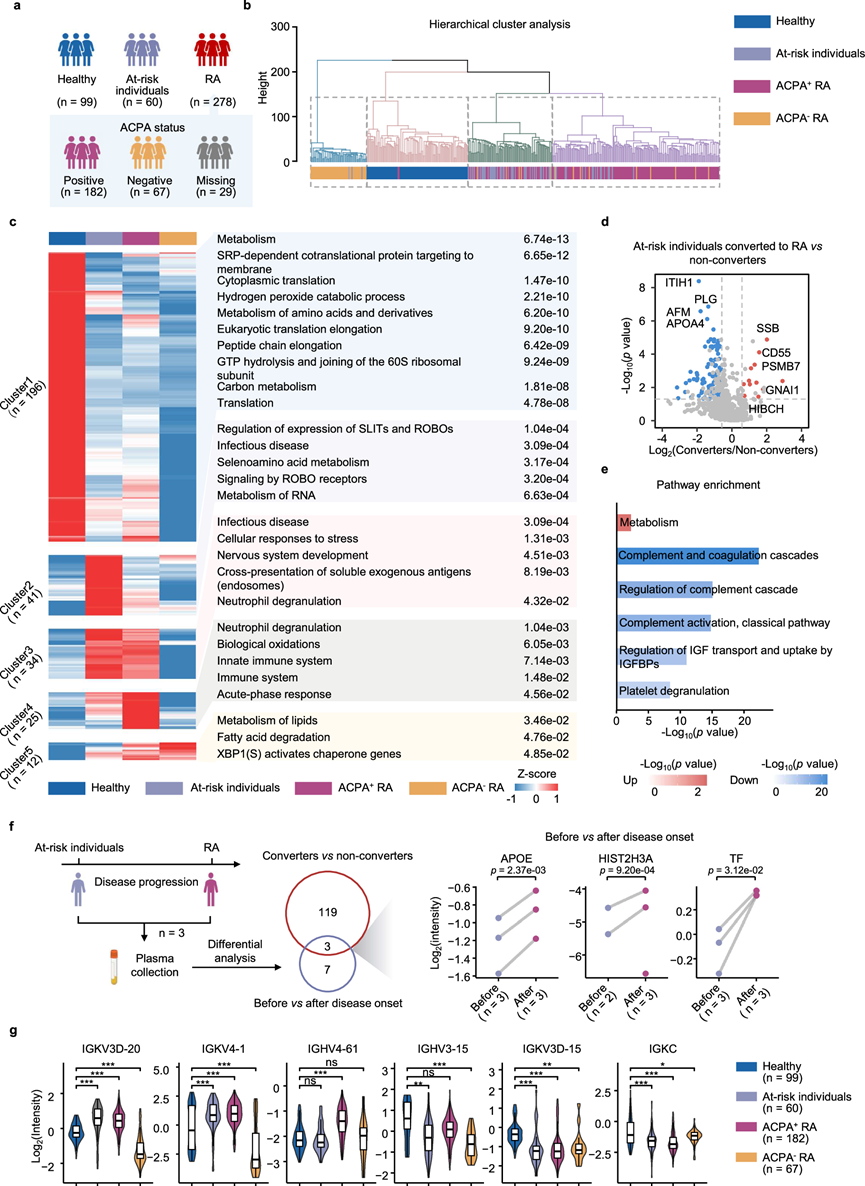
图2. RA 发展过程中的血浆蛋白质组异质性。
(a) 不同临床亚组中的个体数量。(b) 树状图显示了跨样本蛋白质组数据的层次聚类。(c) 热图显示了健康个体、高危个体、ACPA 阳性 RA 患者和 ACPA 阴性 RA 患者中蛋白质的无监督 k 均值聚类。(d) 差异表达蛋白 (DEP)火山图。(e)通路富集分析。(f) 从三名高危个体在 RA 发病前后采集的样本的蛋白质组学分析设计示意图(左),维恩图(中间)显示两次比较中重叠的 DEP,散点图(右)显示 RA 发病前后重叠 DEP 的强度。(g) 小提琴图显示四个临床组中抗体片段的强度。
03
鉴定与疾病活性相关的蛋白质
接下来,他们研究了与疾病活性相关的蛋白质。他们观察到在 ACPA 阳性 RA 患者中 DAS28-CRP 评分存在明显的性别差异,男性的疾病活性高于女性。相反,ACPA 阴性 RA 没有表现出这种性别相关的差异(图 3a-b)。由于疾病活性随年龄增长而增加,特别是在 ACPA 阳性女性中(图 3c-d),因此仅对女性 ACPA 阳性 RA 患者进行了差异表达滑动窗口分析(DE-SWAN)。该分析显示,女性在 45 岁以后年龄相关蛋白质的数量迅速减少(图 3e)。在本研究中,这种年龄分类进一步揭示了 DAS28-CRP 的差异,其中 45 岁以下的女性与 45 岁以上的女性相比疾病活性降低(图 3f)。临床指标方面,压痛关节数(TJC)与CRP水平呈现相似趋势,均在45岁以上女性中升高(图 3f)。
为了减少性别和年龄对与疾病活性相关的蛋白质计算的影响,他们在后续分析中校正了年龄和性别。通过多元线性建模,他们初步鉴定了与DAS28-CRP相关的蛋白质,其中较多的蛋白质与DAS28-CRP呈负相关(图3g)。与DAS28-CRP呈正相关的蛋白质,如CRP、LRG1、ORM1、SERPINA4和C9,主要与急性期反应和免疫系统相关。相反,与DAS28-CRP呈负相关的蛋白质主要参与生物合成和代谢(图 3h)。他们进一步基于具体的DAS28-CRP参数进行了相关性分析(图 3i)。在与临床参数最显著相关的蛋白质中,SERPINA3、LRG1 和 HP 与 CRP 呈正相关,而 ACOX1 和 LRG1 与肿胀关节数 (SJC) 呈正相关。此外,HSD17B10 和 RPL23A 分别与视觉模拟量表 (VAS) 和 TJC 呈负相关(图 3i)。ACPA 阴性RA患者的增强免疫反应与 DAS28-CRP 呈一致的正相关。出乎意料的是,几乎没有蛋白质与 DAS28-CRP 或其四个参数呈负相关。
由于 45 岁以下和 45 岁以上 ACPA 阳性女性的 DAS28-CRP 评分存在差异,他们研究了年龄对该组疾病活性的影响。对与年龄和 DAS28-CRP 相关的蛋白质进行了重叠分析(图 3j)。他们发现 CRP、SERPINA3、SAA2 和 HP 水平随年龄增长而升高,并与疾病活性呈正相关。相反,A2M、AHSG 和 TF 随年龄增长而降低,与疾病活性呈负相关,突出了衰老对疾病进展的特定影响。此外,APOC3、RBP4、FN1 和 NCL 随年龄增长而升高,但与疾病活性呈负相关。这些保护性蛋白质与年龄相关的增加值得进一步研究,以了解其中的潜在机制。
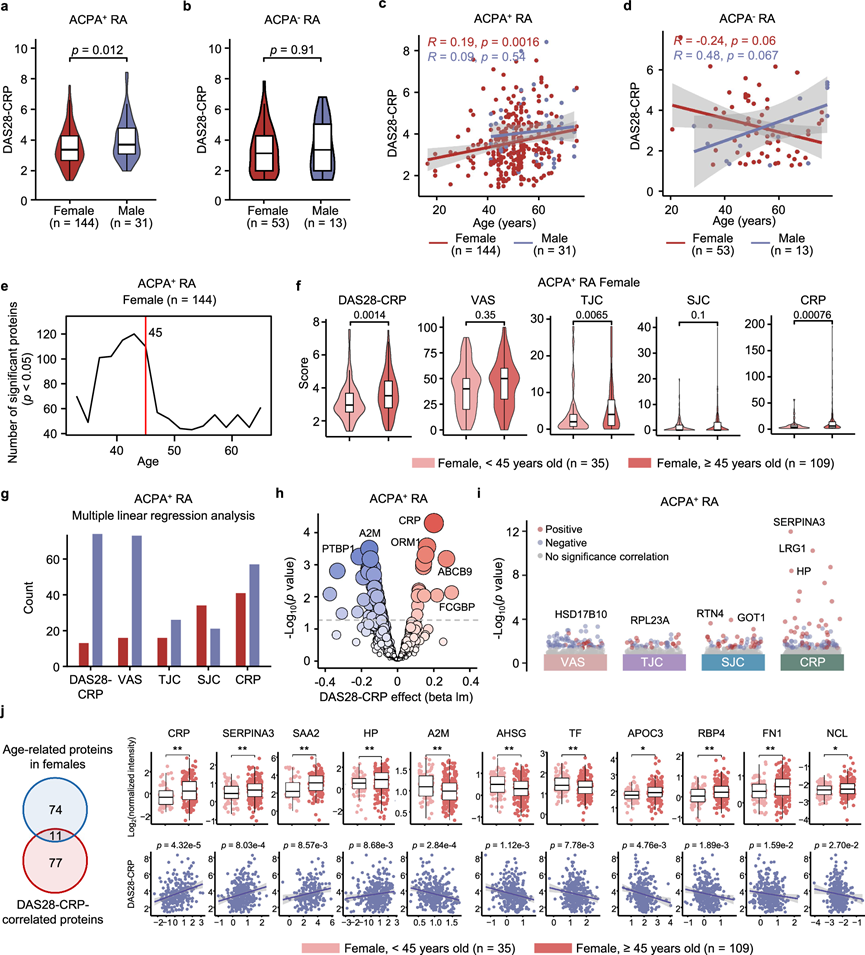
图3. 性别和年龄对疾病活性和蛋白质组的影响。
(a-b) ACPA 阳性或 ACPA 阴性RA 患者按性别分组的 DAS28-CRP 评分小提琴图。(c-d) 带有拟合回归线的散点图,说明ACPA 阳性或 ACPA 阴性 RA中按性别分组的年龄和 DAS28-CRP 之间的Spearman 相关性。(e) ACPA 阳性女性中不同年龄段蛋白质的DE-SWAN 分析。(f) 小提琴图显示 45 岁以上和以下 ACPA 阳性女性中 DAS28-CRP 和 4 项临床指标( VAS、SJC、TJC 和 CRP)的年龄特异性差异。(g-i) ACPA 阳性 RA 患者 ( n = 175) 的 DAS28-CRP 指标与蛋白质之间的多元线性回归分析。(j) 维恩图显示在 45 岁以下和 45 岁以上 ACPA 阳性女性之间表现出显著变化或与 DAS28-CRP 显著相关的蛋白质的重叠(左)。箱线图(右上)显示 45 岁以下和 45 岁以上 ACPA 阳性女性之间重叠蛋白质的标准化强度。散点图(右下方)显示蛋白质与 DAS28-CRP 之间的回归分析。
04
分析 DAS28-CRP 的非线性蛋白质组学波动
血浆蛋白与DAS28-CRP之间的关系错综复杂,超越了线性关联。为了解读DAS28-CRP(评估疾病活性最重要的参数)随蛋白质组动力学波动的复杂性,人们采用了两种策略。首先,为了研究基于临床分类的蛋白质组学差异,他们根据 DAS28-CRP 将 ACPA 阳性 RA 患者分为四组:(I)缓解(<2.6),(II)低度(2.6-3.2),(III)中度(3.2-5.1)和(IV)高(>5.1)。为了降低蛋白质组固有的复杂性,他们使用无监督的层次聚类将具有相似轨迹的蛋白质分组,从而产生六个不同的聚类(图 4a)。在聚类3 中,随着疾病活性的增加,与急性期反应、先天免疫和中性粒细胞活性相关的蛋白质呈上升趋势。在聚类6 中,参与碳代谢、IGF 转运和糖酵解的蛋白质随着 DAS28-CRP 的增加而持续减少。聚类5 和 聚类2 中的蛋白质参与丙酮酸代谢、ROBO 信号传导和翻译相关过程,值得注意的是,聚类1和聚类4中补体的波动表明,随着疾病活性水平的变化,补体成分的激活和消耗之间存在动态平衡。对ACPA阴性RA患者进行的类似分析揭示了与ACPA阳性RA患者的差异。ACPA阴性RA患者通常表现出先天免疫活性增强(随疾病活性增加而降低)、适应性免疫反应(例如抗原呈递和T细胞受体信号传导)减弱,以及氨基酸代谢和轴突导向显著增强。总体而言,这些结果表明,某些血浆蛋白随DAS28-CRP水平升高的变化呈非线性。
其次,鉴于大多数蛋白质在 DAS28-CRP 中的非线性趋势,如局部估计的散点图平滑 (LOESS) 估计的轨迹所示(图 4b),他们使用 DE-SWAN 分析来捕捉较小尺度40的局部波动。他们分析了 40 个样本窗口内的蛋白质水平,比较了 20 个样本片段内的两组,并将窗口从低到高疾病活性逐步滑动 0.1 DAS28-CRP 值。该分析确定了 DAS28-CRP 评分分别为 3.1、3.8 和 5.0 的三个关键峰,揭示了与这些 DAS28-CRP 值相对应的蛋白质水平变化波(图 4c-d)。这些峰与不同的蛋白质组有关。在 DAS28-CRP 评分为 3.1 时,观察到上调的先天免疫功能,例如补体激活和中性粒细胞脱颗粒,同时观察到前向转运受到抑制。 DAS28-CRP评分为3.8时,炎症通路进一步上调,葡萄糖代谢受损。DAS28-CRP评分为5.0时,表明氧化应激升高,ROBO信号和蛋白质代谢降低(图 4e)。DAS28-CRP相关蛋白的这些动态和非线性变化表明,应针对不同疾病活性水平的特定蛋白制定治疗策略。此外,他们评估了DAS28-CRP的四个组分与三个峰上鉴定的蛋白质之间的相关性。与VAS相关的蛋白质在DAS28-CRP 3.8和5.0时与DEP显著重叠,而与其他参数相关的蛋白质在DAS28-CRP 5.0时与DEP重叠较大(图 4f)。这些发现表明DAS28-CRP相关蛋白质组与不同的疾病活性参数表现出不同的关联。
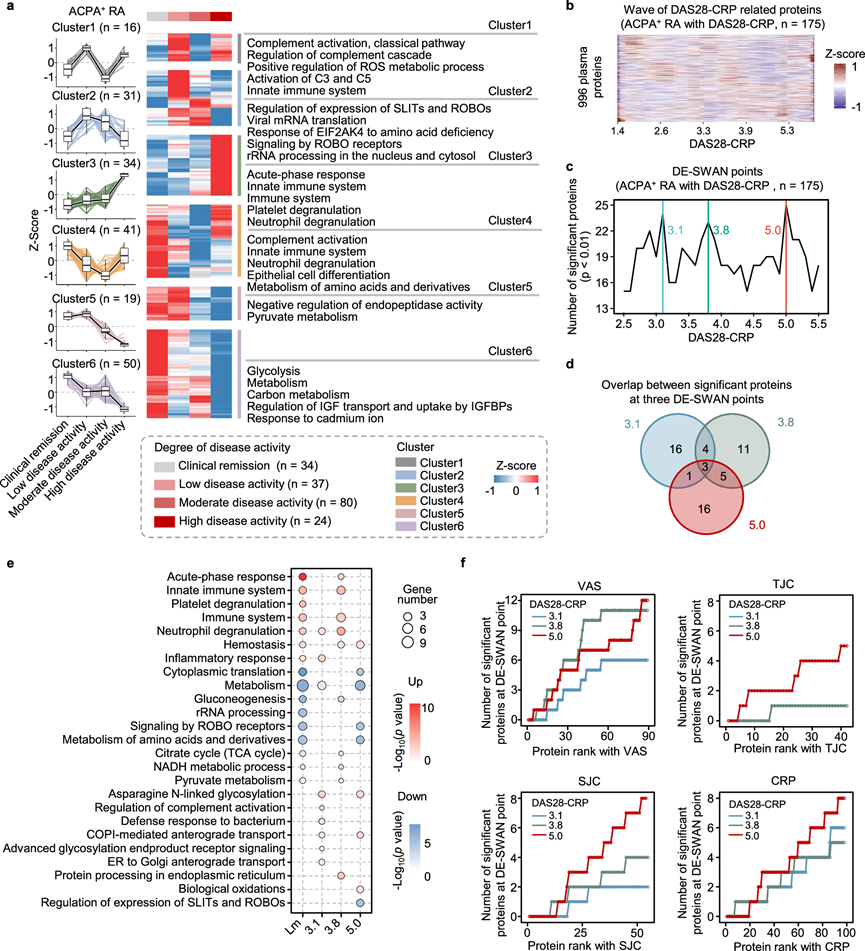
图4. 深入探索疾病活性相关的蛋白质动态。
(a) 对四种疾病活性组中的 DEP进行无监督k均值聚类分析。(b) 热图可视化跨 DAS28-CRP 的蛋白质轨迹。(c) 不同疾病活性水平的 DEP 数量。(d) 在三个局部峰处具有显著差异表达的蛋白质重叠。(e) 气泡图可视化了通过 DAS28-CRP 线性回归和 DE-SWAN 中三个峰处鉴定出的显著蛋白质的富集通路。(f) 线图可视化了蛋白质与 VAS、TJC、SJC 和 CRP 的线性回归分析结果。
05
通过机器学习预测治疗反应的蛋白质组学特征
以 MTX 为基础的 csDMARD 疗法是一线治疗,但对各种组合的反应率并不一致。对纵向队列对 csDMARD 的治疗反应进行深入分析至关重要,但仍有待探索。为了解决这个问题,他们使用了 206 例用各种 csDMARD 治疗的患者的随访数据。随后,按照欧洲抗风湿病联盟 (EULAR) 标准,在三个多月后进行了评估。他们重点关注 MTX + 来氟米特 (LEF) (n = 89) 和 MTX + 羟氯喹 (HCQ)组,因为这些组的样本量足以进行统计分析。临床缓解和疾病活性较低的 RA 患者排除在外,因为中度至高度疾病活性的患者更有可能对治疗有反应。两组中应答者和无应答者的年龄和性别差异均不显著。最初,他们在不考虑性别和年龄影响的情况下对应答者和无应答者进行了差异分析。在对 MTX + LEF 治疗有应答的患者中,与免疫和能量代谢相关的蛋白质增加,而与脂质氧化相关的蛋白质减少(图 5a-c)。在对 MTX + HCQ 治疗有应答的患者中,他们检测到与代谢、免疫和 Toll 样受体级联相关的蛋白质水平升高,与运输途径相关的蛋白质水平降低(图 5d-f)。此外,他们分析了 ACPA 阳性 RA 组中应答者和无应答者之间的这些差异,该组具有足够的样本量进行统计分析。 MTX + LEF 应答者显示补体活化、纤溶和自噬增加,代谢和糖酵解途径下调,而 MTX + HCQ 应答者表现出免疫活化上调和线粒体运输途径下调。鉴于性别可能会影响治疗反应,他们还研究了其对反应相关蛋白质组学的影响。在 MTX + LEF 的女性应答者中,他们观察到蛋白质转运和炎症途径升高,而男性应答者则显示内吞作用增加。在 MTX + HCQ 应答者中,女性表现出无义介导的衰变增加和氨基酸代谢降低。
此外,他们开发了利用血浆蛋白预测治疗反应的模型。通过对特征蛋白进行最小绝对收缩和选择算子 (LASSO) 特征选择,他们构建了线性回归模型并计算了这些蛋白质对模型的贡献得分。最终选择绝对贡献值大于 1 的蛋白质用于建模(图 5g-h)。他们确保训练集和测试集中有反应者和有反应者的数量相等。经过 10 倍交叉验证以确定最佳正则化参数后,他们进行了 100 次迭代以生成平均受试者工作特征 (ROC) 曲线,确保预测稳定可靠。在预测 MTX + LEF 治疗反应的模型中使用了五种蛋白质,其中 LGALS3BP 和 MYH9 在有反应者中增加,而 ECI2、COL1A1 和 CBR1 在有反应者中减少。对于 MTX + HCQ 治疗,RPL27A 为正向预测因子,GGT1 为负向预测因子。LASSO 选择的蛋白质预测因子在多种其他特征选择方法(随机森林、递归特征消除结合支持向量机、XGBoost、稳定性选择和弹性网络)中均排名前 10,证明了它们的稳健性。交叉验证得出 MTX + LEF 治疗组中训练集的平均 ROC 为 0.96,测试集的平均 ROC 为 0.88(图 5i)。MTX + HCQ 治疗组中训练集的预测 ROC 值为 0.92,测试集的预测 ROC 值为 0.82(图 5j)。进行了 SHAP 分析以解释单个蛋白质对预测模型的贡献,证实了它们的作用方向与通过特征选择确定的方向一致。此外,他们利用 LASSO 识别的特征,结合随机森林和 XGBoost 构建了预测模型,但其 ROC 中值仍然低于 LASSO。这些发现一致凸显了 LASSO 卓越的预测性能。此外,将 DAS28-CRP 参数(VAS、SJC、TJC 和 CRP)纳入蛋白质特征后,预测性能略有提升,在测试集中,MTX + LEF 的ROC 中值为 0.90( vs 0.88),MTX + HCQ 的 ROC 中值为 0.84。
他们在一个独立的队列中验证了本研究的模型性能,该队列由 46 名接受 MTX + HCQ 治疗的 RA 患者和 19 名接受 MTX + LEF 治疗的 RA 患者组成。酶联免疫吸附试验 (ELISA) 结果显示,应答者和无应答者之间的生物标志物变化与蛋白质组学数据一致。将这些蛋白质水平整合到本研究的模型中保持了强大的分类效率,MTX + LEF 的 ROC 值为 0.90,MTX + HCQ 的 ROC 值为 0.86。使用混淆矩阵确定最佳截止值,MTX + LEF 模型成功识别出 11 名应答者中的 9 名,且没有假阴性。相比之下,MTX + HCQ 模型表现出 0.63 的灵敏度和 1.0 的特异性,这可能受到较小发现队列规模的影响(图 5k)。总体而言,两种 LASSO 模型都表现出了强大的预测性能,可以准确预测两种最常见的 MTX 联合疗法的治疗反应,为个性化治疗策略提供了宝贵的见解。
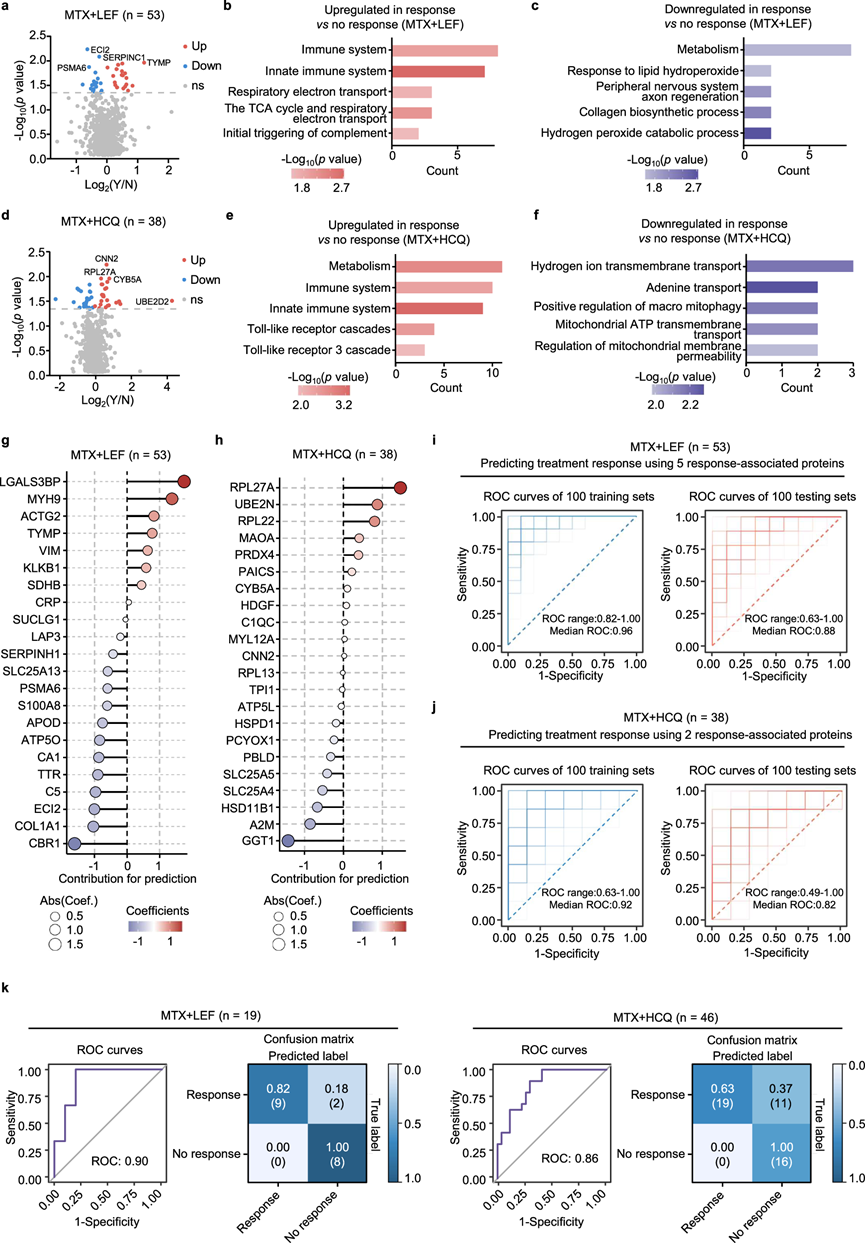
图5. 机器学习驱动的关键蛋白质发现,用于预测对 csDMARD治疗的反应。
(a)MTX + LEF 治疗有反应和无反应之间的 DEP 火山图。(b-c) 蛋白质的富集分析。(d) MTX + HCQ 治疗有反应和无反应之间的DEP火山图。(e-f) 对 MTX + HCQ 治疗有反应和无反应的上调和下调蛋白质的富集分析。(g-h) LASSO 回归分析显示 DEP对 MTX + LEF和 MTX + HCQ组 治疗反应预测的贡献。(i-j) ROC 曲线显示了 LASSO 模型对 MTX + LEF 和 MTX + HCQ 疗效的预测性能。(k) ROC曲线显示了整合 ELISA 测量的蛋白质水平后的模型性能。
06
类风湿性关节炎患者治疗后蛋白质组学变化
为了研究对MTX + LEF或MTX + HCQ治疗有响应的RA患者在治疗后的蛋白质组学变化,他们进行了差异分析(图 6a-b)。他们发现,在MTX + LEF治疗后,响应患者的视黄醇代谢和细胞质翻译增加,而肌动蛋白细胞骨架和急性期反应降低(图 6a-c)。相反,在MTX + HCQ治疗后,响应患者的mRNA代谢、视黄醇代谢和细胞粘附增加,而补体途径降低(图 6b-d)。值得注意的是,在无响应患者中,无论是哪种治疗,这些途径都没有显示出明显的变化。为了确定影响药理疗效的关键因素,他们对与治疗反应相关的蛋白质和csDMARDs治疗后发生显著变化的蛋白质进行了重叠分析。在MTX + LEF组中,鉴定出8种参与急性反应、肌动蛋白细胞骨架组织、线粒体生物合成激活和代谢的常见蛋白质(图 6g)。在MTX + HCQ组中,鉴定出6种重叠蛋白质(图 6h)。这些蛋白质可能成为这两种csDMARD疗法的潜在靶点。此外,他们还探讨了性别和 ACPA 状态对治疗引起的蛋白质组学变化的影响。由于接受两种治疗的 ACPA 阴性 RA 患者数量有限,接受 MTX + HCQ 治疗的男性患者数量也有限,因此这些患者未纳入分析。在接受 MTX + LEF 的 ACPA 阳性 RA 患者中,翻译、氨基酸代谢和轴突导向均增加。MTX + LEF 治疗后,女性反应者蛋白质和 RNA 代谢升高,而男性反应者肌动蛋白细胞骨架调控增加。相反,MTX + HCQ 治疗后,ACPA 阳性反应者的 RNA 代谢和轴突导向增加。
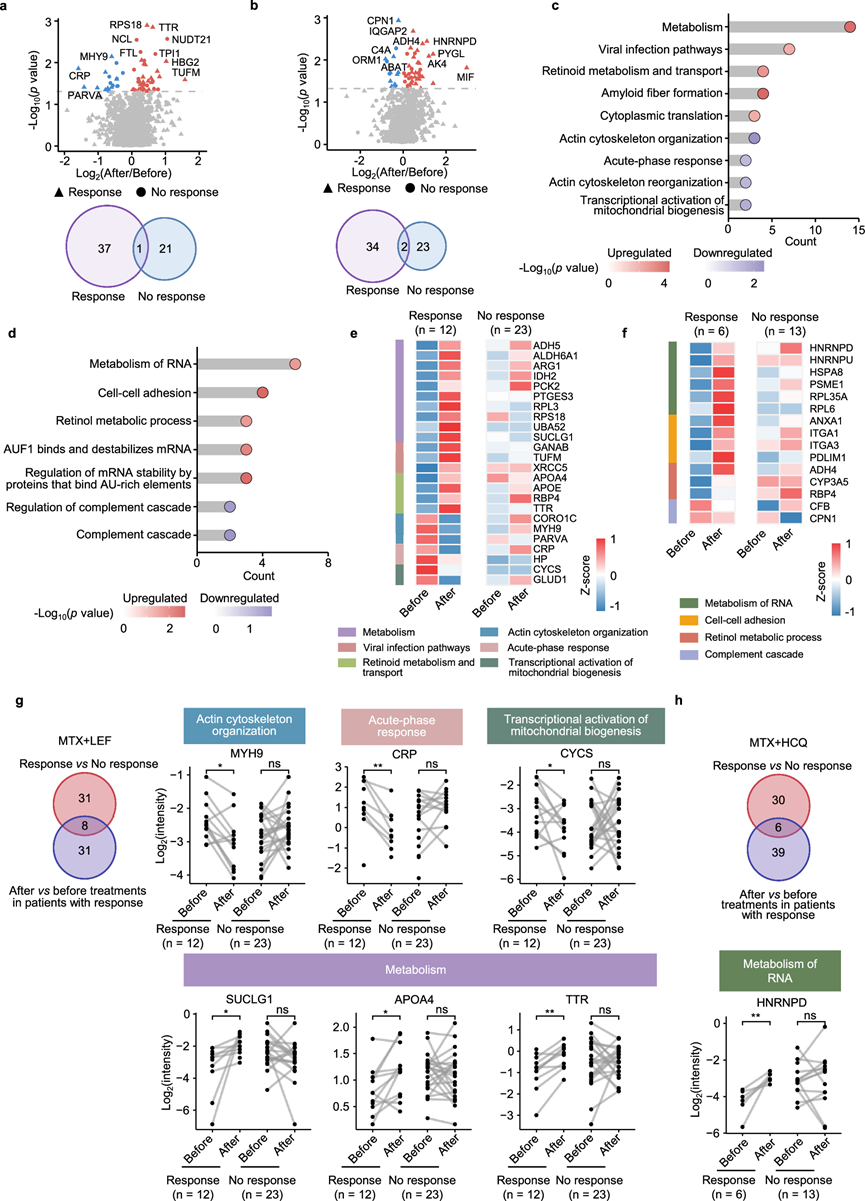
图6. 接受 csDMARD治疗且反应不同的 RA 患者的血浆蛋白特征。
(a) 火山图显示 MTX + LEF 治疗前后的 DEP。(b) 火山图显示 MTX + HCQ 治疗前后的 DEP。(c) MTX + LEF 治疗前后 DEP 的通路富集分析。(d) MTX + HCQ 治疗前后 DEP 的通路富集分析。(e) MTX + LEF 治疗前后 DEP 相对丰度的热图,按反应分开。(f) MTX + HCQ 治疗前后 DEP 相对丰度的热图。(g-h) 维恩图显示 MTX + LEF和 MTX + HCQ疗法的治疗相关蛋白和反应相关蛋白的重叠。
+ + + + + + + + + + +
结 论
本研究对 278 例 RA 患者、60 例高危人群和 99 例健康对照者的纵向队列进行了血浆蛋白质组学分析,观察到高危人群和 RA 患者具有不同的蛋白质组学特征,且蛋白质水平的变化与疾病活动度相关,尤其是在 DAS28-CRP 阈值分别为 3.1、3.8 和 5.0 时。MTX和LEF的联合用药可调节促炎通路,而 MTX 联合HCQ则影响能量代谢。本研究建立了一个机器学习模型来预测治疗反应,该模型在测试集中分别获得了 0.88 (MTX + LEF) 和 0.82 (MTX + HCQ) 的平均受试者工作特征 (ROC) 曲线下面积。利用酶联免疫吸附试验数据,在独立队列中进一步验证了这些模型的有效性。总体而言,本研究揭示了类风湿关节炎不同阶段和亚型中独特的血浆蛋白质组特征,为预测疾病发作和治疗反应提供了有价值的生物标志物。
+ + + + +



 English
English


