文献解读|Cell Rep Med(10.6):空间多组学揭示混合型小细胞肺癌的单克隆起源、神经内分泌可塑性和微环境特征
✦ +
+
论文ID
原名:Spatial multi-omics unveils the monoclonal origin, neuroendocrine plasticity, and microenvironment niches in combined small-cell lung cancer
译名:空间多组学揭示混合型小细胞肺癌的单克隆起源、神经内分泌可塑性和微环境特征
期刊:Cell Reports Medicine
影响因子:10.6
发表时间:2026.04.21
DOI号:10.1016/j.xcrm.2026.102741
背 景
混合型小细胞肺癌(cSCLC)是一种罕见且病理机制尚不明确的小细胞肺癌(SCLC)亚型,约占所有SCLC病例的2%-5%。cSCLC的病理特征是SCLC与任何亚型的非小细胞肺癌(NSCLC)成分混合,包括肺腺癌(LUAD)、肺鳞状细胞癌(LUSC)或大细胞神经内分泌癌(LCNEC)。cSCLC的诊断主要依据手术切除肿瘤标本的病理学评估。由于小活检可能无法全面反映肿瘤的组织学多样性,因此在晚期不可切除的患者中,cSCLC常常漏诊。cSCLC具有异质性,且预后比原发性SCLC更差,但由于对cSCLC的生物学、谱系可塑性和肿瘤微环境(TME)的分子机制了解有限。
实验设计
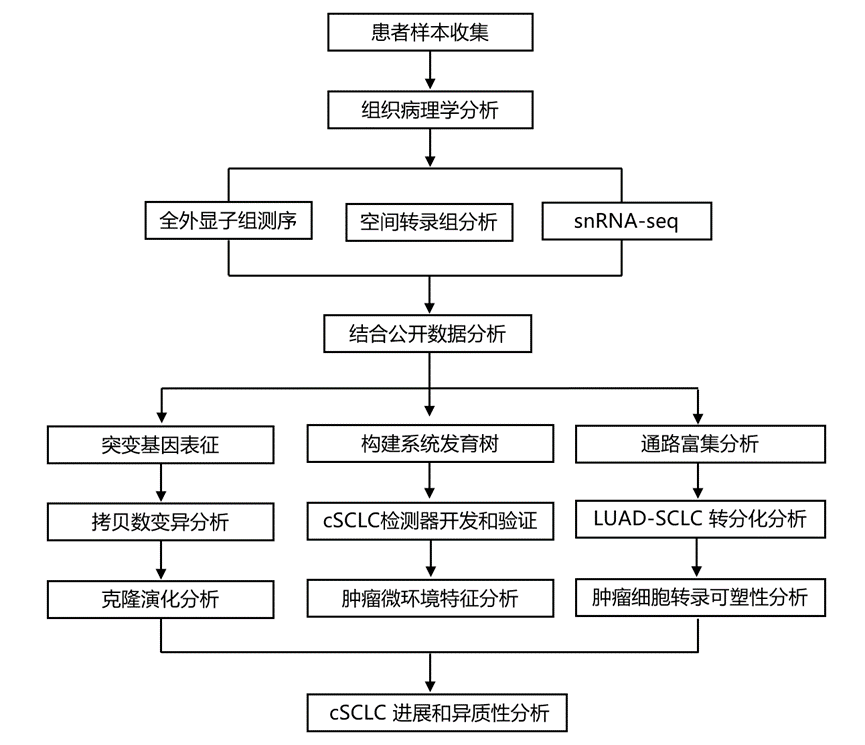
结 果
01
cSCLC患者队列和研究设计
本研究共纳入19例cSCLC患者,包括10例SCLC/LUAD(患者[P] 1–P10)、3例小细胞肺癌/肺鳞癌(SCLC/LUSC)(P11-P13)和6例小细胞肺癌/大细胞神经内分泌癌(SCLC/LCNEC)(P14–P19)(图1A)。除P17外,所有肿瘤样本中SCLC和NSCLC或LCNEC成分区域均通过病理检查清晰界定(图1B)。P17的SCLC和LCNEC成分紧密混合,边界不清。在福尔马林固定石蜡包埋(FFPE)的cSCLC样本中,通过显微切割收集多个SCLC和NSCLC(或LCNEC)成分区域,进行多区域全外显子组测序(WES)。共对来自16例患者的95个SCLC、NSCLC和LCNEC区域进行了WES(图1C)。分别对12例和 6 例患者进行了单细胞核转录组分析(snRNA-seq)和空间转录组学 (ST) 分析,涵盖了所有三种组织学亚型。采用多区域全外显子组测序(WES)技术,对同一例cSCLC肿瘤的FFPE切片及其配对的邻近正常组织中SCLC和NSCLC成分的突变谱进行空间表征。共对95个肿瘤区域和16个配对的邻近正常组织进行了高深度测序。
在所有患者中,TP53和RB1是最常见的突变基因(图 2A)。除 P3 外,所有患者的 SCLC 和 NSCLC(或 LCNEC)区域均存在TP53体细胞突变(表 S5),表明这些突变是 cSCLC 的克隆性突变。RB1突变在 6 例患者中鉴定为克隆性突变,在 P2 和 P9 中鉴定为亚克隆性突变。在 P2 中,RB1在 5 个区域(4 个 SCLC 和 1 个 LUAD)中为突变型,但在 1 个 LUAD 区域中为野生型(图 2A)。在 40% (4/10) 的 cSCLC/LUAD 亚型患者中检测到EGFR突变。在这 4 例患者中, P6、P8 和 P9 的所有 SCLC 和 LUAD 区域均检测到EGFR突变,表明这些突变是 cSCLC 的克隆性突变。在P7组中,4个SCLC区域中有3个存在EGFR突变,2个肺腺癌(LUAD)区域中全部存在EGFR突变。在SCLC/LUAD亚型中检测到的EGFR突变类型与纯LUAD患者中报道的突变类型相似,包括19号外显子缺失(P6和P9)、L858R(P7)以及E709V+G719C(P8)(图2B)。重要的是,在SCLC和LUAD成分中均存在的EGFR突变频率为40%,与两个独立的亚洲SCLC/LUAD队列的报道一致(图2B)。该频率接近纯LUAD亚洲男性患者的报道频率(44%),但显著高于纯原发性SCLC患者的报道频率(约3%),这表明cSCLC中SCLC成分具有独特的遗传特征,并支持SCLC/LUAD亚型中神经内分泌转化(NE转化)。
对于全基因组拷贝数变异(CNA),来自同一患者的不同组织学亚型表现出高度一致的CNA模式,提示它们可能来源于相同的祖细胞(图2C)。在cSCLC中,最常见的扩增染色体臂是1q、5p和6p,而常见的缺失染色体臂是3p、4q、5q、10q和15q(图2C)。常见的CNA特征在SCLC和NSCLC成分中保持一致,并且与纯SCLC不同,后者通常在3q和5q处扩增,并在13q(包含RB1基因)和17p(包含TP53基因)处缺失。值得注意的是,3p缺失已确定为SCLC/LUAD亚型发生神经NE转化的危险因素。在10例SCLC/LUAD样本中有6例存在3p缺失,在2例SCLC/LUSC样本中有1例存在3p缺失,在所有4例SCLC/LCNEC样本中均存在3p缺失。SCLC区域的CNA负荷显著高于LUAD或LUSC区域(图2D)。然而,在SCLC/LCNEC样本中,SCLC和LCNEC区域的CNA负荷无显著差异(图2D),这可能是由于NE组织学特征相关的增殖能力更强、基因组不稳定性更高所致。
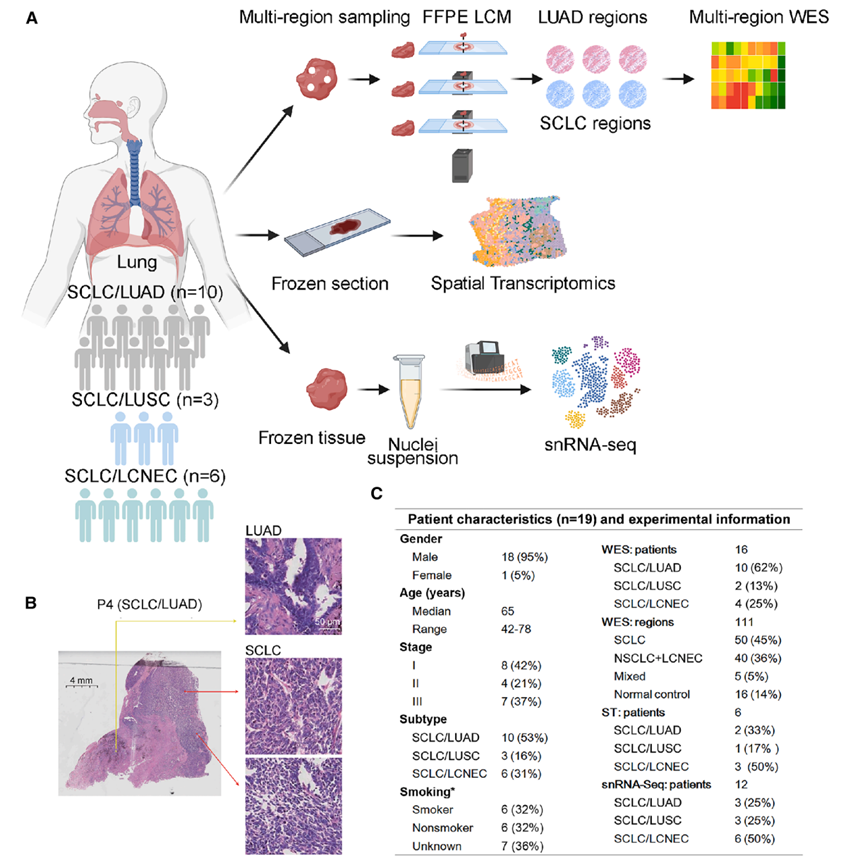
图1. 研究设计、方法和患者队列概述。
(A) cSCLC 表征工作流程,包括多区域 WES、ST 和 snRNA-seq。(B) 代表性的 H&E 染色显示 P4 中 SCLC 和 LUAD 成分共存。(C) 19 例 cSCLC 患者的人口统计学特征、临床特征和多组学数据。
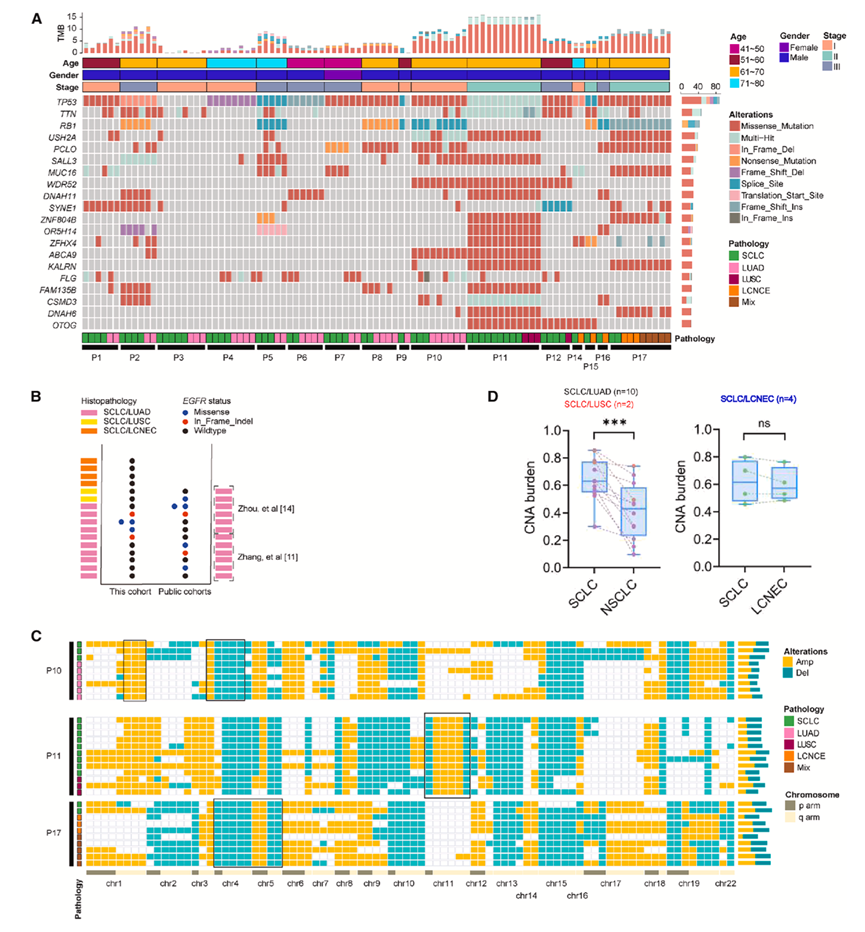
图2. 通过多区域全外显子组测序分析的cSCLC突变图谱和拷贝数变异。
(A) 体细胞突变图显示了cSCLC患者不同区域中突变频率最高的20%基因。(B) cSCLC样本中EGFR突变的患病率。(C) 热图显示了来自 P10、P11 和 P17 的多个肿瘤区域中染色体臂水平的CNA。(D) 各组分间平均CNA负荷的比较。
02
基因组进化揭示了小细胞肺癌的单克隆起源
他们研究了来自同一cSCLC肿瘤的多个SCLC和NSCLC(或LCNEC)区域的突变谱,发现不同组织学感兴趣区域(ROI)之间的体细胞突变具有高度一致性,即使是从不同组织块中分离出来的ROI也是如此。例如,从P11中收集了三个肿瘤组织块(B1-B3),并对12个ROI进行了WES(B1:2个SCLC,1个LUSC;B2:3个SCLC,1个LUSC;B3:4个SCLC,1个LUSC)。维恩图显示,同一组织块内不同组织学亚型的ROI之间以及不同组织块之间的体细胞突变存在大量重叠(图3A),提示这些不同组织学亚型可能具有单克隆起源。在P8的不同组织块中,SCLC和LUAD区域也发现了类似的体细胞突变一致性。
为了阐明cSCLC的克隆演化,他们利用在每个样本的不同组织学ROI中鉴定的非同义突变构建了系统进化树。每个样本内的多个组织学ROI共有致癌突变,例如TP53、RB1、EGFR和PTEN,这表明这些突变发生在组织学分化之前(图3B)。在对 SCLC/LUSC 病例 P11 进行密集采样后,在 SCLC 和 LUSC 成分中均检测到了TP53和染色质调节因子KDM6A 和FAT4的突变改变,而早期驱动事件,如NRAS和ARID1A (肺癌中的关键表观遗传肿瘤抑制基因),在各个区域中几乎普遍分布(NRAS存在于所有 SCLC ROI 和 3 个 LUSC ROI 中的 2 个;ARID1A存在于所有 LUSC ROI 和 9 个 SCLC ROI 中的 8 个),少数突变阴性 ROI 可能反映了较低的肿瘤细胞密度和变异等位基因频率低于与肿瘤内容空间异质性相关的检测阈值。相比之下,AFF1、PTEN、BCL9和CAMTA1的突变仅限于SCLC ROI,而LCK和WT1 的突变则仅限于LUSC ROI,这表明谱系特异性的私有分支是在从共同祖先分化后出现的。在整个队列中观察到了类似的共享主干驱动基因改变以及谱系限制性私有突变模式(图3B)。值得注意的是,TP53几乎在所有样本的系统发育树中都始终位于根部,这与先前关于 cSCLC 不同组分中TP53改变几乎普遍存在的报道一致。
总之,这些数据支持一个分支进化模型,在该模型中,形态不同的 SCLC 和NSCLC(或LCNEC)组分起源于同一个祖先克隆,该克隆随着时间的推移分化成不同的形态和谱系状态。值得注意的是,在四例SCLC/LUAD患者(P6-P9)中,他们在小细胞肺癌和肺腺癌区域均检测到了EGFR突变——这种突变在肺腺癌中常见,但在原发性小细胞肺癌中极为罕见(图2B)。这一发现提示小细胞肺癌和肺腺癌细胞可能起源于共同的EGFR基因-突变祖细胞,进一步支持混合型小细胞肺癌/肺腺癌组织学的小细胞肺癌中肺腺癌向小细胞肺癌NE转化。
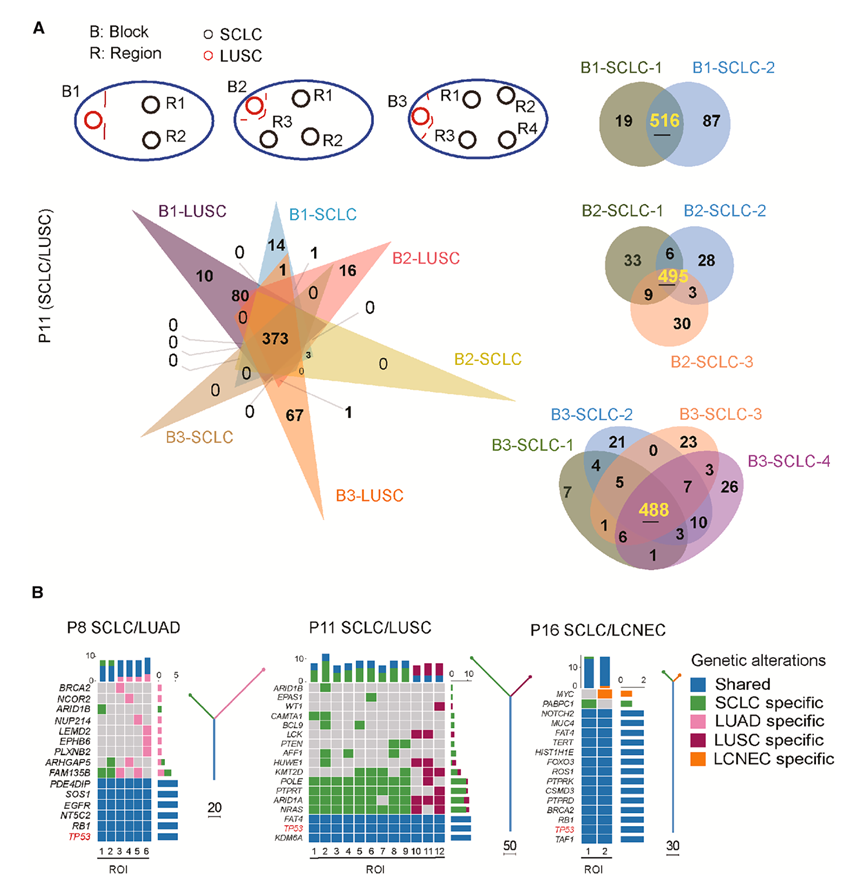
图3. 通过多区域全外显子组测序对cSCLC进行克隆演化和系统发育分析。
(A) P11中不同空间区域突变的一致性。(左上)通过激光捕获显微切割取样的组织块(B1-B3)和空间区域(R)示意图。(左下)维恩图显示了不同组织块和组织学成分中体细胞突变的重叠情况,重点突出了373个共有突变的核心集合。(右)维恩图展示了特定组织块(B1、B2和B3)中不同小细胞肺癌(SCLC)区域体细胞突变的一致性。(B) P8(小细胞肺癌/肺腺癌)、P11(小细胞肺癌/肺鳞癌)和 P16(小细胞肺癌/大细胞神经内分泌癌)的系统发育树和突变热图。
03
基于突变的、灵敏度更高的cSCLC诊断测试方法
cSCLC 的诊断主要基于手术切除肿瘤标本的病理学评估。在大多数 cSCLC 肿瘤中,SCLC 和NSCLC(或LCNEC)成分在空间上是分离的,且 SCLC 区域通常明显更大。由于活检取样量有限,存在 NSCLC 成分可能未检出的风险,从而导致依赖活检诊断的不可切除患者中,容易将cSCLC误诊为原发性SCLC。他们开发了一种基于突变的诊断测试(cSCLC Detector),用于通过组织活检或液体活检从 SCLC 患者中检测 cSCLC。cSCLC Detector 是一个包含 4 个基因的单核苷酸变异 (SNV) 检测组(EGFR、KRAS、BRAF和PIK3CA)。据报道,所有基因改变均对LUAD和LUSC具有高度特异性(图 4A)。为了评估 cSCLC Detector 的性能,他们收集了共 38 例经组织病理学确诊的 cSCLC 样本(SCLC/LUAD 和 SCLC/LUSC),其中 12 例来自本研究,26 例来自既往研究。cSCLC Detector在本队列( n = 38)中显示出 61% 的敏感性,尤其是在 SCLC/LUAD和 SCLC/LUSC患者中,敏感性分别为 74% 和 27% (图4B)。SCLC /LUSC 亚型的敏感性相对较低,主要归因于 LUSC 中缺乏高度特异性和复发性驱动突变。随后,他们使用来自两个先前研究过的SCLC队列的组织测序数据测试了 cSCLC Detector ,结果显示 14.1% 的样本cSCLC-Detector 检测结果呈阳性(图 4C-D)。此外,他们还使用来自另一个先前研究过的初诊小细胞肺癌患者队列(n = 254)的血液循环肿瘤 DNA(ctDNA)数据测试了cSCLC Detector,结果显示 14.2% 的样本(36/254)cSCLC-Detector 检测结果呈阳性,与组织基因组测序的结果相似(图 4C-D)。相比之下,既往研究报道所有小细胞肺癌患者中 cSCLC 病例占比为 2%–5%,cSCLC 检测器能够通过小尺寸活检样本对 cSCLC 进行分子检测,灵敏度有所提高,这可能归因于即使仅对 SCLC 成分进行采样,也能检测到这些 NSCLC 特异性基因(图 4 E)。
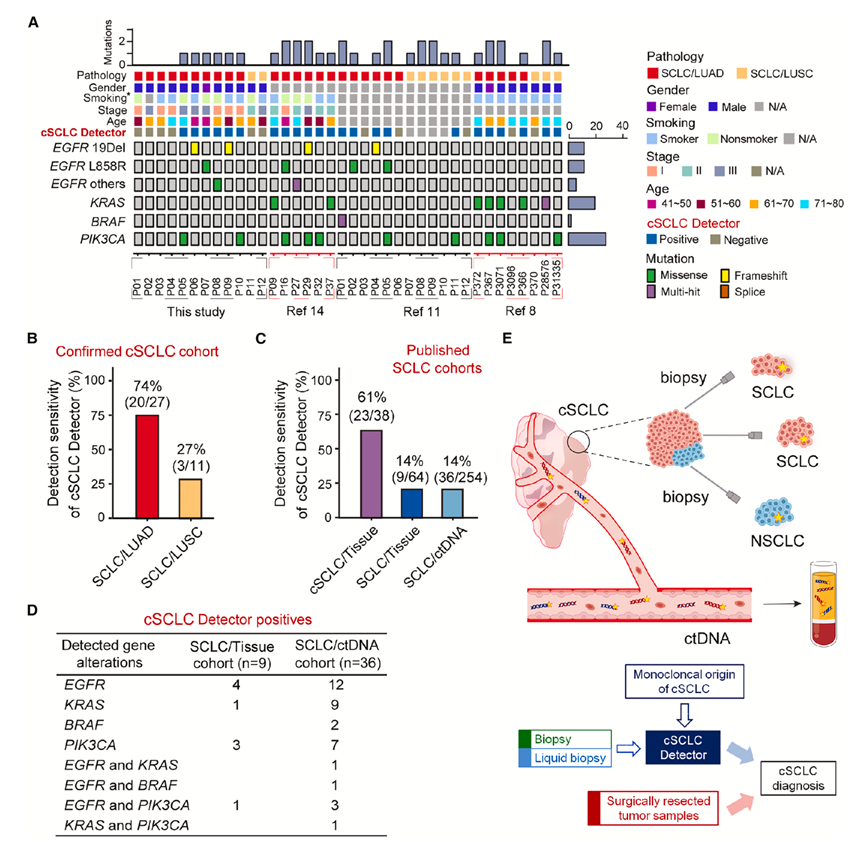
图4. cSCLC 检测器的开发和验证。
(A) cSCLC Detector 在 38 例确诊 cSCLC 患者中检测到的突变图谱。(B) cSCLC 检测器在 SCLC/LUAD、SCLC/LUSC亚组和所有确诊的 cSCLC 队列中的性能。(C) cSCLC 检测器在已发表的 SCLC 组织( n = 64)和血液 ctDNA(n = 254)队列中的性能。(D) 使用 cSCLC 检测器在中的“阳性”病例中检测到的突变:组织(n = 9)和 ctDNA。(E) 示意图显示了小活检病理学在 cSCLC 诊断中的局限性,以及 cSCLC 检测器在提高 cSCLC 检测灵敏度方面的原理。
04
空间转录组学鉴定出由侵袭性癌症相关成纤维细胞分隔的肿瘤区域
为了进一步研究cSCLC的空间分子特征及其肿瘤微环境(TME),他们对6例患者的组织切片进行了ST,每个样本的空间捕获点数量在1186至2556个之间,并鉴定出10个不同的距离(图5A)。为了注释这些聚类,他们整理了一个包含LUAD、LUSC和主要小细胞肺癌亚型(SCLC-A:ASCL1优势型;SCLC-N:NEUROD1优势型;SCLC-P:POU2F3优势型)患者的参考单细胞转录组分析(scRNA-seq)数据集。斑点注释是通过评估其与参考注释的相似性来进行的,该相似性指标整合了Jensen-Shannon散度和余弦相似度(图5B)。
在聚类分析中,聚类1(占斑点总数的21.5%)的特征是THY1、PDGFRB和胶原相关基因的高表达,表明该区域以成纤维细胞为主(图5B-C)。聚类4(5.9%)由表达CD3D(T细胞)、CD79A(B细胞)和CD68 (巨噬细胞)等标记基因的免疫细胞组成,表明该区域存在免疫浸润。聚类2(13.4%)显示出强烈的非小细胞肺癌/大细胞神经内分泌癌信号,并混合了成纤维细胞和免疫细胞。相比之下,聚类6显示出与小细胞肺癌细胞富集相关的特征,以CHGB、NCAM1、NEUROD1和ASCL1为标记(图5C)。然而,在小细胞肺癌富集聚类中未检测到POU2F3的表达,这可能是由于ST在捕获低丰度转录本方面存在固有的局限性。
将这些聚类投影到ST图像上,揭示了组织切片中清晰的肿瘤和非肿瘤区域。在所有cSCLC样本中,均显示了分离的肿瘤区域(图5D)。这些空间模式与CNA谱相一致,其中肿瘤富集区域表现出更显著的全基因组CNA(图5E)。cSCLC中不同的肿瘤区域表现出不同程度的免疫浸润。富含NSCLC/LCNEC成分的聚类2,基于免疫标志物表达显示出较高的免疫浸润(图5B-C),而富含SCLC成分的聚类6则显示出相对较低的免疫浸润,这表明肿瘤区域可能是cSCLC内免疫排斥空间异质性的基础。
有趣的是,成纤维细胞经常出现在TME内不同肿瘤区域之间并对其进行分隔(图5D),这凸显了成纤维细胞在肿瘤微环境空间结构化中的潜在作用。在具有清晰SCLC/NSCLC区室化的cSCLC样本中,这些位于边界的成纤维细胞与富含胶原的基质带相吻合,这些基质带将SCLC区域与NSCLC区域分隔开来,类似于最近在NSCLC中描述的COL11A1+ CAF屏障。先前的一项研究报道,富含癌症相关成纤维细胞亚型3(CAF S3,一种位于SCLC肿瘤边缘的侵袭性亚型)的SCLC表现出显著更差的临床预后。cSCLC中这些分隔肿瘤区域的成纤维细胞富含CAF S3亚型特征(图5F),其特征是表达细胞外基质(ECM)、胶原组织和细胞-基质黏附特征(图5G)。与 COL11A1+ myCAF 样状态一致,这些成纤维细胞表达COL11A1以及多种纤维胶原蛋白(COL1A1、COL1A2和COL3A1)、ECM/活化成纤维细胞标志物(FAP、POSTN和CTHRC1)以及基质重塑因子,如THBS2、SPARC、MMP2和MMP11,表明存在 ECM 生成、促纤维增生程序,与先前定义的 NSCLC 中的 COL11A1+ CAF 基因模块密切相关。
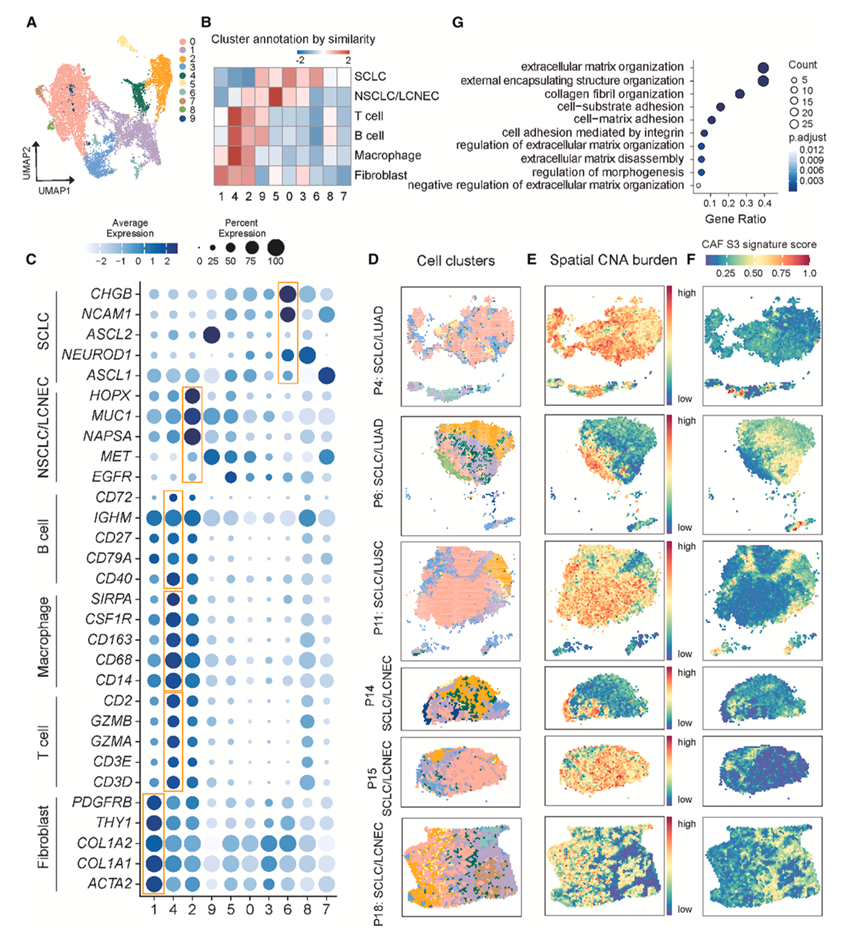
图5. 用于表征 cSCLC 微环境的 ST 斑点共嵌入。
(A) 6 个 cSCLC 样本的 ST 点的均匀流形近似和投影(UMAP)。(B) 热图展示了根据与参考单细胞RNA测序数据集(小细胞肺癌、肺腺癌和肺鳞癌)的相似性(Z评分)进行的聚类注释。(C) 用于定义细胞谱系的经典标记基因的表达。(D) 6 名患者的聚类分布空间图。(E) 不同组织学区域的空间CNA负荷。(F) CAF S3 特征在分隔肿瘤区域的成纤维细胞带中富集。(G) 定义 CAF S3 特征的基因的GO富集分析。
05
差异性肿瘤微环境(TME)特征
空间反卷积揭示了肿瘤和非肿瘤成分的空间组织结构,这与基于聚类的区域高度吻合(图6A)。将肿瘤成分反卷积为主要的SCLC亚型(SCLC-A、-N、-P)和非小细胞肺癌(NSCLC)(LUAD、LUSC)或LCNEC亚型,而非肿瘤成分包括成纤维细胞、内皮细胞和各种免疫细胞。NSCLC/LCNEC区域的特征是免疫细胞和成纤维细胞高度浸润,而SCLC区域的浸润程度极低(图6A)。为了量化这些空间模式,他们应用Ripley K函数来评估肿瘤、免疫和基质成分之间的空间关系(图6B)。在 SCLC 和 NSCLC/LCNEC 成分在空间上相互排斥的样本中,NSCLC/LCNEC 区域表现出与免疫细胞和成纤维细胞更强的聚集,而 SCLC 区域则表现出排斥浸润细胞的倾向,表明存在免疫沙漠环境。
为了验证推断的肿瘤和TME成分的空间分离,他们对7例cSCLC/LUAD亚型(P1-P7)的组织切片进行了多重免疫荧光(mIF)染色。Napsin A+ LUAD区域的特征是CD3+ T细胞和PDGFRβ +成纤维细胞的大量浸润。相比之下,相邻的突触素+ SCLC区域则表现出“冷”免疫表型,T细胞和成纤维细胞稀少(图6C)。这些正交数据证实,NSCLC成分支持浸润性TME,而SCLC成分维持免疫排斥的微环境,这与之前的临床结果一致。
在选择性治疗压力下,EGFR突变型LUAD首次观察到向类似SCLC的NE表型的转化。他们试图研究这些成分与纯SCLC和LUAD的比较,以及它们在NE转化谱系中的位置。他们整合了先前一项研究的转录组数据,该研究包括组织学转化后的LUAD和SCLC样本(合并组织学类型为T-LUAD和T-SCLC),以及转化前LUAD样本和转化后SCLC样本。由此产生的投影显示,沿对角轴存在一个连续谱,从从未转化的LUAD(右下)延伸到转化后SCLC(左上),T-LUAD和T-SCLC位于两者之间,形成清晰的NE转化轨迹(图6D)。值得注意的是,来自SCLC和LUAD区域的ST数据与T-LUAD和T-SCLC区域的吻合度更高,而非纯LUAD或SCLC的极端区域,这表明这些区域代表了具有共存LUAD和SCLC转录组特征的过渡可塑性状态(图6D)。在P6中,SCLC和LUAD区域在空间上分离,LUAD和SCLC斑点的投影转录组状态在转化谱系上更加极化。相比之下,在P4中,LUAD和SCLC成分在空间上交错分布,两个区域的转录组状态更接近NE转化轨迹的中间区域,这表明空间上更混合的肿瘤结构可能与谱系可塑性增强的中间状态相关,这种增强的谱系可塑性积极地塑造着LUAD和SCLC之间的转变。
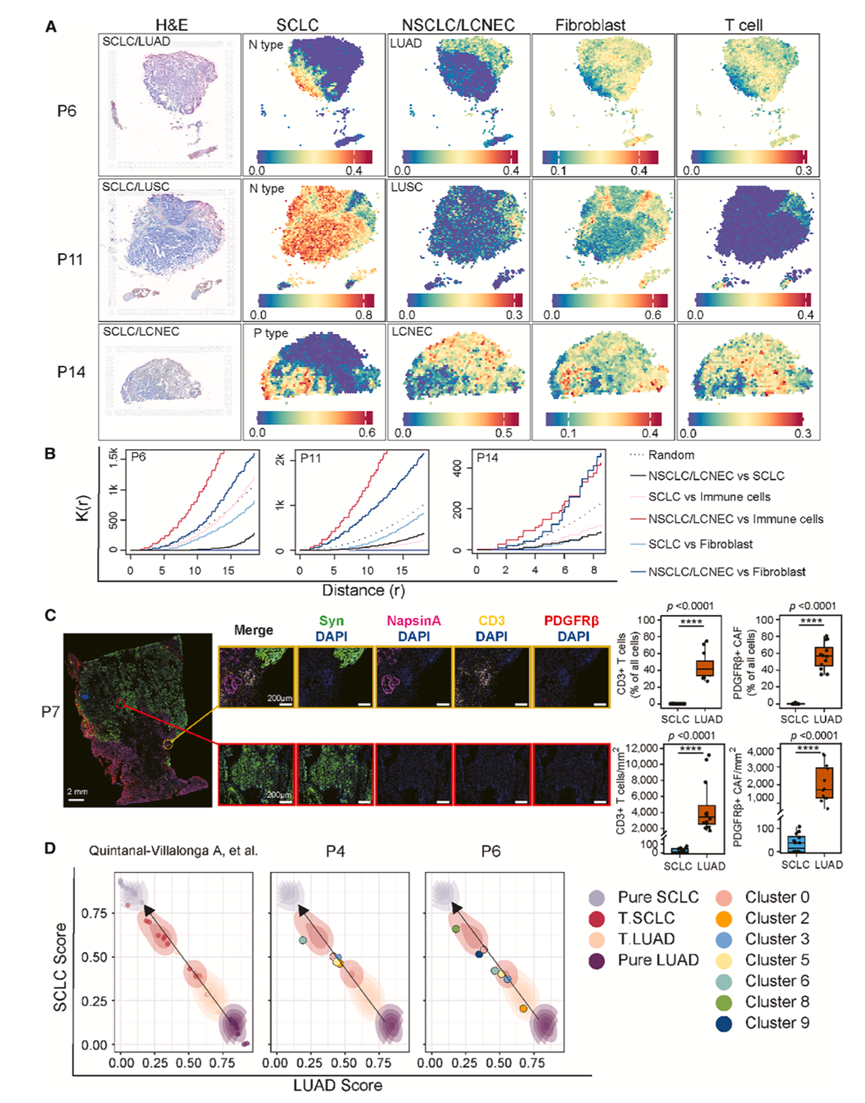
图6. 空间结构和谱系可塑性提示cSCLS 内原位LUAD 向 SCLC 的转分化。
(A) P6(小细胞肺癌/肺腺癌)、P11(小细胞肺癌/肺鳞癌)和P14(小细胞肺癌/大细胞神经内分泌癌)中细胞类型组成的空间反卷积。(B) Ripley K 分析域之间的空间关系。(C) 小细胞肺癌 (SCLC) 区域免疫排斥的 mIF 验证 (P7)。(D) LUAD 和 SCLC 转录组特征的投影。
06
不同的转录状态分析
他们对 12 例 cSCLC 样本进行了snRNA-seq 分析(图 1C),共鉴定出 150,738 个高质量细胞。这些数据与上述纯 SCLC 和非小细胞肺癌 (NSCLC) 样本的参考 scRNA-seq 数据集进行了整合。细胞聚类分析鉴定出不同的 SCLC 和 NSCLC 细胞群,其中聚类3表达 SCLC 标志物,如ASCL1、ASCL2和NEUROD1 ,聚类6表达 NSCLC 标志物,包括MUC1和NAPSA。成纤维细胞形成聚类7,其特征是表达COL1A1,而 T 细胞则聚集在聚类2,其特征是表达CD3D和CD3E。聚类5由多种免疫细胞组成,包括上部表达CD14和CD163的巨噬细胞,以及下部 B 细胞、浆细胞、中性粒细胞和肥大细胞,其中 B 细胞标志物CD79A和CD40表达尤为突出(图 7 A-B)。
从 cSCLC 样本中分离出的单个细胞核与 NSCLC、成纤维细胞和巨噬细胞聚类有显著重叠,但与 SCLC 和 T 细胞聚类的重叠有限。此外,cSCLC 的大多数细胞形成不同的细胞聚类(聚类0、1 和 4),这些细胞聚类因其全基因组拷贝数变异 (CNA) 显著升高而鉴定为恶性细胞(图 7A-C)。肺癌标志物检测显示,这些 cSCLC 细胞聚类表达 SCLC 相关基因,例如ASCL1、SCG2和ASCL2(图 7B),表明其与纯 SCLC 细胞相似,但转录状态不同。
SCLC分子亚型的特征在于ASCL1(A)、NEUROD1(N)和POU2F3(P)的互斥表达。对参考数据集的重新分析证实,P基本上与A和N互斥,而A和N之间存在有限的可塑性。相比之下,ST反卷积结果表明两种亚型的共定位更为普遍。N型和A型在P6、P11和P15中共存。在P14中,他们观察到A型和P型细胞共存(图S8);虽然POU2F3表达较低,可能是由于ST中转录本缺失所致,但其他簇状细胞样P型标记物,如ASCL2和MOCOS,与ASCL1一起清晰表达,表明A型和P型亚型均存在。然而,目前尚不清楚这反映的是不同亚型特异性细胞的混合,还是处于混合可塑状态、表现出多种纯亚型分子特征的细胞的存在。
他们利用snRNA-seq数据评估了cSCLC肿瘤细胞中A、N和P亚型的可塑性。首先,应用SPOTlight 反卷积方法对CNV定义的肿瘤细胞进行推断(图7C),从而鉴定出SCLC样细胞,并将SCLC评分>0.75且NSCLC评分<0.25的细胞归类为SCLC样单细胞。然后,通过计算亚型特异性标记的富集评分来定量这些细胞中A、N和P亚型的活性,从而在ANP亚型空间中表征每个细胞的转录特征。为了建立比较的参考,他们使用参考数据集分析了来自纯SCLC患者的代表每种SCLC亚型(A、N、P)的典型单细胞,并在三元图中可视化了它们的分布(图7D)。这些参考细胞紧密聚集在各自的A、N或P顶点,证实了纯亚型之间的清晰分离。
相比之下,来自 cSCLC 样本的 SCLC 样单细胞在三元空间中呈现广泛的分布(图 7E),许多细胞占据中间组成区域,而非聚集在单一亚型顶点。这种模式表明 cSCLC 具有显著的亚型可塑性,因为单个 SCLC 样肿瘤细胞表现出跨越多个亚型的混合表达特征,这与纯 SCLC 肿瘤细胞中观察到的互斥亚型谱形成鲜明对比。值得注意的是,这种可塑性不仅限于 NE A 和 N 亚型;他们还在单个细胞中检测到与 A 和/或 N 标记共存的强 P 型特征,例如 P14,这与 ST 反卷积结果一致(图 7E)。这表明 cSCLC 的 SCLC 样细胞中 NE 和 POU2F3 亚型之间存在可塑性,而这一现象此前在纯 SCLC 样本中未见报道。
为了探究生物程序如何沿着这条轴线演化,他们从MSigDB数据库中整理了八个功能通路类别:生长和信号通路(G1)、DNA损伤和修复(G2)、细胞周期调控(G3)、代谢通路(G4)、表观遗传调控(G5)、炎症和免疫反应(G6)、细胞死亡通路(G7)以及肿瘤微环境和组织重塑(G8)。他们使用AUCell对单细胞通路活性进行定量,并分析了按NSCLC-SCLC相对同源性评分排序的细胞,结果显示多个模块呈现协调一致的单调变化。NSCLC评分高的细胞表现出T细胞介导的细胞毒性、抗原呈递和中性粒细胞趋化性的显著富集,这与NSCLC肿瘤典型的高度炎症微环境相符。与此同时,这些细胞中细胞外基质(ECM)组织和胶原重塑特征达到峰值,这与以基质组为重点的研究结果相呼应,这些研究强调基质重塑是NSCLC进展的标志。沿着连续谱向右移动,他们观察到G2期(DNA重组、双链断裂修复)和G3期(G2/M检查点、细胞周期蛋白依赖性激酶调控)活性逐渐升高,最终在经典的SCLC细胞中达到顶峰,这凸显了细胞向增殖状态转变,并伴有基因组不稳定性增加,这与TP53和RB1普遍缺失以及SCLC对DNA损伤反应通路的依赖性的潜在影响相一致。NSCLC向SCLC的转变轨迹以细胞因子驱动的炎症代谢向氧化磷酸化 (OXPHOS) 增强和选择性自噬的转变为标志(图7F),这与 SCLC 细胞利用线粒体呼吸和脂肪酸 β-氧化快速生长,而自噬通过 NRBF2-p62 相互作用赋予化疗耐药性的事实相一致。
为了检验 cSCLC 细胞在转录水平上是否代表 NSCLC 和 SCLC 之间的真正中间状态,将 NSCLC 样本分层为 LUAD 和 LUSC,并应用二次规划,将中间状态建模为 NSCLC 和 SCLC 特征的线性组合。以纯 LUAD、LUSC 和 SCLC 单细胞作为终点,他们观察到真正的参考细胞集中在连续谱的两端,而 cSCLC 肿瘤细胞在 LUAD-SCLC 轴上的中间区域呈现单峰分布(图 7G)。这种模式表明,SCLC/LUAD 样本中的单个肿瘤细胞并非仅仅反映肿瘤成分的逐渐变化(即 LUAD 样细胞逐渐由SCLC 样细胞取代),而是确实占据了 NE 转化轴上的中间过渡状态,这证实了在 P4 和 P6 中观察到的空间过渡状态确实是中间/混合状态,而不是两个固定细胞群的简单混合。有趣的是,在具有 SCLC/LUSC 亚型的 cSCLC 样本中,他们观察到了类似的模式,肿瘤细胞在 LUSC-SCLC 轴的中间区域再次呈现单峰分布而非双峰分布(图 7G),表明这些病例中存在混合状态,并提示 SCLC/LUSC 亚型中也可能发生沿 NE 转化轴的可塑性转变,类似于 SCLC/LUAD。总而言之,这些发现支持以下假设:cSCLC 的单个肿瘤细胞在完全获得 SCLC 表型之前,会通过中间/混合状态发生 NE 转化。
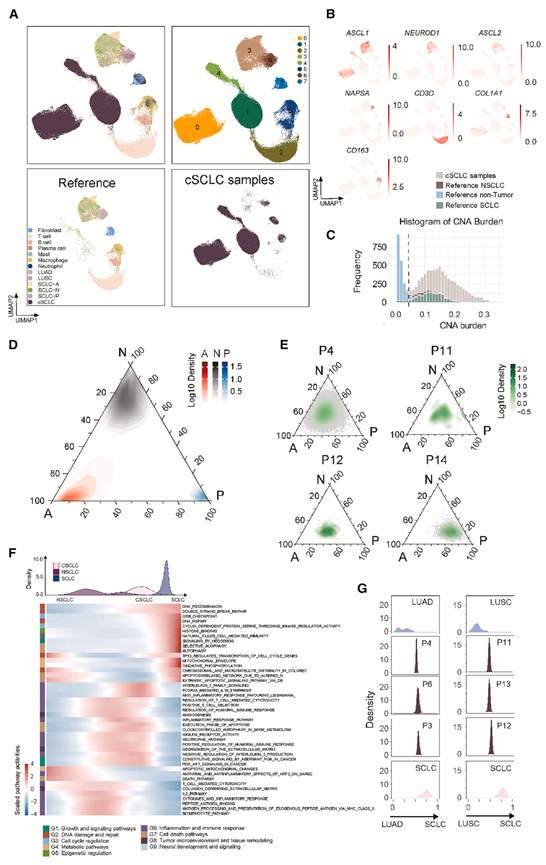
图7. snRNA-seq揭示了cSCLC肿瘤细胞的转录可塑性。
(A) 本研究和公共数据集中的snRNA-seq的UMAP(左上),以及同一UMAP中的细胞聚类(右上)。来自公共参考数据集(左下)和cSCLC(右下)的细胞的分离嵌入。(B) 标记基因表达。(C) CNA负担分布。(D) 纯 SCLC 细胞在 A/N/P 空间中的三元图。(E) P4、P11、P12 和 P14 的三元图。(F) 热图显示单个细胞的标准化通路活性评分。(G) 典型 LUAD、LUSC 和 SCLC 样本(上、下图)以及单个 cSCLC 样本(中间图,P3–P13)的二次规划衍生 SCLC-NSCLC 同一性评分的密度。
+ + + + + + + + + + +
结 论
本研究对19例未经治疗的cSCLC肿瘤进行了多组学分析。不同的组织学成分具有单克隆起源,而差异则与不同的突变和拷贝数变异模式相关。本项研究结果定义了空间上相互排斥或交错分布的肿瘤区域,这些区域具有不同的TME和免疫图谱;富含成纤维细胞的边界区域可能影响TME和治疗反应。本研究发现了谱系可塑性,包括腺癌向小细胞肺癌的转分化以及小细胞肺癌亚型的共存,并开发了 cSCLC Detector,这是一种基于突变的灵敏检测方法,可提高组织和液体活检中 cSCLC 的检出率。这些发现揭示了 cSCLC 的演变和异质性,强调了针对这种侵袭性亚型制定个性化诊断和治疗策略的必要性。
+ + + + +



 English
English


